Preparation, catalytic property and antibacterial property of Ag@Fe3O4 core-shell composite nanomaterials
-
摘要: 采用“一锅法”制备纳米核-壳结构的Ag@Fe3O4复合材料。利用TEM、XRD、UV-vis DRS、振动探针式磁强计(VSM)对Ag@Fe3O4复合材料进行表征。以甲基橙为目标污染物,研究Ag@Fe3O4复合材料在过量NaBH4介质中加氢还原的催化活性,并探讨其催化机制;以单质Ag和Fe3O4作参比,研究Ag@Fe3O4复合材料对金黄色葡萄球菌和大肠杆菌的抑菌性能。结果表明,在10 min内,Ag@Fe3O4复合材料对甲基橙的加氢还原催化率为98%以上,且活性Ag转移电子至甲基橙的N=N键,使其断裂还原成对氨基苯磺酸钠和对二氨基苯;抑菌实验表明,Ag@Fe3O4复合材料比单质Ag具有更强的抑菌活性,并对细胞壁中含有更薄的磷脂双分子层的大肠杆菌更为敏感。Abstract: The Ag@Fe3O4 composites with nano core-shell structure were successfully prepared by a one-pot method. The resulting Ag@Fe3O4 composites were characterized by TEM, XRD, UV-vis DRS and vibrating sample magnetometry (VSM). The catalytic performance and mechanism of Ag@Fe3O4 composites were investigated by photometrically monitoring the reduction of methyl orange in the presence of excess of NaBH4. Furthermore, the antibacterial of Ag@Fe3O4 composites against Staphylococcus aureus (S.aureus) and Escherichia coli (E.coli) was studied by the paper diffusion experiment using Ag and Fe3O4 as the references. The results indicate that over 98% of methyl orange is catalytically degraded within 10 min. This superior catalytic activity may be resulted from transferring electron to N=N bond by Ag, thereby causing N=N fracture and generating sodium 4-aminobenzenesulfonate and p-diaminobenzene. Antibacterial experiment shows that Ag@Fe3O4 composites more excellent bacteriostatic activity than Ag and is more sensitive to E.coli than to S.aureus. The main reason can be ascribed to the fact that phospholipid bilayer in cell wall of E.coli is thinner than that of S.aureus.
-
Keywords:
- composite materials /
- Ag /
- catalytic /
- inhibition /
- the Core-shell type /
- Fe3O4
-
纳米银颗粒(SNP)在可见光区域具有较强的等离子共振吸收,吸收可见光后,表面等离子共振体易成为核结点而具有均相催化和多相催化性能,其依据介质中溶质的结构特性而具有加氢催化和氧化催化活性[1-2],且表面电子易与介质生成过氧化物或强氧化物而具备一定的杀菌性[3-5]。SNP的杀菌性能不同于传统抗生素,大多数抗生素抑菌原理是结合细菌特定的结合位点导致细菌失活[6],无法对细菌造成根本性破坏,细菌通过基因突变或自身修复功能产生特异性蛋白质来适应抗生素产生大量的耐药菌。研究结果表明,SNP可结合蛋白质中的半胱氨酸形成强的配合物而改变蛋白质空间结构,细菌中的细胞壁、细胞膜、核酸、呼吸酶等细胞器都含有大量半胱氨酸,SNP破坏细菌细胞器中蛋白质空间结构,使发生不可逆变性,导致细菌死亡[6-7]。但SNP的催化和抑菌性能与比表面积有关,比表面积越大,催化和抑菌性能越强,但比表面积越大,表面能越高,Ag越易团聚,限制了SNP的催化和抑菌性能[8],同时SNP回收难、制备方法复杂、循环利用率低等缺点限制了SNP的应用。
Fe3O4作为重要的尖晶型磁性材料被广泛应用于光热治疗、磁性选矿和生物材料等领域[9-10]。如以Fe3O4为核,在表面负载Ag可以提高其在近红外光学性能,从而提高催化活性,且复合材料具备一定的抑菌性能[2]。Olena等[10]合成Fe3O4@Ag-抗生素复合材料,将Ag负载在Fe3O4表面不仅可以解决Ag团聚的问题,且分离简单,回收方便,利用Ag杀菌彻底性,与抗生素结合对耐药菌产生很强的毒理性,但载体表面的Ag粒子无法均匀释放,通过修饰将Ag负载在基体表面易脱落。Jiang等[11]研究了SiO2@Ag复合材料对甲基橙、曙红和罗丹明的加氢催化活性中Ag的稳定性和比表面积对催化剂效率的影响,结果表明,在介质中比表面积和粒子稳定性等均影响其加氢催化性能,但加氢后的产物未进行讨论,且大多数研究者单方面增加其抑菌活性或催化性能而未研究其双重活性。本研究以AgNO3和Fe(NO3)3为原料,利用两种盐的电极电位EAg+/Ag=+0.799 eV (标准氢电极电位为参比)大于EFe3+/Fe2+=+0.77 eV,在还原介质中Ag的生成速率大于Fe2+的原理,采用“一锅法”制备以Ag为核,在其表面包覆Fe3O4合成纳米核-壳型Ag@Fe3O4复合材料[12]。不仅可以解决Ag团聚的问题,提高其稳定性,也可提高Ag的催化性能和抑菌活性,且可调节催化反应速率。以甲基橙为目标污染物研究加氢催化活性并简单验证其产物[13],采用金黄色葡萄球菌(S.aureus)和大肠杆菌(E.coli)为模式菌[14],以化学方法合成的单质Ag为参比,研究目标产物的抑菌性能,并探讨其机制。
1. 实验材料及方法
1.1 原材料
Fe(NO3)3·9H2O、NaCl、乙二醇、醋酸钠(NaAc),天津市大茂化学试剂厂;聚乙烯吡咯烷酮K30 (PVP)、抗坏血酸、甲基橙,天津市致远化学试剂有限公司;AgNO3、NaOH、NaBH4,广州市鑫铂化工有限公司;酵母浸粉、胰蛋白胨、琼脂,上海展云化工有限公司;金黄色葡萄球菌(S.aureus)、大肠杆菌(E.coli),陕西省食用菌研究所。
1.2 核-壳型Ag@Fe3O4复合材料和Fe3O4的制备
采用“一锅法”制备Ag@Fe3O4[12]。准确称取1.612 g Fe(NO3)3·9H2O、0.1 g AgNO3和2.87 g NaAc分散在40 mL乙二醇中,超声分散均匀。将其转入反应釜中,在200℃下反应10 h,得到目标产物(通过调节AgNO3和Fe(NO3)3·9H2O的浓度和时间控制Ag的粒径和Fe3O4的厚度)。
Fe3O4的制备重复以上操作步骤,不添加AgNO3,将溶液转入反应釜中,在200℃下反应10 h。离心分离,水洗3次后得到最终目标产物,将其储存于干燥箱中备用。
1.3 纳米银颗粒(SNP)的制备
首先,准确称取170 mg PVP和170 mg AgNO3分散于40 mL超纯水中,然后逐滴加入400 µL 5 mol/L NaCl溶液,黑暗环境下搅拌20 min,得到AgCl胶体。
将320 mL 50 mmol/L的抗坏血酸缓慢加入到44 mL 0.5 mol/L的NaOH溶液中。反应10 min后,逐滴滴入上述AgCl溶胶,在避光条件下反应2 h。反应结束后,于12000 r/min转速下离心并水洗3次[15],去除上清液后,分离得到目标产物(通过调节NaOH的浓度控制SNP的粒径),将其储存于干燥箱中备用。
1.4 测试与表征
利用TEM (Tecnai,FEI)观察和分析样品的微观结构;采用D8 ADVANCE X射线粉末衍射仪(德国BRUKER)测试Ag@Fe3O4复合材料晶型结构,CuKα靶(λ=0.154 nm),电压为40 kV,电流为35 mA,扫描速度2θ=7°。采用紫外-可见漫反射吸收光谱(Cray 100)测试材料的元素结构,扫描速率为200 nm/min,扫描范围为200~800 nm。
1.5 磁性能测试
采用7407型振动样品磁强计(美国Lake Shore公司)测定Ag@Fe3O4复合材料磁化曲线。测试温度为20℃,磁场范围为–15000~15000 Oe (1Oe=10~4 T)
1.6 催化实验
催化活性的评估为NaBH4还原甲基橙,甲基橙对紫外-可见光具有响应,且吸收峰的强弱和浓度呈正相关。因此,采用紫外-可见分光光度计进行监测,在4 mL的石英比色皿进行。取1 mL 0.25 mmol/L甲基橙溶液和2 mL 0.02 mol/L NaBH4混合均匀并加入比色皿中,滴加0.2 mL 0.5 mg/mL催化剂,在扫描范围为200~800 nm,每间隔2 min监测465 nm处吸光度的变化[16],计算降解率R如下:
R=(C0−C)/C0×100% 式中:C0为初始浓度;C为残留浓度。
1.7 抑菌实验
以金黄色葡萄球菌(S.aureus)和大肠杆菌(E.coli)为模式菌,采用滤纸片扩散法[14]评价复合材料的抑菌性能。
首先把S.aureus和E.coli隔夜活化,无菌环境下用灭过菌的生理盐水把活化好的菌悬液稀释到5×105 CFU (Colony-forming units)/mL,取50 µL均匀涂布在灭过菌的固体LB培养基上,用灭过菌的超纯水把材料稀释成不同浓度。将沾有3 µL不同材料的无菌滤纸放置在接过菌的LB培养基上,37℃培养12 h观察结果。
2. 结果和讨论
2.1 Ag@Fe3O4复合材料的微观形貌
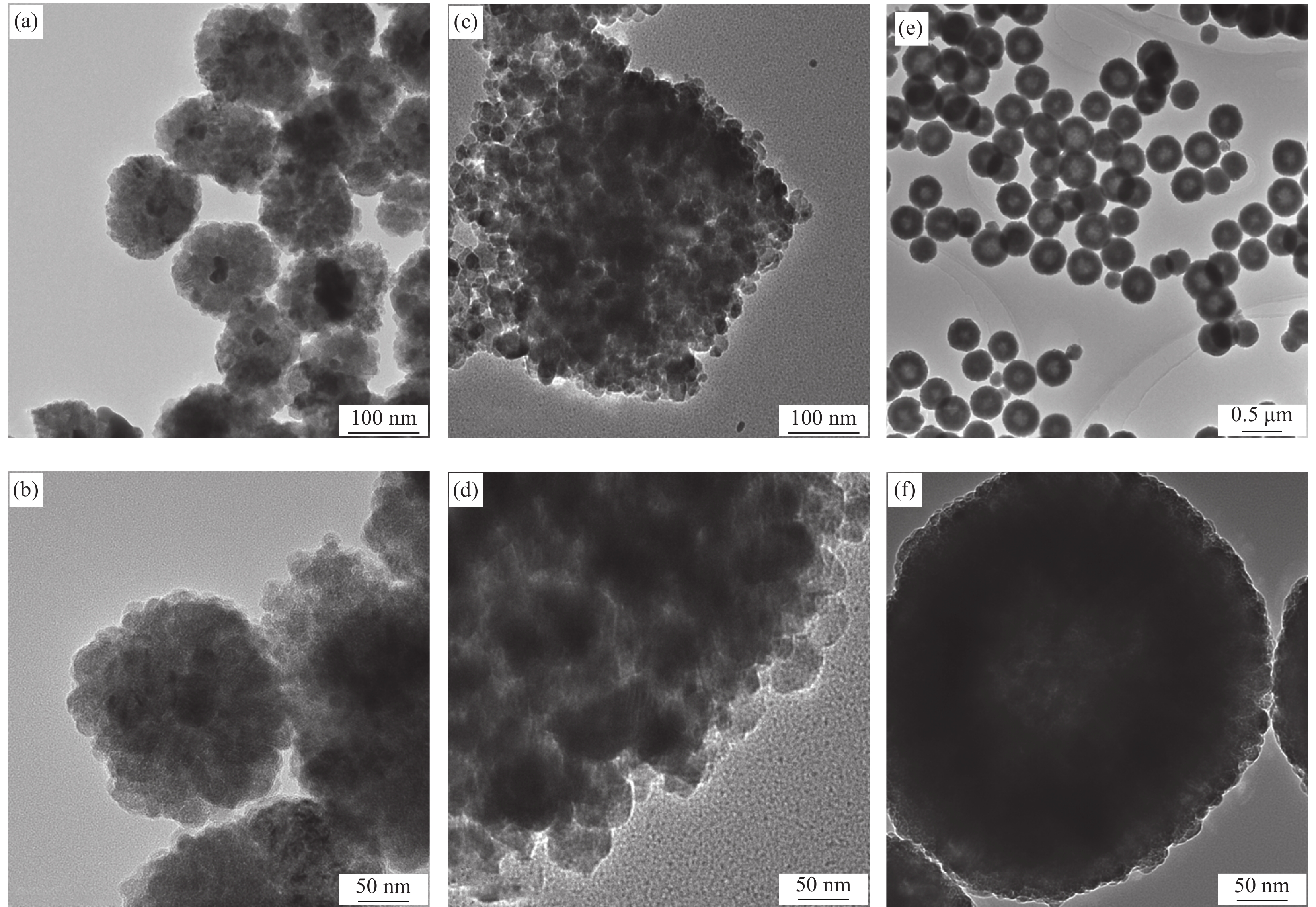
图1为Ag@Fe3O4复合材料、SNP和Fe3O4的TEM图像。由图1(a)和图1(b)可知,单分散Ag@Fe3O4复合材料为双层球结构,内球Ag粒径为(25±5) nm,外球Fe3O4厚度为(75±5) nm,表面粗糙,有明显孔隙。由图1(c)和图1(d)可知,SNP为球形结构,粒径为(25±5) nm。由图1(e)和图1(f)可知,Fe3O4为单分散的球形结构,表面光滑,分散均匀,粒径为(500±25) nm。与Ag@Fe3O4复合材料相比,SNP明显发生团聚现象,其原因是由于SNP在介质中易团聚所致,证明在Ag表面包覆Fe3O4可提高其稳定性。对比Ag@Fe3O4和Fe3O4发现,Ag@Fe3O4复合材料表面为介孔状,说明通过此方法合成的Ag@Fe3O4复合材料为单分散双层球材料。
2.2 Ag@Fe3O4复合材料的微观结构
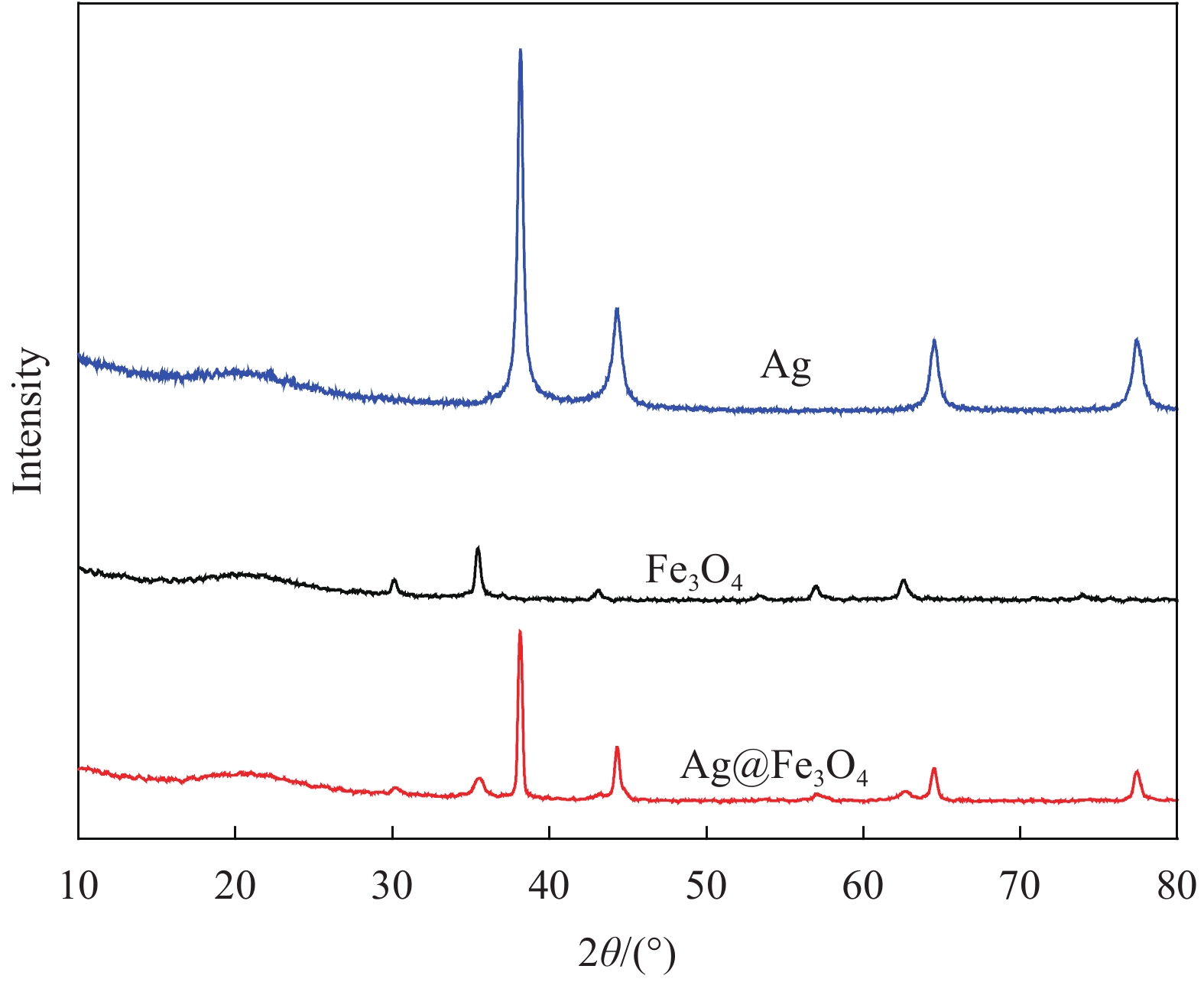
图2为Fe3O4、Ag和Ag@ Fe3O4复合材料的XRD图谱。可以看到,存在尖锐的X射线衍射峰,说明产物均具有良好的晶型。Fe3O4在2θ=30.2°、35.8°、43.1°、53.4°、57.0°和62.6°处分别对应Fe3O4的(220)、(311)、(422)、(511)和(440)晶面[17],与卡片JCPDS NO.79-0419相对应,其合成的Fe3O4为尖晶型,且无杂峰出现,说明该条件下合成的Fe3O4为纯相。Ag在2θ=38.9°、44.28°、64.43°和77.38°处依次对应面心立方Ag (JCPDS 4-0783)的(111)、(200)、(230)和(331)晶面[18],证明合成的Ag为立方相晶体,而Ag@Fe3O4复合材料同时含有Fe3O4和Ag的衍射峰,说明目标产物中同时含有尖晶型Fe3O4和立方相Ag。证明产物双层球形型Ag@Fe3O4复合材料中Ag和Fe3O4均为晶型。
2.3 Ag@Fe3O4复合材料的元素组成
图3为Fe3O4、SNP和Ag@Fe3O4复合材料的UV-vis漫反射吸收图谱。可知,Fe3O4没有出现吸收峰,SNP和Ag@Fe3O4复合材料在402 nm和475 nm处有强的吸收峰,由于Fe3O4在可见光区域没由吸收峰[19],单质Ag的特征吸收峰为400~420 nm[15],而Ag@Fe3O4复合材料中Ag表面发生等离子共振,电子转移而产生红移[20],红移的位置由Fe3O4的厚度和Ag粒径决定。通过TEM、XRD和UV-Vis可以证明,合成的Ag@Fe3O4复合材料为核-壳双层球结构,且以单质Ag为核,Fe3O4包覆在Ag表面形成双层球结构。其原理是电极电位EAg+/Ag=+0.799 eV (标准氢电极电位为参比)大于EFe3+/Fe2+=+0.77 eV,在反应介质中Ag+还原成Ag0的速率比Fe3+还原成Fe2+更快,因此单质Ag先成核,Fe3O4以Ag为晶种生成核-壳型Ag@Fe3O4复合材料[12]。
2.4 Ag@Fe3O4复合材料的磁性能
图4为Fe3O4和Ag@Fe3O4复合材料的饱和磁强度。可知,Fe3O4的饱和磁强度Ms为74.0 emu/g。Ag@Fe3O4复合材料Ms为60.1 emu/g,由于SNP没有磁性,稀释了Fe3O4的磁性,导致复合材料磁性有所下降[21],但Ag@Fe3O4复合材料仍具有很强的磁性。
2.5 Ag@Fe3O4复合材料的催化性能
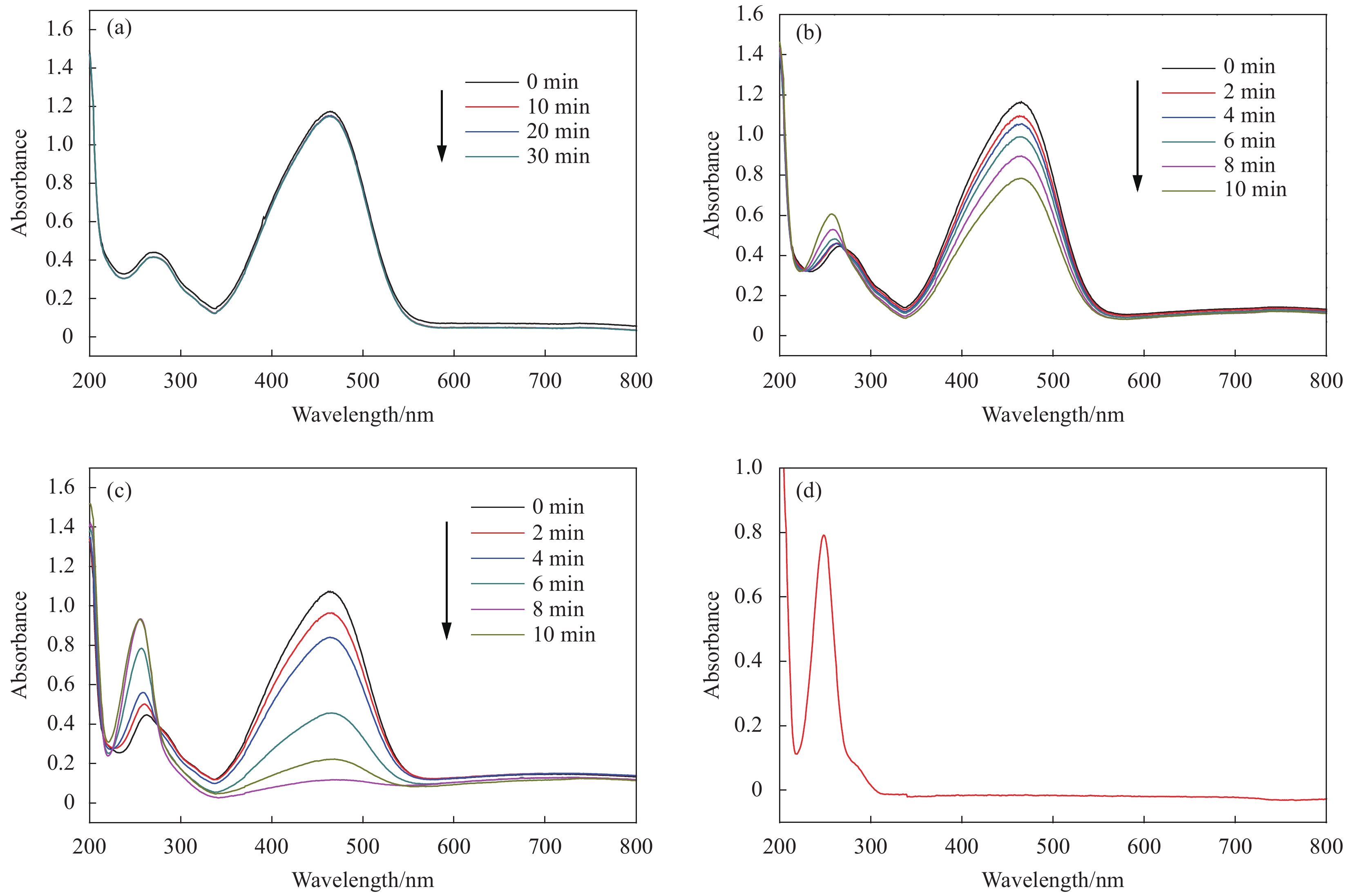
图5为Fe3O4、SNP和Ag@Fe3O4复合材料对甲基橙的加氢催化活性测试结果。由图5(a)可知,甲基橙峰面积/吸光度随着时间增加在30 min内几乎无变化。由图5(b)可知,染料峰面积/吸光度逐渐降低,为降解过程,在10 min后降解约46% (以染料起始浓度C0为参比),具体材料用量如表1所示。由图5(c)可知,在10 min内几乎完全降解,还原催化率为98%以上。通过对比可知,Fe3O4对甲基橙的加氢无催化活性,Ag@Fe3O4复合材料的催化活性明显强于SNP,其主要原因是由于SNP在介质中易团聚(TEM图像可以清楚地看出)。以Ag为核,将Fe3O4负载在Ag表面可提高其稳定性。Ag@Fe3O4复合材料在降解甲基橙过程中,前6 min降解速率慢,6 min后速度加快,其原因是由于材料先通过Fe3O4壳吸附染料和NaBH4,达到吸附平衡后,金属Ag作为催化剂加速甲基橙和NaBH4的加氢反应。此外,从图5(b)和图5(c)可以看出,在249 nm处出现新的吸收峰,且随着甲基橙的浓度降低而升高,对应于甲基橙的降解产物,其产物为对氨基苯环酸钠[16],为了验证该产物,对氨基苯环酸钠[22]进行紫外-可见光谱分析,其紫外特征吸收峰为249 nm (如图5(d)所示),证明Ag对甲基橙降解产物中含对氨基苯磺酸钠。甲基橙直接烷化的机制如图6所示[11,16]。可知,Ag在还原介质中转换电子的效率决定其催化性能,而电子转换效率由Ag粒子表面吸附的亲核试剂NaBH4和亲电试剂甲基橙的浓度所致,吸附浓度越大,催化效率高。原则上Ag粒径越小,表面能越大,吸附甲基橙和NaBH4越多,但Ag粒径越小越易团聚。SNP由于团聚和吸附同时进行,导致体系不稳定,表面活位点减少,降低了催化效率,而Ag@Fe3O4复合材料的Ag被Fe3O4包覆,不仅增加了Ag的稳定性,且其形貌增加了Ag的活性位点,利于BH4–通过孔道输送电子与Ag结合形成过渡态,过渡态和甲基橙中的N=N双加氢还原成对氨基苯磺酸和对二氨基苯[16],释放出单质Ag,因此Ag作为电子转移基体从BH4–转移到N=N而具备加氢催化活性[16,23]。此结果证明,Ag@Fe3O4复合材料对甲基橙具有强的吸附性和加氢催化性能,且强磁性利于目标产物回收利用,把Fe3O4包覆在Ag表面解决了Ag团聚的难题,不仅增加了Ag催化降解的活性位点,且显著提高其催化性能,防止暴露在空气中氧化和克服其使用难以循环利用的问题。
表 1 实验所用材料、剂量和不同材料对甲基橙的催化效率Table 1. Table information of experimental material, dosage and catalytic efficiency of different materials for methyl orangeSample Concentration Volume/mL Catalytic efficiency R/% Methyl orange 0.25 mmol/L 1 — NaBH4 0.02 mol/L 2 — Fe3O4 0.5 mg/mL 0.2 0 Ag 0.5 mg/mL 0.2 46 Ag@Fe3O4 0.5 mg/mL 0.2 98 Note: R=(C0–C)/C0×100%, C0—Initial concentration, C—Residual concentration. 2.6 Ag@Fe3O4复合材料的抑菌性能
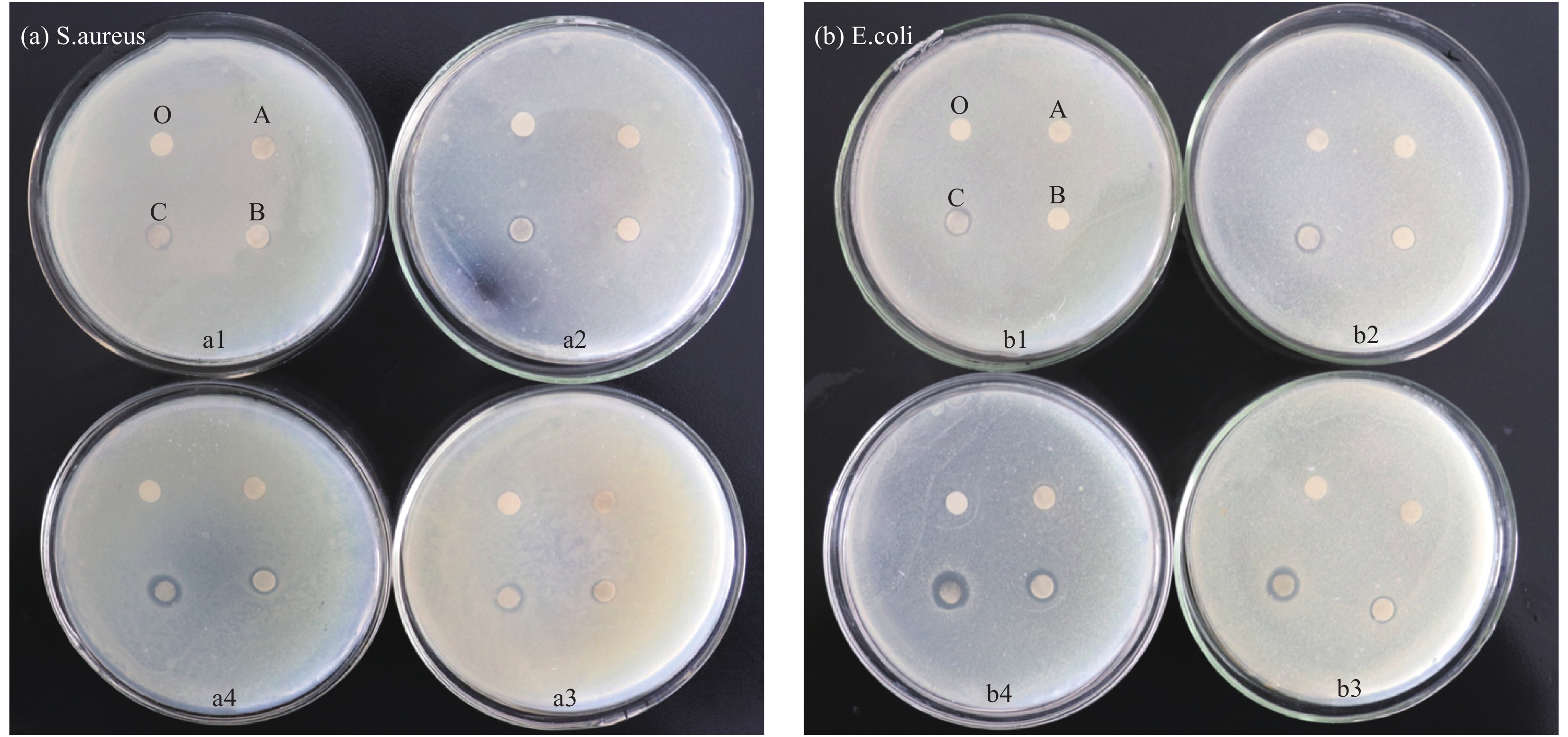
图7为不同浓度的水、SNP、Fe3O4和Ag@Fe3O4复合材料对大肠杆菌(E. coli)和金黄色葡萄球菌(S. aureus)的滤纸片扩散照片。可知,水和Fe3O4没有形成透明的抑菌圈,SNP和Ag@Fe3O4复合材料具有明显的抑菌圈,相比于SNP和Ag@Fe3O4复合材料,水和Fe3O4没有抑菌性,随着浓度的增大。SNP和Ag@Fe3O4复合材料的抑菌圈越来越大,说明抑菌活性随浓度增加而增强。且同菌同浓度下,Ag@Fe3O4复合材料的抑菌圈大于SNP,说明Ag@Fe3O4复合材料的抑菌活性比SNP更强,由于SNP在介质中易团聚,降低了Ag的抑菌性能。同浓度下,Ag@Fe3O4复合材料对E. coli的抑菌圈更大,说明其对E. coli的杀菌活性更强,具体抑菌机制如图8所示。由于E. coli和S.aureus细胞壁中都具有蛋白质和磷脂双分子层,E. coli细胞壁中含有更多的脂多糖和更少的磷脂分子层,S.aureus则含有更多的磷脂分子层和更少的磷壁酸,Ag@Fe3O4复合材料缓慢释放出Ag,Ag在介质溶液中释放电子生成Ag+和微量自由基氧化物或强氧化物(需氧型细菌体内均含有超氧化物歧化酶(SOD),SOD可清除细菌壁外微量自由基氧化物),Ag和Ag+很难渗透含有大量磷脂双分子层的S.aureus,但更容易和含巯基的膜蛋白和通道蛋白等结合,E. coli含有大量的蛋白质,因此Ag@Fe3O4复合材料对E. coli更为敏感。此外,更多的Ag进入细胞内部和细胞质反应生成活性氧(ROS),Ag+可改变SOD的空间结构使其失活,细胞壁外大量的自由基氧化物和强氧化物、ROS、Ag和Ag+协同进入细胞内部,破坏细胞器[24-25],和DNA上的半胱氨酸反应改变核酸的一级结构、改变细菌渗透压平衡等,导致细菌死亡,且不产生抗药性。
![]() 图 7 不同浓度的水、SNP、Fe3O4和Ag@Fe3O4复合材料对大肠杆菌(E. coli)和金黄色葡萄球菌(S. aureus)的滤纸片扩散照片Figure 7. Inhibition zones of as-synthesized water, SNP, Fe3O4e and Ag@Fe3O4 composite with different concentrations against Escherichia coli (E. coli) and Staphylococcus aureus (S. aureus)O—Water; A—SNP; B—Fe3O4; C—Ag@Fe3O4; a1, b1—10 µg/mL; a2, b2—20 µg/mL; a3, b3—30 µg/mL; a4, b4—40 µg/mL
图 7 不同浓度的水、SNP、Fe3O4和Ag@Fe3O4复合材料对大肠杆菌(E. coli)和金黄色葡萄球菌(S. aureus)的滤纸片扩散照片Figure 7. Inhibition zones of as-synthesized water, SNP, Fe3O4e and Ag@Fe3O4 composite with different concentrations against Escherichia coli (E. coli) and Staphylococcus aureus (S. aureus)O—Water; A—SNP; B—Fe3O4; C—Ag@Fe3O4; a1, b1—10 µg/mL; a2, b2—20 µg/mL; a3, b3—30 µg/mL; a4, b4—40 µg/mL3. 结 论
(1)基于电极电位EAg+/Ag=+0.799 eV大于EFe3+/Fe2+=+0.77 eV,在介质中单质Ag生成速率高于Fe3O4的原理,采用“一锅法”合成核-壳型Ag@Fe3O4复合材料。通过TEM、XRD、UV-vis、振动探针式磁强计(VSM)对材料进行形貌和晶型分析,制备的Ag@Fe3O4复合材料为双层球形核-壳复合材料,不仅可解决Ag团聚的问题,且回收方便。
(2)由于Ag具有丰富的表面等离子体,在质子介质中转换电子而具有加氢催化性能,在溶液中释放电子可增强抑菌活性。在探究加氢催化活性和抑菌性能中Ag@Fe3O4复合材料表现出对甲基橙具有较高的加氢催化性能,其降解甲基橙的产物为对氨基苯磺酸钠和对二氨基苯。
(3) Ag@Fe3O4复合材料对
大肠杆菌(E. coli)和金黄色葡萄球菌(S. aureus)均具有更好的抑菌性,且对E. coli更为敏感,因此其优越的催化性能和抑菌活性可应用于污水处理、医疗器械等领域。 -
图 7 不同浓度的水、SNP、Fe3O4和Ag@Fe3O4复合材料对大肠杆菌(E. coli)和金黄色葡萄球菌(S. aureus)的滤纸片扩散照片
Figure 7. Inhibition zones of as-synthesized water, SNP, Fe3O4e and Ag@Fe3O4 composite with different concentrations against Escherichia coli (E. coli) and Staphylococcus aureus (S. aureus)
O—Water; A—SNP; B—Fe3O4; C—Ag@Fe3O4; a1, b1—10 µg/mL; a2, b2—20 µg/mL; a3, b3—30 µg/mL; a4, b4—40 µg/mL
表 1 实验所用材料、剂量和不同材料对甲基橙的催化效率
Table 1 Table information of experimental material, dosage and catalytic efficiency of different materials for methyl orange
Sample Concentration Volume/mL Catalytic efficiency R/% Methyl orange 0.25 mmol/L 1 — NaBH4 0.02 mol/L 2 — Fe3O4 0.5 mg/mL 0.2 0 Ag 0.5 mg/mL 0.2 46 Ag@Fe3O4 0.5 mg/mL 0.2 98 Note: R=(C0–C)/C0×100%, C0—Initial concentration, C—Residual concentration. -
[1] SONG S Y, LIU R X, ZHANG Y, et al. Colloidal noble-metal and bimetallic alloy nanocrystals: A general synthetic method and their catalytic hydrogenation properties[J]. Chemistry: A European Journal,2010,16(21):6251-6256. DOI: 10.1002/chem.200903279
[2] PRADHAN N, ANLI P. Catalytic reduction of aromatic nitro compounds by coinage metal nanoparticles[J]. Langmuir,2001,17(5):1800-1802. DOI: 10.1021/la000862d
[3] MEI L, LU Z T, ZHANG X G. Polymer-Ag nanocomposites with enhanced antimicrobial activity against bacterial infection[J]. ACS Applied Materials & Interfaces,2014,6(18):15813-15821. DOI: 10.1021/am502886m
[4] CONG Y, XIA T, ZOU M, et al. Mussel-inspired polydopamine coating as aversatile platform for synthesizing polystyrene/Ag nanocomposite particles with enhanced antibacterial activities[J]. Journal of Materials Chemistry B,2014,2(22):3450-3461.
[5] DENG H, MCSHAN D, ZHANG Y, et al. Mechanistic study of the synergistic antibacterial activity of combined silver nanoparticles and common antibiotics[J]. Environmental Science & Technology,2016,50(16):8840-8848.
[6] ZHOU W H, JIA Z J, XIONG P, et al. Bioinspired and biomimetic AgNPs/gentamicin-embedded silk fibroin coatings for robust antibacterial and osteogenetic applications[J]. ACS Applied Materials & Interfaces,2017,9(31):25830-25846. DOI: 10.1021/acsami.7b06757
[7] ZHENG K Y, MAGDIEL I, SETYA W, et al. Antimicrobial cluster bombs: Silver nanoclusters packed with daptomycin[J]. ACS Nano,2016,10(8):7934-7942. DOI: 10.1021/acsnano.6b03862
[8] HAMIDREZA A, EHSAN N K, SAMANEH K, et al. Multifunctional thin-film nanofiltration membrane incorporated with reduced graphene oxide@TiO2@Ag nanocomposites for high desalination performance, dye retention, and antibacterial properties[J]. ACS Applied Materials & Interfaces,2019,11(26):23535-23545. DOI: 10.1021/acsami.9b03557
[9] DAVIT J, WU Y T, WANG D. Preparation and self-assembly of dendronized janus Fe3O4-Pt and Fe3O4-Au heterodimers[J]. ACS Nano,2017,11(8):7958-7966. DOI: 10.1021/acsnano.7b02485
[10] OLENA I C, JUSTYNA J S, EERSON C, et al. Fourier transform infrared and Raman spectroscopy studies on magnetite/Ag/antibiotic nanocomposites[J]. Applied Surface Science,2016,364:400-409. DOI: 10.1016/j.apsusc.2015.12.149
[11] JIANG Z J, LIU C Y, SUN L W, et al. Catalytic properties of silver nanoparticles supported on silica spheres[J]. Journal of Physical Chemistry B,2005,109(5):1730-1735. DOI: 10.1021/jp046032g
[12] ZHANG Y X, DING H L, LIU Y Y, et al. Facile one-step synthesis of plasmonic/magnetic core/shell nanostructures and their multifunctionality[J]. Journal of Materials Chemistry,2012,22(21):10779-10786. DOI: 10.1039/c2jm16293h
[13] PRADAN N, PAL A, PA T, et al. Silver nanoparticle catalyzed reduction of aromatic nitro compounds[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects,2002,196(2-3):247-257.
[14] 石振武, 郭少波, 薛群虎. 纳米复合材料Ag@TiO2@SiO2制备、光催化及其抑菌性能[J]. 无机材料学报, 2016, 31(5):466-472. SHI Z W, GUO S B, XUE Q H. Preparation, photocatalytic property and antibacterial property of Ag@TiO2@SiO2 composite nanomaterials[J]. Journal of Inorganic Materials,2016,31(5):466-472(in Chinese).
[15] CHEN B, JIAO X L. Size-controlled and size-designed synthesis of nano/submicrometer Ag particles[J]. Crystal Growth & Design,2010,10(8):3379-3386.
[16] SAKIR M, ONSES M S. Solid substrates decorated with Ag nanostructures for the catalytic degradation of methyl orange[J]. Results in Physics,2019,12:1133-1143. DOI: 10.1016/j.rinp.2018.12.084
[17] XU Z C, HOU Y L, SUN S H. Magnetic core/shell Fe3O4/Au and Fe3O4/Au/Ag nanoparticles with tunable plasmonic properties[J]. Journal of the American Chemical Society,2007,129(28):8698-8699. DOI: 10.1021/ja073057v
[18] AMANULLA M F, KULANDAIVELU B J, MORUKATTU G, et al. Biogenic synthesis of silver nanoparticles and their synergistic effect with antibiotics: A study against gram-positive and gram-negative bacteria[J]. Nanomedicine: Nanotechnology, Biology, and Medicine,2010,6(1):103-109. DOI: 10.1016/j.nano.2009.04.006
[19] PADMANABH J, ZHOU Y, TEVHIDE O A, et al. Quantitative SERS-based detection using Ag-Fe3O4 nanocomposites with an internal reference[J]. Journal of Materials Chemistry C,2014,2(46):9964-9968. DOI: 10.1039/C4TC01550A
[20] ANANDA S, GRISESER F, ASHOKKUMAR M. Sonochemical Synthesis of Au-Ag core-shell bimetallic nanoparticles[J]. Journal of Physical Chemistry C,2008,112(39):15102-1510. DOI: 10.1021/jp806960r
[21] LI S H, WANG E B, TIAN C G, et al. Jingle-bell-shaped ferrite hollow sphere with a noble metal core: Simple synthesis and their magnetic and antibacterial properties[J]. Journal of Solid State Chemistry,2008,181(7):1650-1658.
[22] 中华人民共和国工业和信息化部. 对氨基苯磺酸钠: HG/T 2746—2010[S]. 北京: 化工出版社, 2011. Ministry of Industry and Information Technology of the People’s Republic of China. Sodium sulphanilate: HG/T 2746—2010[S]. Beijing: Chemical Industrial Press, 2011(in Chinese).
[23] JIANG W Q, ZHOU Y F, ZHANG Y L, et al. Superparamagnetic Ag-Fe3O4 core-shell nanospheres: Fabrication, characterization and application as reusable nanocatalysts[J]. Dalton Transactions,2012,41(15):4594-4601. DOI: 10.1039/c2dt12307j
[24] LI P, LI J, WU C Z, et al. Synergistic antibacterial effects of β-lactam antibiotic combined with silver nanoparticles[J]. Nanotechnology,2005,77(16):1912-1917.
[25] 郭少波, 马剑琪, 兰阿峰, 等. 核-壳纳米Ag@ZrO2复合材料的制备及其抑菌性能研究[J]. 复合材料学报, 2016, 33(4):821-826. GUO S B, MA J Q, LAN A F, et al. Preparation and its antibacterial properties of core-shell nano Ag@ZrO2 composite[J]. Acta Materiae Compositae Sinica,2016,33(4):821-826(in Chinese).
-
期刊类型引用(6)
1. 史娟,梁犇,宋凤敏,郝梦超,韩媛媛,吴迎花,邱莹,杨骏鹏,郭少波. ZnFe_2O_4@聚多巴胺@Ag纳米复合材料的制备及其抑菌性. 复合材料学报. 2023(12): 6774-6788 .  本站查看
本站查看
2. 郑锦丽,葛红光,马书婷,李宗林,郭少波,史娟,欧婷. 核壳型磁性纳米复合材料Fe_3O_4@SiO_2@mTiO_2@Pt的制备及催化性能. 功能材料. 2022(01): 1064-1071+1076 .  百度学术
百度学术
3. 肖鹏,李秀琴,冯霞,张蓓蓓,李博轩. BP-GO-AgNPs复合粉末添加量对BP-GO-AgNPs复合涂层抑菌性能的影响. 复合材料科学与工程. 2022(06): 47-52 .  百度学术
百度学术
4. 刘也,郭少波,梁艳莉,葛红光,马剑琪,刘智峰,刘波. 核壳型纳米复合材料Cu Fe2O4@NH2@Pt的制备及催化性能. 应用化学. 2022(08): 1237-1245 .  百度学术
百度学术
5. 马书婷,郑锦丽,张宁琪,郭少波,季晓晖,刘智峰. Fe_3O_4@SiO_2@mTiO_2-Au复合材料的制备及其催化性能研究. 贵金属. 2022(02): 1-8 .  百度学术
百度学术
6. 段娟娟,朱婷,晏志薇,刘洁,方梦婕,罗明珠,谭美辉,严敏,陈萍华,蒋华麟. 基于铁基复合材料的制备及其应用进展. 天津化工. 2021(05): 11-13 .  百度学术
百度学术
其他类型引用(1)
-





 下载:
下载: