Influence of chloride and sulfate on steel corrosion in simulated concrete pore solutions
-
摘要:
通过电化学测试、XRD测试和密度泛函理论(DFT)计算,本文探讨了在不同pH值(12.4、12.9和13.5)的模拟混凝土孔隙溶液中Cl−和SO2−4单独及共同作用对钢筋锈蚀行为的影响及其机制。结果表明:在pH值较低的饱和Ca(OH)2 (CH)溶液中,当Cl−浓度仅达到0.02mol/L时,开路电位(OCP)即由−375 mV急剧下降至−575 mV,表明Cl−在低浓度情况下就会显著加速腐蚀;而在pH值较高的ST溶液中,随着腐蚀离子浓度从0.01 mol/L逐步增加至0.4 mol/L,钢筋的极化电阻(Rp)从约100 kΩ·cm2稳定下降至5 kΩ·cm2,但整体耐腐蚀性明显优于其他pH值的情况,显示了高pH值对腐蚀的有效抑制作用。此外,当Cl−和SO2−4共存时,由于竞争吸附机制的作用,整体腐蚀速率介于两者单独存在时之间,SO2−4的存在一定程度上减缓了Cl−引发的腐蚀。本文基于上述结果提出了一个竞争吸附-催化腐蚀的两阶段反应模型,详细揭示了二者共同作用下的腐蚀行为,Cl−通过破坏钝化膜加速腐蚀进程,SO2−4则通过影响腐蚀产物的稳定性和分布参与腐蚀过程。
Abstract:Through electrochemical tests, XRD analysis, and density functional theory (DFT) calculations, this study investigated the individual and combined effects of Cl− and SO2−4 ions on the corrosion behavior of steel reinforcement in simulated concrete pore solutions at different pH values (12.4, 12.9 and 13.5). The results reveal that in the lower pH CH solution, even at a Cl− concentration of only 0.02 mol/L, the open circuit potential (OCP) drops sharply from −375 mV to −575 mV, indicating significant acceleration of corrosion by Cl− at low concentrations. Conversely, in the higher pH ST solution, as the concentration of corrosion ions increases gradually from 0.01 mol/L to 0.4 mol/L, the steel’s polarization resistance (Rp) stabilizes and decreases from approximately 100 kΩ·cm2 to 5 kΩ·cm2, demonstrating superior overall corrosion resistance compared to lower pH conditions, highlighting the effective inhibition of corrosion at higher pH value. Furthermore, in the presence of both Cl− and SO2−4 ions, the overall corrosion rate lies between the rates observed when each ion is present individually, due to the competitive adsorption mechanism. The presence of SO2−4 mitigates to some extent the corrosion initiated by Cl−. Based on these findings, the study proposes a two-stage competitive adsorption-catalytic corrosion reaction model, elucidating in detail the corrosion behavior under their combined influence: Cl− accelerates corrosion by disrupting the passive film, while SO2−4 participates in the corrosion process by influencing the stability and distribution of corrosion products.
-
钢筋混凝土广泛应用于基础设施建设中,但钢筋腐蚀问题严重影响了建筑耐久性和使用寿命[1]。通常,混凝土中钢筋表面的钝化膜可抵抗环境的腐蚀[2-3],但在腐蚀介质、碱性水泥基质影响和物理或机械损伤等特殊条件下,钝化膜可能会局部或完全破坏,导致腐蚀加剧。Cl−腐蚀是造成钝化膜破坏的关键因素之一,当其浓度超过一定阈值时,如因暴露在海水、除冰盐或其他含氯化物的物质中,钝化膜会受到破坏,加速钢筋腐蚀过程[4-7]。此外,钢筋混凝土结构还会暴露在Cl−和SO2−4共存的环境中,如中国西北地区[8]、阿拉伯海湾地区[9-10]及海洋工程项目[11-12]等,引起复杂的腐蚀行为。
目前针对钢筋腐蚀的研究更多关注的是Cl−的影响,而SO2−4的腐蚀性及其在氯盐-硫酸盐的复合环境中的作用并没有统一的结论。例如,Haleem等[13-14]和Maes等[15]的研究认为SO2−4具有腐蚀性且相比于Cl−较强,后者还认为氯盐的存在抑制了硫酸盐的腐蚀。然而,Xu等[16]认为SO2−4不存在腐蚀性,只起着抑制点蚀、腐蚀发生后促进腐蚀的作用。Cao等[17]和Yang等[18]则认为SO2−4具有腐蚀性但要弱于Cl−。此外,Stroh等[19]、Dong等[20]和Dehwah等[21]的研究认为当SO2−4存在时,降低了Cl−的吸附能力,导致其腐蚀速率加快,而Tumidajski等[22]和宋立康等[23]的研究认为SO2−4是通过降低混凝土的孔隙率来降低Cl−在混凝土中的扩散。左晓宝等[24]认为SO2−4具有腐蚀性,在复合盐存在的情况下起着前期抑制腐蚀、后期促进腐蚀的作用。
为了更好地模拟钢筋的耐腐蚀性,混凝土孔隙溶液被广泛应用,它能快速有效地模拟实际环境[25-29]。然而混凝土具有高碱性(其pH值大于12.5),钢筋在混凝土中一般处于钝化状态[30-31]。出于低碳环保的要求,人们会在水泥中加入矿物掺合料,但混凝土孔隙溶液的pH值会因掺加外加剂或胶凝材料、碳化等因素而引起波动,从而影响钢筋钝化膜的稳定性并增加腐蚀风险。翟海涛等[32]的研究发现钢筋发生腐蚀时的Cl−浓度与模拟混凝土孔隙溶液的pH值有关,pH值越高,钢筋腐蚀电位越大。Shin等[33]的研究认为大部分在碳钢表面产生的腐蚀产物是由于流动加速腐蚀的影响,而pH值的提高会减少流动加速腐蚀,达到一定抑制效果。Liu等[34]的研究表明pH值的降低会让钝化膜在较低的Cl−浓度下发生腐蚀,而在高碱性溶液中钝化膜可以为钢提供更好的保护作用。
考虑到上述实际和理论问题,本文旨在阐明低碳钢在不同pH值(12.4、12.9和13.5)的模拟混凝土孔隙溶液中由Cl−和SO2−4引发的腐蚀行为。通过综合运用电化学测试方法、X 射线衍射法(XRD)和密度泛函理论(DFT)计算,分析了腐蚀电位、极化电阻、腐蚀电流密度和电化学阻抗谱,来解释Cl−和SO2−4的相互作用机制,并提出了一个竞争吸附与催化腐蚀的两阶段离子反应模型。
1. 试 验
1.1 原材料
从直径16 mm 的钢筋中截取厚度为 5 mm 的电极片,其含量为0.20%碳、0.55%硅、1.42%锰、0.028%硫和 0.026%磷,其余为铁元素。每组试验采用3个电极片作为对照。使用M-2T型金相研磨机,逐级用 400#、800#、
1000 # SiC砂纸打磨、抛光钢筋片一端至镜面,再用酒精和丙酮清洗表面油污生锈,并浸泡在酒精中封存。工作电极面积为 1 cm2。试验池容量约为 400 mL,所用化学试剂均为分析纯,配制溶液时采用去离子水。其中,第一种模拟液为饱和Ca(OH)2溶液(CH),pH值约为12.4;第二种模拟液为普通硅酸盐水泥粉末与去离子水按1∶10质量比混合搅拌后静置48 h,取其过滤后的上清液(LC),pH值约为12.9;第三种模拟液是根据普通硅酸盐水泥高压萃取法[35]得到,由 饱和Ca(OH)2+0.1 mol/L NaOH+0.3 mol/L KOH (LC)组成,pH值约为13.5。1.2 试验过程
腐蚀试验是在钢试样放入模拟液中浸泡9 d完成钝化后进行的,每种溶液中每3个试样分为一组。每24 h,第一组和第二组分别加入0.01 mol/L的Cl−和SO2−4;第三组加入0.01 mol/L的Cl−和0.01 mol/L的SO2−4。在ST溶液中,当腐蚀离子浓度达到0.1 mol/L,第组每隔24 h分别增加0.03 mol/L的Cl−、SO2−4或两者,直至各组腐蚀离子的浓度达到 0.4 mol/L。Cl−和SO2−4由NaCl和Na2SO4提供,溶液搅拌均匀。
1.3 电化学测试
采用美国普林斯顿P4000电化学工作站,在经典的三电极设置中进行。钢试样作为工作电极,饱和甘汞电极(Saturated calomel electrode,SCE)作为参比电极,铂电极作为辅助电极。测试在开路电位(OCP)稳定后进行。线性极化电阻(LPR)测试的参数:扫描电位与OCP的对比为±10 mV,扫描速率10 mV/min。电化学阻抗谱(EIS)测试使用振幅为10 mV的正弦电压信号干扰电压,扫描频率范围为10 mHz~100 kHz。
1.4 X射线衍射
从电极表面刮下腐蚀产物并研磨成粉末,然后用74 μm筛网过筛,并在60℃下真空干燥24 h。干燥后的粉末储存在热塑性真空密封袋中。X 射线衍射分析使用D8 Discover衍射仪进行,参数如下:铜靶 (Kα,λ=
0.15406 nm),工作电压40 kV,工作电流30 mA,扫描范围5°~85°,扫描速度0.3 s/步,步长0.02°。1.5 密度泛函理论
利用Materials Studio软件中的CASTEP模块[36]和GGA-PW91[37]交换关联泛函进行模拟。平面波截止能量设为340 eV,自洽场(SCF)收敛标准为2.0×10−6 eV/原子。系统能量、最大位移和最大力的收敛标准分别为2.0×10−5 eV/原子、
0.0001 nm 和 0.3 eV/nm。使用超软赝势[38]模拟离子与价电子的相互作用,布里渊区k点取样为4×4×1[39]。计算模型采用(4×4)五原子层Fe(100)表面作为界面,固定底部三层,允许顶部两层松弛。设1.5 nm真空层以减少周期效应。Cl−和SO2−4吸附在Fe(100)表面的不同位点,计算吸附能如下式:
Eads = Eadsorbate/surf - (Eadsorbate+Esurf) (1) 其中:Eadsorbate/surf表示系统的总能量;Eadsorbate和Esurf分别表示分离吸附物的能量和金属表面的能量。
2. 结果与讨论
2.1 腐蚀电位
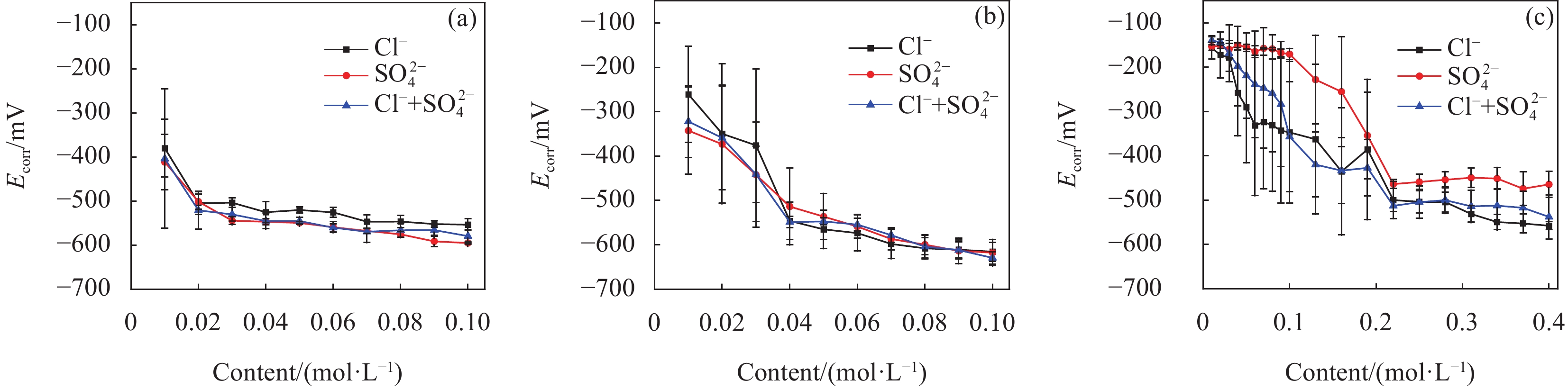
为了比较低碳钢在CH、LC和ST模拟液中的腐蚀差异,采用开路电位测试法(OCP)分析腐蚀电位(Ecorr)。图1显示,随着腐蚀离子浓度的增加,所有溶液中低碳钢的Ecorr值普遍下降,以下是关于各溶液的具体描述,其中Ecorr是各图中3条曲线的一个整体趋势。
在CH溶液中(图1(a)),Ecorr从−375 mV显著下降到−575 mV,尤其当腐蚀离子浓度达 0.02 mol/L时,腐蚀明显加剧。另外,Cl−的曲线略高于其他两者,说明其腐蚀性最低,SO2−4和Cl−+SO2−4二者接近且较高。对于LC 溶液(图1(b)),Ecorr从−300 mV下降到−625 mV,当腐蚀离子浓度为0.04 mol/L时腐蚀加剧。3条曲线表现较接近,说明Cl−、SO2−4和Cl−+SO2−4对钝化后钢筋的腐蚀影响相似。在ST溶液中(图1(c)),Ecorr从−300 mV下降到−525 mV,当腐蚀离子浓度为0.22 mol/L时腐蚀加剧。SO2−4的曲线略高于另外两条曲线,说明其腐蚀性最低,而Cl−和Cl−+SO2−4接近,但Cl−的初期腐蚀速率较快,这表明SO2−4的存在减轻了Cl−引发的腐蚀。此外,ST模拟液的Ecorr要高于CH和LC模拟液,表明pH值升高会降低Cl−和SO2−4的吸附和腐蚀能力,因而其钝化膜的耐腐蚀性更好,而LC次之,CH最弱。
2.2 极化电阻和腐蚀电流密度
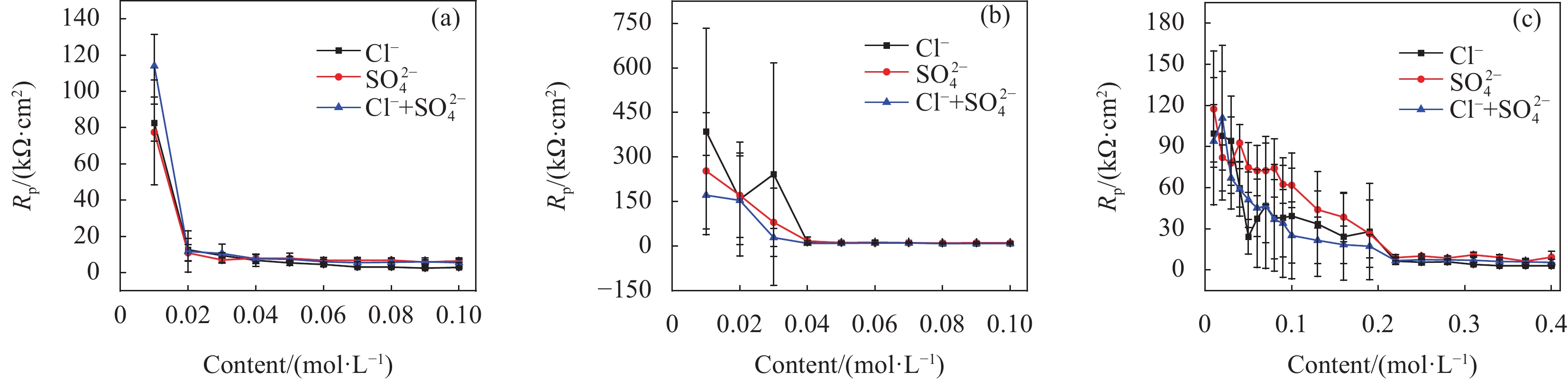
通过线性极化电阻测试,计算得到极化电阻 (Rp) 和腐蚀电流密度 (Icorr)的平均值和标准差。图2显示,CH、LC和ST模拟液中钢试样的Rp曲线均呈下降趋势,其中ST溶液中钢筋的耐腐蚀性较强,LC 次之,CH最弱。
在CH溶液中(图2(a)),腐蚀离子浓度在0.01 mol/L至0.02 mol/L范围内,Rp急剧从约100 kΩ·cm2降至10 kΩ·cm2,继续降至5 kΩ·cm2直到0.10 mol/L,显示腐蚀离子浓度为0.02 mol/L时腐蚀显著,与Ecorr分析结果一致。在LC溶液中(图2(b)),腐蚀离子浓度在0.01 mol/L至0.04 mol/L范围内,Rp从约300 kΩ·cm2显著下降到10 kΩ·cm2,至0.10 mol/L时进一步降至5 kΩ·cm2,即腐蚀离子浓度为0.04 mol/L时腐蚀趋于稳定。其中,Cl−的曲线变化最为显著,表现出较强的腐蚀性,SO2−4次之,而Cl−+SO2−4在浓度达到0.04 mol/L以前的腐蚀性最弱,但之后与前二者近似。在ST溶液中(图2(c)),腐蚀离子浓度在0.01 mol/L至0.22 mol/L范围内,Rp从约100 kΩ·cm2急剧下降到10 kΩ·cm2,至0.40 mol/L时进一步降至 5 kΩ·cm2,表明腐蚀离子浓度为0.22 mol/L时3腐蚀趋于稳定。起初3条曲线较接近,但腐蚀离子浓度为0.04 mol/L至0.22 mol/L时,SO2−4曲线略高,下降变化较少,表明其腐蚀速率最低,Cl−和Cl−+SO2−4二者相似,与Ecorr曲线的分析一致。
通过线性极化电阻测试(LPR)得到极化电阻(Rp),利用Stern-Geary公式可以计算腐蚀电流密度(Icorr),如下式:
Icorr=βaβc2.303(βa+βc)Rp=BRp (2) 其中:βa和βc分别为阳极和阴极极化曲线斜率;Rp为极化电阻;B为Stern-Geary常数(腐蚀状态下取B=26 mV)。
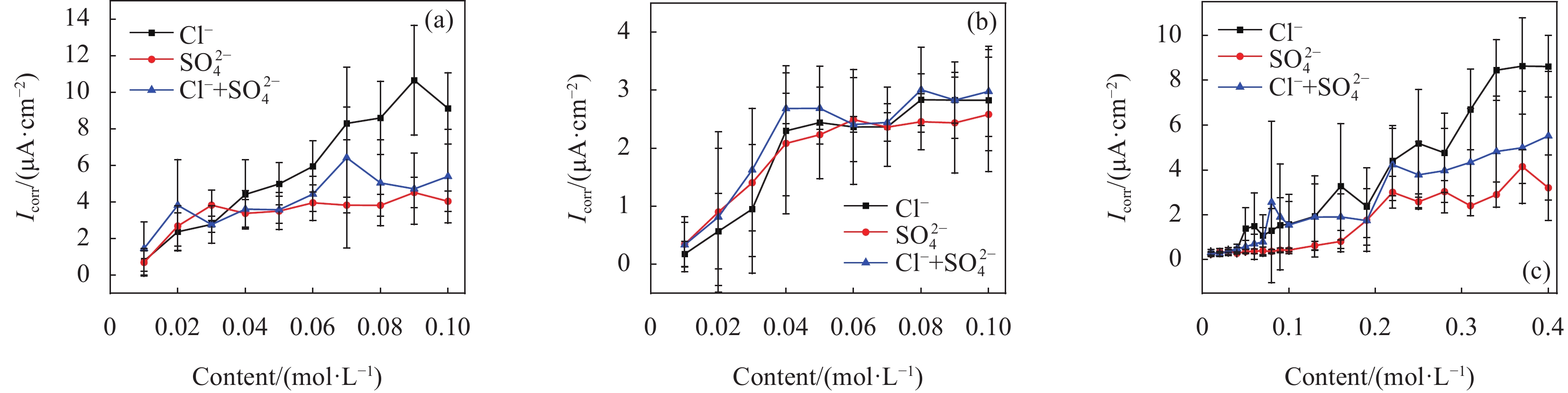
图3为浸泡在含有腐蚀离子的CH、LC和ST溶液中钢试样的Icorr曲线。如图3(a)所示,随着腐蚀离子浓度的增加,Icorr值也逐渐增大,其中有关Cl−的曲线最高,Cl−+SO2−4次之,SO2−4最低。这表明在CH溶液中,Cl−对钢筋的腐蚀作用最强,而SO2−4最弱。复合离子情况下可能由于离子竞争吸附作用,SO2−4在一定程度上降低了Cl−的腐蚀性。由图3(b)可知,随着腐蚀离子浓度的增加,Icorr值也逐渐增大,且3条曲线比较接近。这表明在LC溶液中,3种离子情况对钢筋的腐蚀性相对接近。由图3(c)可知,ST溶液与CH溶液中的情况类似。此外,整体来看可知溶液的pH值越高,钢筋的耐腐蚀性越好。
![]() 图 3 不同模拟液中腐蚀阶段钢试样的腐蚀电流密度(Icorr)曲线:(a)第一种模拟液(CH)中;(b)第二种模拟液(LC)中;(c)第三种模拟液(ST)中Figure 3. Corrosion current density (Icorr) curves of steel specimens in corrosion stage of SCPSs: (a) In the first simulated solution (CH); (b) In the second simulated solution (LC); (c) In the third simulated solution (ST)
图 3 不同模拟液中腐蚀阶段钢试样的腐蚀电流密度(Icorr)曲线:(a)第一种模拟液(CH)中;(b)第二种模拟液(LC)中;(c)第三种模拟液(ST)中Figure 3. Corrosion current density (Icorr) curves of steel specimens in corrosion stage of SCPSs: (a) In the first simulated solution (CH); (b) In the second simulated solution (LC); (c) In the third simulated solution (ST)2.3 电化学阻抗谱
电化学阻抗谱(EIS)能详细反映金属表面的电化学反应,通过变化的腐蚀离子浓度揭示钢筋表面钝化膜的腐蚀情况[40]。通常,EIS的高频区(Nyquist曲线左端)反映电解质和电极表面的电阻信息,而低频区(Nyquist曲线右端)反映电化学腐蚀过程中的电荷转移电阻。
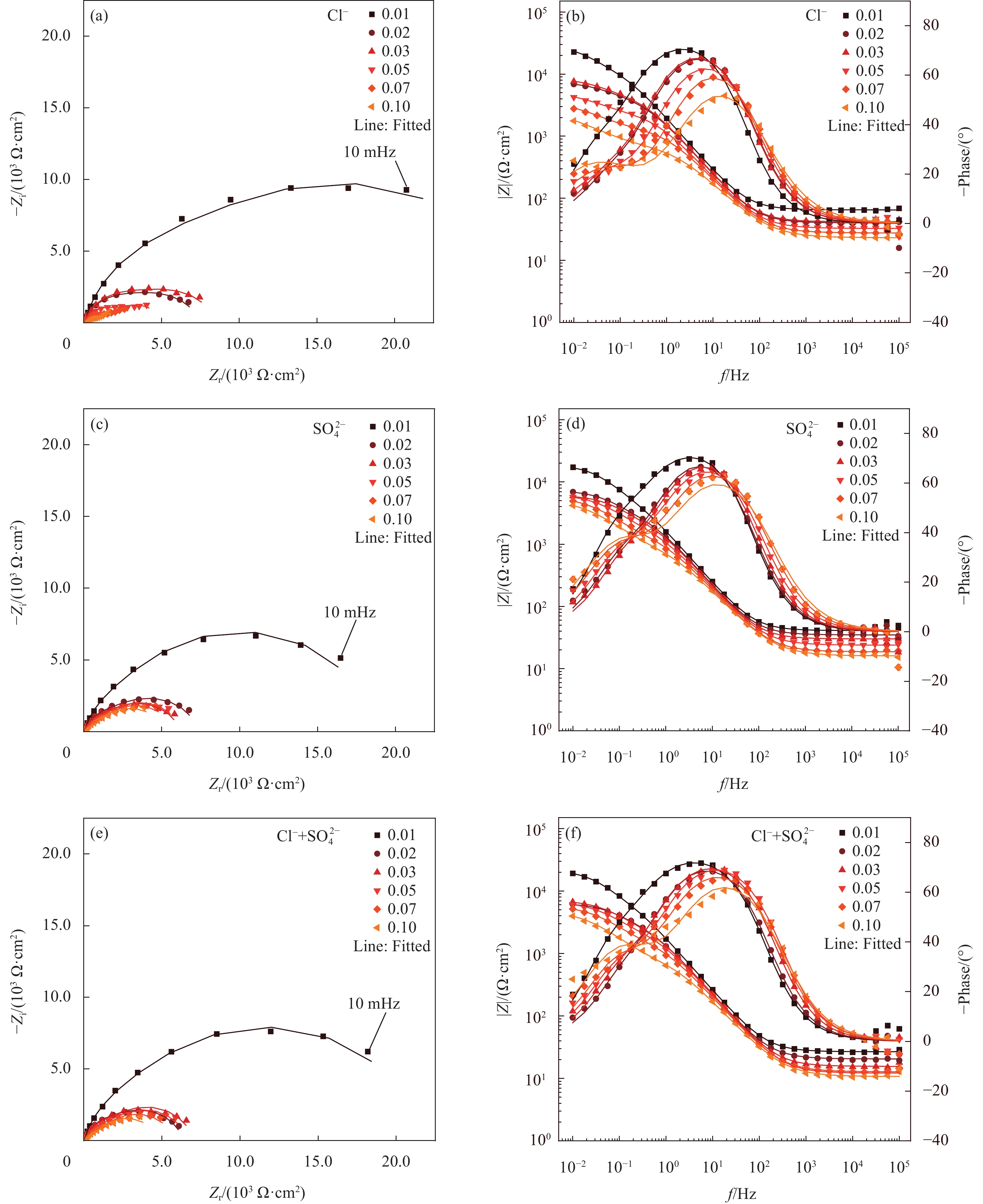
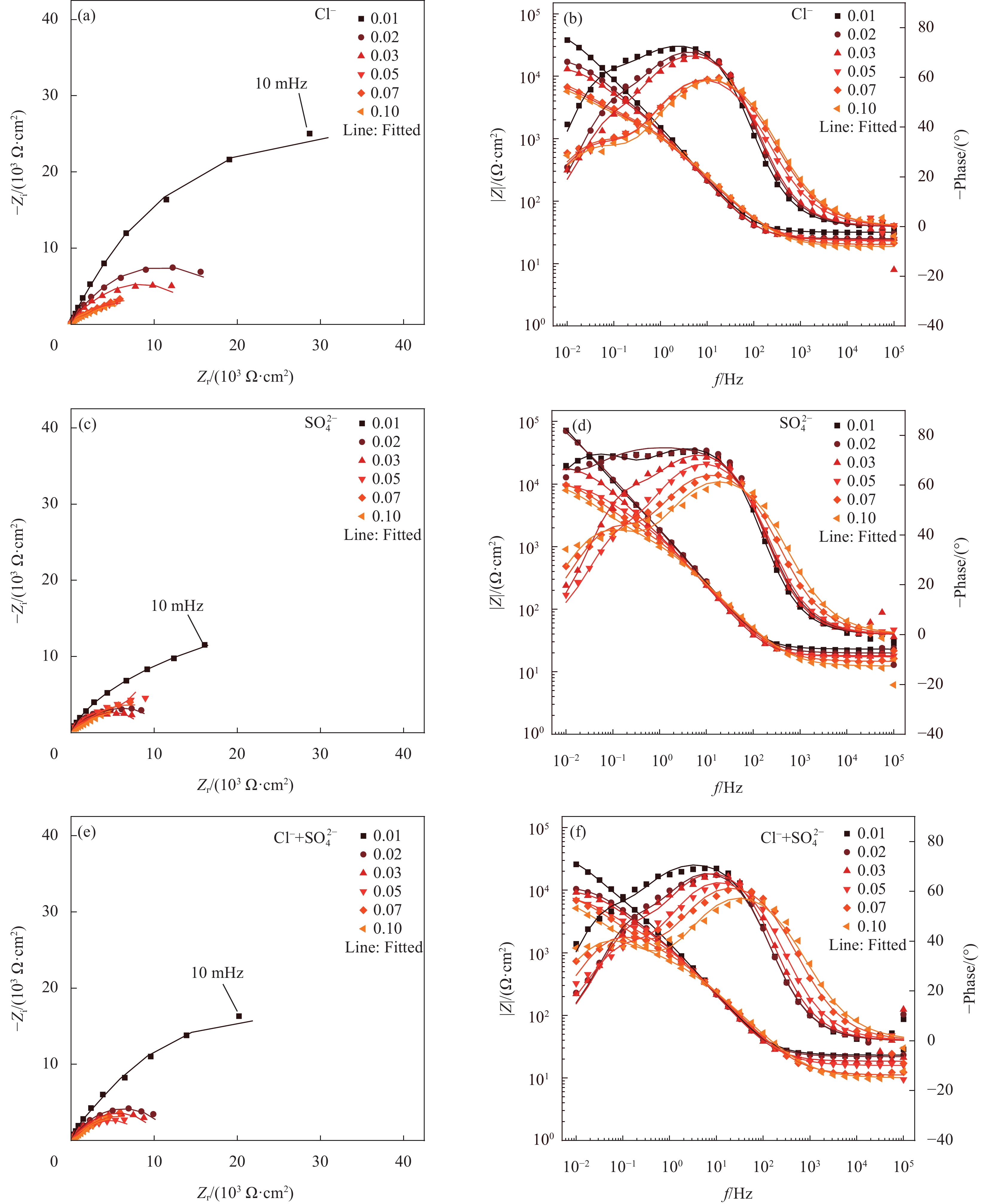
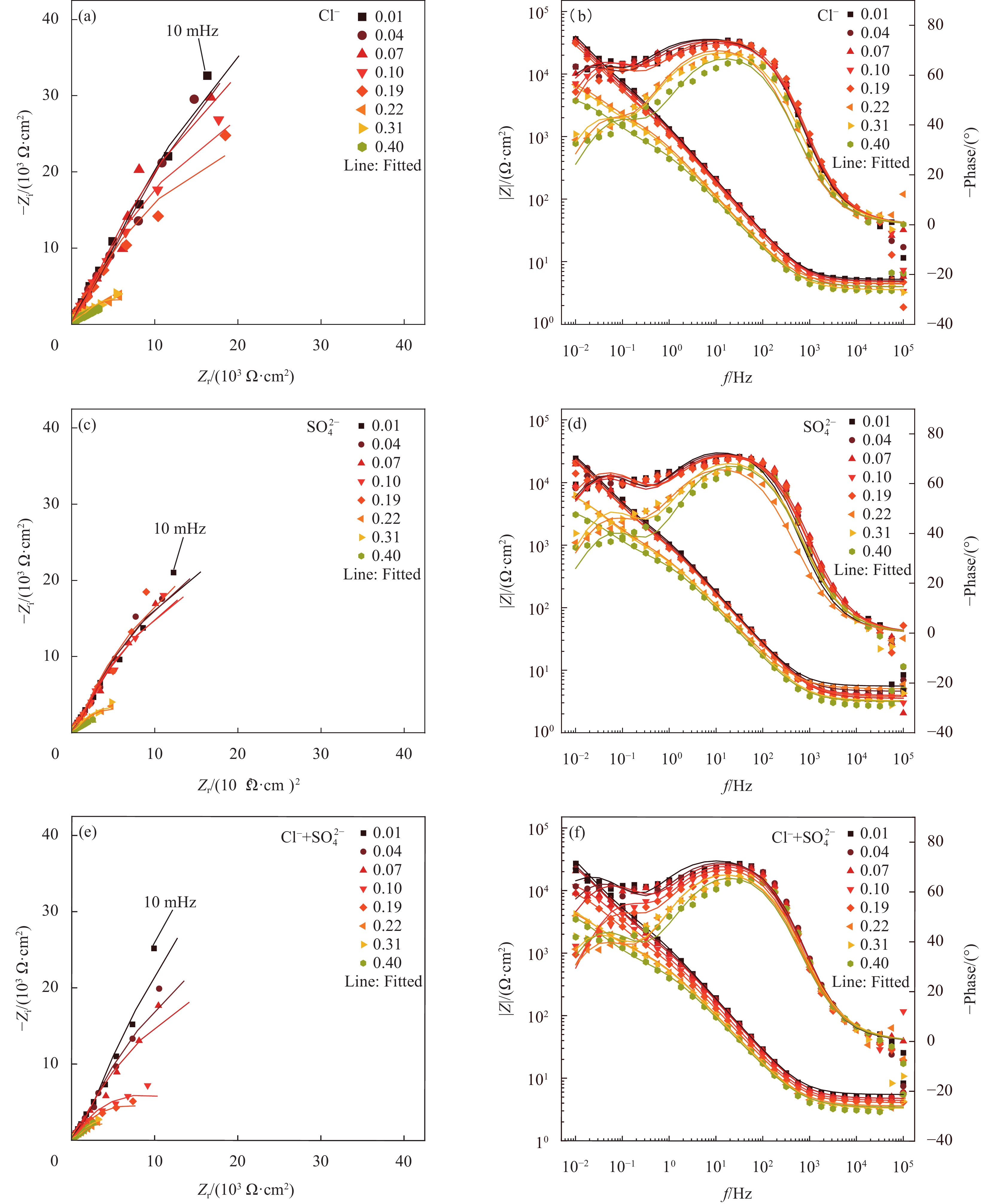
在图4、图5和图6中,随着腐蚀离子浓度的增加,钢筋的容抗弧半径都逐渐减小。CH溶液(图4)中随着腐蚀离子浓度的增加,钢筋的容抗弧半径在腐蚀离子浓度为0.01 mol/L至0.02 mol/L范围时急剧下降,然后趋于稳定。这表明,当CH溶液中的腐蚀离子浓度超过0.01 mol/L时,钢筋开始加速腐蚀。在LC溶液(图5)中,当加入Cl−或Cl−+SO2−4时,腐蚀离子浓度超过0.01 mol/L,容抗弧半径便明显减小。当加入SO2−4时,腐蚀离子浓度超过0.02 mol/L,容抗弧半径才减小。在ST溶液(图6)中,当为单一腐蚀离子时,腐蚀离子浓度在0.1 mol/L至0.19 mol/L范围时,容抗弧半径变化明显,而为复合腐蚀离子时,腐蚀在0.07 mol/L至0.1 mol/L浓度之间才表现出显著加剧。因此,Cl−的腐蚀性要高于SO2−4,复合离子的存在会进一步加剧腐蚀,且随pH值升高,Cl−保持较显著的腐蚀性,而SO2−4会表现的相对减弱。
![]() 图 4 第一种模拟液(CH)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图Figure 4. Electrochemical impedance spectroscopy (EIS) results and equivalent electrical circuit fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the first simulated solution (CH): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram
图 4 第一种模拟液(CH)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图Figure 4. Electrochemical impedance spectroscopy (EIS) results and equivalent electrical circuit fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the first simulated solution (CH): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram![]() 图 5 第二种模拟液(LC)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图Figure 5. Electrochemical impedance spectroscopy (EIS) results and equivalent electrical circuit fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the second simulated solution (LC): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram
图 5 第二种模拟液(LC)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图Figure 5. Electrochemical impedance spectroscopy (EIS) results and equivalent electrical circuit fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the second simulated solution (LC): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram![]() 图 6 第三种模拟液(ST)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图Figure 6. Electrochemical impedance spectroscopy (EIS) results and fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the third simulated solution (ST): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram
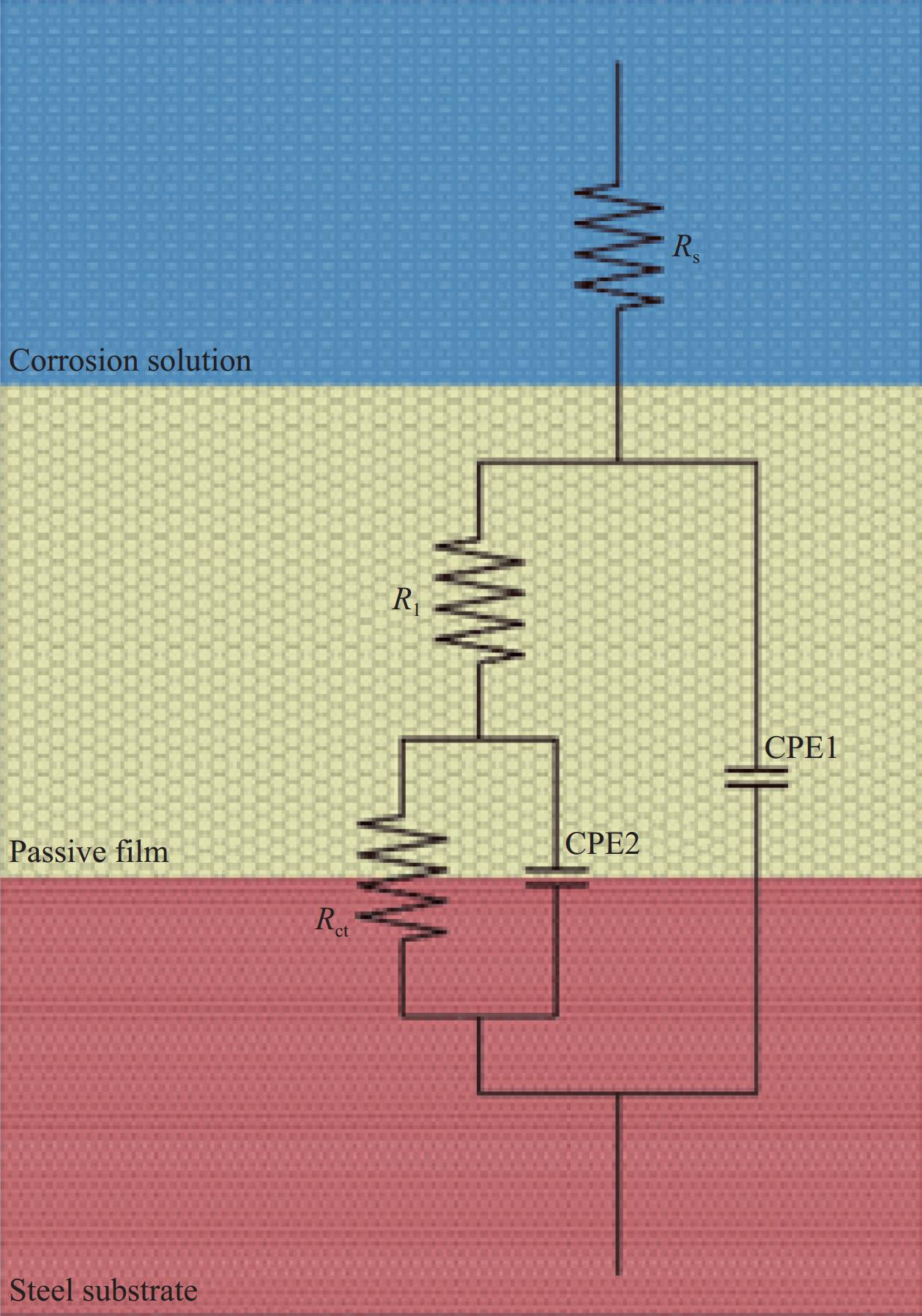
图 6 第三种模拟液(ST)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图Figure 6. Electrochemical impedance spectroscopy (EIS) results and fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the third simulated solution (ST): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram为深入理解钢筋腐蚀过程,通过等效电路(ECC)分析EIS测试的结果。如图7所示,其中Rs表示电解质电阻,恒相位角元素CPE1和CPE2分别表示钝化膜相特性和钢筋表面动态效应,R1表示钝化膜电阻,Rct表示电荷转移电阻。其中,图4、图5和图6中的点作为测量值,线作为拟合值,从图可以看出,测量值与拟合值之间的拟合度较合理,这表明所选的EEC可以准确地反映EIS结果。
由表1可知,等效电路R(Q(R(QR)))对EIS数据的卡方数值的数量级均保持在10−2到10−4之间,表明该电路能良好拟合EIS数据。腐蚀过程中,各模拟液中的Rs值逐渐降低,CH溶液的Rs值最大,LC次之,ST最小。而CPE2对应的参数Q和a值都可用来反映钝化膜的完整性,Q值越小,越接近理想电容行为,即钝化膜完整,而a值越接近1,钝化膜越完整。从表1看,随着腐蚀的进展,Q值增加,而a值下降,在CH和LC溶液中随腐蚀离子浓度增加的变化较大,而ST溶液中较小。电荷转移电阻Rct反映钝化膜的电化学腐蚀反应阻力,其减小意味着钝化膜受到破坏。
表 1 不同模拟液中腐蚀电化学阻抗谱(EIS)数据的等效电路拟合结果Table 1. Equivalent electrical circuit fitting results of electrochemical impedance spectroscopy (EIS) data in different simulated solutionsContent/
(mol·L−1)Rs/
(Ω·cm2)CPE1, Q/
(S·sn·cm−2)CPE1,a
[0<a<1]R1/(Ω·cm2) CPE2, Q/
(S·sn·cm−2)CPE2,a
[0<a<1]Rct/
(Ω·cm2)Chi-squared CH-Cl− 0.01 65.42 0.0000917 0.8863 4164 0.0000714 0.4761 41280 5.62×10−4 0.02 40.35 0.0001129 0.8703 2597 0.0002508 0.4036 6510 1.85×10−3 0.03 42.19 0.0001079 0.8758 2195 0.0002016 0.3551 9236 7.96×10−4 0.05 33.03 0.0001247 0.8633 802.3 0.0004566 0.2367 19660 7.51×10−4 0.07 28 0.0001379 0.8521 752.2 0.0010090 0.3267 13790 6.27×10−4 0.1 23.6 0.0001617 0.83 298.7 0.0015650 0.3055 1665 6.81×10−4 CH-SO2−4 0.01 41.22 0.0001062 0.8848 4059 0.0000951 0.6181 16650 1.05×10−3 0.02 35.17 0.0001150 0.8848 1883 0.0002298 0.5316 6555 6.93×10−4 0.03 30.32 0.0001140 0.8887 1317 0.0002200 0.5174 5769 2.09×10−3 0.05 24.24 0.0001285 0.8705 1027 0.0003002 0.5019 6891 8.19×10−4 0.07 18.98 0.0001310 0.8709 605.9 0.0004202 0.4764 7953 3.39×10−3 0.1 16.46 0.0001365 0.8598 335.3 0.0005371 0.4666 8298 6.53×10−3 CH
Cl−+SO2−40.01 26.53 0.0001563 0.8879 4824 0.0000884 0.8907 26730 1.29×10−3 0.02 20.73 0.0001161 0.8732 1628 0.0001767 0.4851 5558 3.03×10−3 0.03 15.74 0.0001152 0.8735 1646 0.0002093 0.4884 6707 1.83×10−3 0.05 12.29 0.0001198 0.8693 1362 0.0002904 0.4951 7037 8.45×10−4 0.07 13.03 0.0001175 0.8771 565.2 0.0003434 0.4542 7912 1.83×10−3 0.1 11.07 0.0001478 0.8374 235 0.0005624 0.453 9741 4.18×10−3 LC-Cl− 0.01 32.04 0.0001148 0.8847 8330 0.0000563 0.6299 73860 3.93×10−4 0.02 25.3 0.0001290 0.8744 2978 0.0001182 0.6136 20830 5.60×10−4 0.03 24.19 0.0001079 0.8758 2195 0.0002016 0.3551 9236 7.96×10−4 0.05 23.1 0.0001176 0.8458 719.1 0.0002957 0.4679 12410 3.83×10−3 0.07 20.43 0.0001043 0.8391 379.3 0.0004010 0.4495 27850 3.01×10−3 0.1 18.96 0.0001411 0.7874 338.4 0.0004679 0.3499 9680 3.23×10−3 LC-SO2−4 0.01 30.1 0.0001085 0.8736 12400 0.0001089 0.4981 89150 6.82×10−4 0.02 25.22 0.0001202 0.8592 1608 0.0001916 0.4244 13390 9.59×10−4 0.03 23.07 0.0001673 0.8145 1621 0.0000909 0.4929 12360 2.51×10−3 0.05 20.76 0.0001310 0.8047 1110 0.0002258 0.4652 20660 8.88×10−4 0.07 19.5 0.0002658 0.7727 2373 0.0004917 0.4257 40920 1.52×10−3 0.1 14.82 0.0001614 0.7415 7872 0.0005338 0.3576 18148 1.16×10−3 LC
Cl−+SO2−40.01 23.06 0.0001348 0.8229 6727 0.0000550 0.5558 60790 4.27×10−3 0.02 22.16 0.0001216 0.8733 7205 0.0001543 0.5928 12610 2.06×10−3 0.03 18.79 0.0001121 0.8835 841 0.0001819 0.5644 11890 4.18×10−3 0.05 12.29 0.0001198 0.8693 1362 0.0002904 0.4951 7037 8.45×10−4 0.07 11.43 0.0001043 0.8391 379.3 0.0004010 0.4495 27850 3.01×10−3 0.1 10.37 0.0001018 0.8181 2699 0.0006246 0.4161 11730 4.13×10−3 ST-Cl− 0.01 5.391 0.0000566 0.9609 18140 0.0001331 0.6403 323900 5.83×10−3 0.04 5.112 0.0000465 0.9876 19410 0.0001591 0.6505 216900 7.50×10−3 0.07 4.982 0.0000389 0.982 9934 0.0001715 0.6763 141800 5.65×10−3 0.10 4.486 0.0001388 0.9657 1653 0.0002079 0.6374 193900 7.77×10−3 0.19 4.112 0.0001461 0.9329 1604 0.0001977 0.6628 173000 2.59×10−2 0.22 4.658 0.0001180 0.9443 2733 0.0004016 0.5089 16170 2.00×10−2 0.31 3.681 0.0001627 0.9025 2393 0.0004476 0.444 29290 2.54×10−2 0.40 4.152 0.0001806 0.9225 1345 0.0007194 0.5227 8297 2.98×10−2 ST-SO2−4 0.01 5.761 0.0000489 0.9533 45472 0.0002232 0.6262 898000 3.12×10−2 0.04 4.793 0.0000472 0.9437 32150 0.0002417 0.6331 840400 2.02×10−2 0.07 3.71 0.0000440 0.9333 12270 0.0002724 0.6245 314900 1.92×10−2 0.10 4.133 0.0000433 0.9126 11170 0.0002714 0.6367 339800 1.72×10−2 0.19 3.825 0.0002788 0.9491 1614 0.0000467 0.5169 445500 8.33×10−3 0.22 5.145 0.0002587 0.8349 2539 0.0005471 0.5214 17930 2.91×10−3 0.31 3.417 0.0000819 0.9798 836 0.0006337 0.5135 32580 1.98×10−2 0.40 3.221 0.0000762 0.9458 1027 0.0009938 0.4746 12670 3.14×10−2 ST
Cl−+SO2−40.01 5.634 0.0000442 0.9522 89602 0.0000362 0.6685 262700 1.72×10−2 0.04 4.987 0.0000429 0.9726 16280 0.0002398 0.6297 267200 1.04×10−2 0.07 5.009 0.0000435 0.9695 13440 0.0002551 0.6265 15990 4.26×10−3 0.10 4.637 0.0000544 0.9868 1703 0.0003090 0.6111 26560 7.15×10−3 0.19 4.223 0.0001823 0.8697 3961 0.0003349 0.551 21510 2.00×10−3 0.22 3.682 0.0006716 0.9053 1201 0.0009439 0.514 34670 1.32×10−2 0.31 3.418 0.0007192 0.9147 913 0.0011370 0.5202 16320 1.36×10−2 0.40 3.547 0.0009536 0.9461 906 0.0010946 0.5018 8690 2.43×10−2 Notes: Rs—Electrolyte resistance; R1—Passivation film resistance; Rct—Charge transfer resistance; Q, a—Parameters in the constant phase angle elements CPE1 and CPE2; Chi-squared is the chi-squared test result. 2.4 XRD
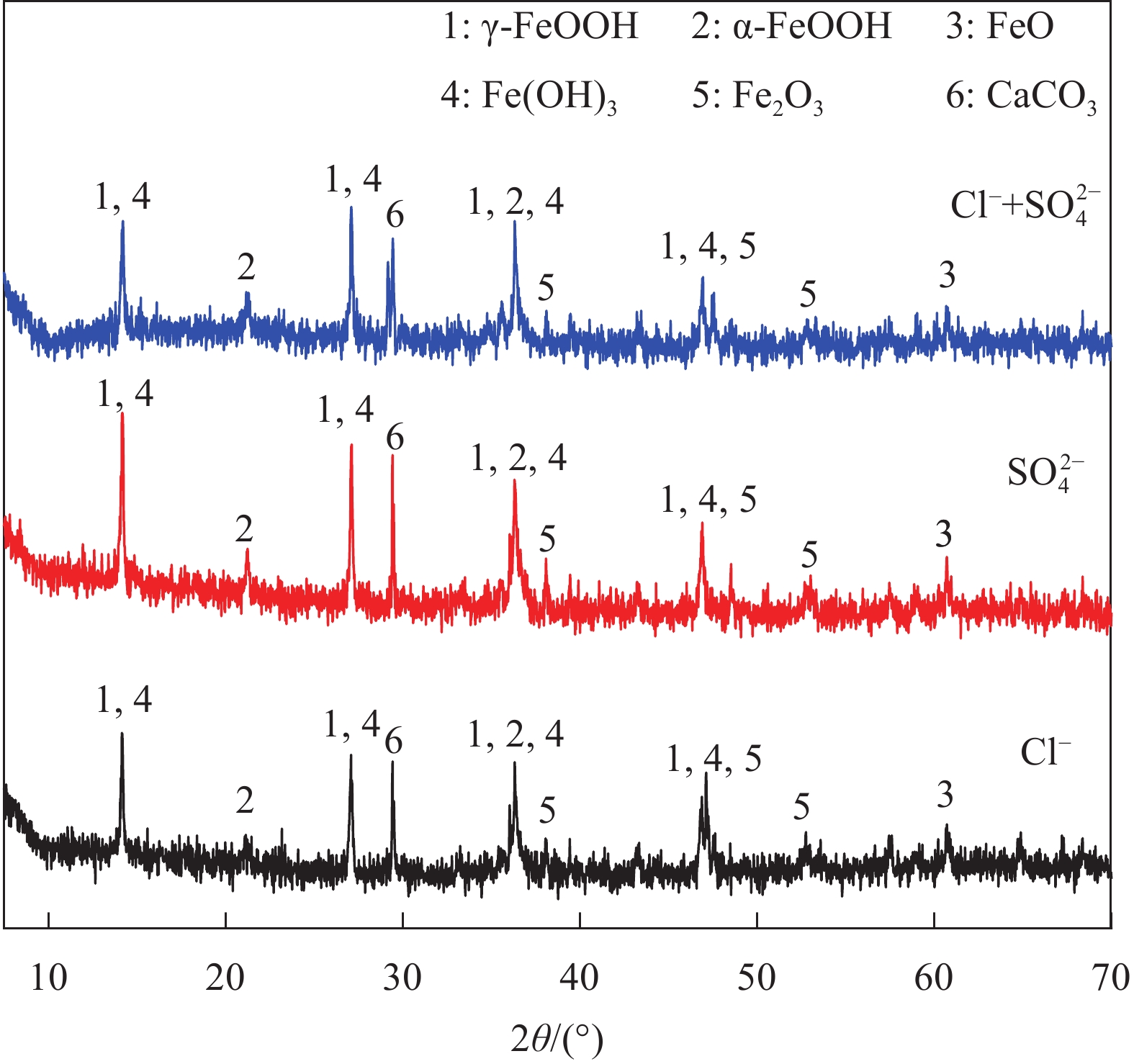
在CH模拟液进行电化学试验后,为了获得足够数量的钢筋腐蚀产物来进行XRD分析,腐蚀时间延长了15 d,并收集了Cl−、SO2−4和Cl−+SO2−4作用下的腐蚀产物。XRD图谱(图8)显示,在不同腐蚀离子作用下产物的主要衍射峰相似,表明其成分一致,包括γ-FeOOH、α-FeOOH、FeO、Fe2O3和Fe(OH)3等,其中检测的CaCO3不属于腐蚀产物,而是由Ca(OH)2与CO2反应生成的。此外,纤铁矿(γ-FeOOH)和水铁矿(Fe(OH)3)对应的衍射峰较多且高,表明其含量较高,而针铁矿(α-FeOOH)和赤铁矿(Fe2O3)的含量则较少,方铁矿(FeO)的含量则最少。
2.5 DFT
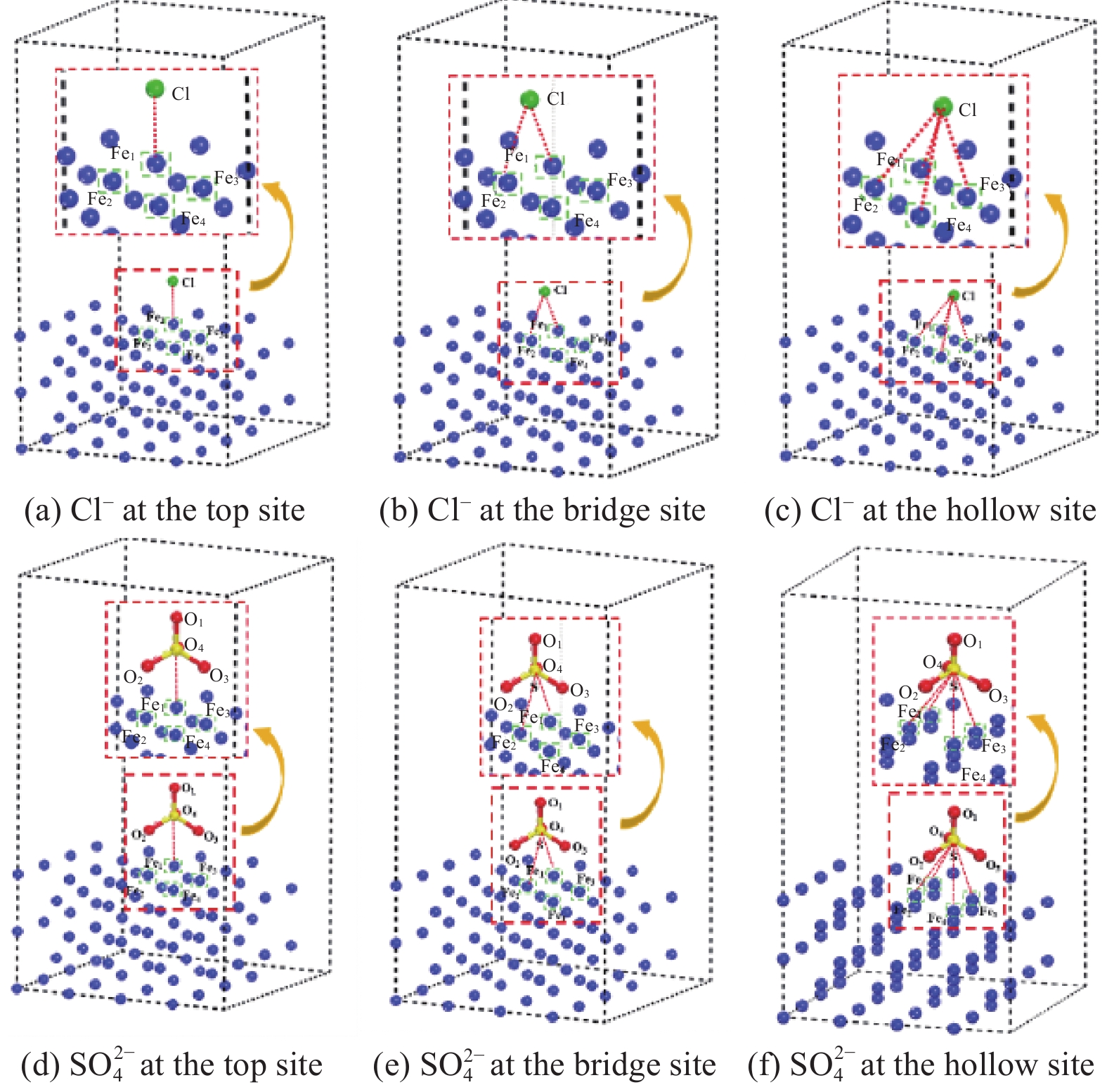
图9为Cl−和SO2−4 在Fe(100)表面的吸附位点(顶位、桥位和空心位)。表2为DFT计算结果,Cl−和SO2−4在Fe(100)表面的吸附能均为负值,表明其存在会促进铁腐蚀。另外,SO2−4的吸附能比Cl−的负值要大,这表明其与铁表面的相互作用强于Cl−。在多离子溶液中,Fe(100)更倾向吸附SO2−4,可能导致它在铁表面的高覆盖率和影响其他离子的吸附。由此可得,SO2−4的优先吸附将会减少Cl−的吸附位点,影响铁腐蚀行为,促进SO2−4相关的腐蚀,同时抑制Cl−引起的局部腐蚀。
表 2 Cl−和SO2−4在Fe(100)表面的吸附能Table 2. Adsorption energy of Cl− and SO2−4 adsorption on Fe(100) surfaceAdsorption energy on Fe(100)/(kJ·mol−1) Top Bridge Hollow Cl− −449.896 −458.134 −363.154 SO2−4 −674.245 −691.320 −739.124 2.6 腐蚀机制分析
电化学测试显示,当模拟液中的腐蚀离子达到一定浓度时,钢筋钝化膜就会被破坏,发生腐蚀。此外,Cl−和SO2−4在腐蚀过程中形成的腐蚀产物基本相同。依据合理的假设,Cl−和SO2−4在钢筋腐蚀的不同阶段都起着催化剂的作用,但并不出现在最终腐蚀产物中。
Cl−和SO2−4在钢筋腐蚀过程中的交互作用机制可以描述为如图10所示的一个两阶段反应模型,包括竞争吸附和催化腐蚀。由图可知,Cl−和SO2−4的同时存在会明显改变金属表面的腐蚀动力学。再者,pH值的上升会减少Cl−和SO2−4的吸附,从而导致Ecorr和Rp升高,腐蚀风险降低,而较低的pH值则加速破坏。
在pH值相同的条件下,SO2−4的强吸附能可以在Cl−存在的情况下占据吸附位点,但其催化效率较弱,因此一定程度上减缓了整个腐蚀过程。以上表明,与Cl−和SO2−4共存的情况相比,Cl−单独存在时有着更高的腐蚀电流密度和更负的腐蚀电位,见图1、图2和图3。同理,当只存在SO2−4时,Cl−引入也会导致可用吸附位点被部分占据。由于竞争性的相互作用强化了催化腐蚀阶段,加速了腐蚀进程,这与SO2−4单独存在时的情况截然不同。
3. 结 论
研究了普通低碳钢试样在不同pH值的模拟混凝土孔隙溶液中的腐蚀行为,重点强调了Cl−和SO2−4单独或复合情况下的影响。采用电化学测试、XRD和密度泛函理论(DFT)计算等分析方法,阐明了腐蚀演变及其机制。主要结论如下:
(1)当腐蚀离子浓度达到0.1 mol/L时,CH模拟液中钢筋的腐蚀产物明显多于LC中,而当腐蚀离子浓度达到0.4 mol/L时,ST模拟液中的钢筋表面仍未出现明显腐蚀产物。因此,提高pH值可减少钝化膜对Cl−和SO2−4的吸附,提高钢筋的耐腐蚀性,而在低pH值条件下,加入相对低浓度腐蚀离子就会引起钝化膜的破坏,诱发钢筋的腐蚀;
(2) Cl−本身会在较低的浓度阈值下引发腐蚀,如CH溶液中Cl−浓度达到0.02 mol/L时,开路电位(OPC)急剧下降,腐蚀明显加剧,而SO2−4在高浓度下才表现出明显的腐蚀。不过,在Cl−存在的情况下加入SO2−4会因竞争吸附被占据吸附位点,从而在一定程度上缓解整个腐蚀过程。此外,Cl−和SO2−4在整个腐蚀反应中都起着催化剂的作用;
(3)实验、理论和DFT计算结果都支持假设所建立的两阶段反应模型,包括竞争吸附和催化腐蚀,解释了不同pH值的模拟混凝土孔隙溶液中Cl−和/或SO2−4诱导的低碳钢腐蚀过程。SO2−4具有更强的吸附能力,从而减少了Cl−的吸附。然而,在第二反应阶段中,Cl−表现出更高的催化效率,因此复合离子存在情况下的腐蚀风险水平介于Cl−和SO2−4单独造成的风险之间。
-
图 3 不同模拟液中腐蚀阶段钢试样的腐蚀电流密度(Icorr)曲线:(a)第一种模拟液(CH)中;(b)第二种模拟液(LC)中;(c)第三种模拟液(ST)中
Figure 3. Corrosion current density (Icorr) curves of steel specimens in corrosion stage of SCPSs: (a) In the first simulated solution (CH); (b) In the second simulated solution (LC); (c) In the third simulated solution (ST)
图 4 第一种模拟液(CH)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图
Figure 4. Electrochemical impedance spectroscopy (EIS) results and equivalent electrical circuit fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the first simulated solution (CH): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram
图 5 第二种模拟液(LC)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图
Figure 5. Electrochemical impedance spectroscopy (EIS) results and equivalent electrical circuit fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the second simulated solution (LC): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram
图 6 第三种模拟液(ST)中不同腐蚀离子对普通低碳钢试样腐蚀过程的电化学阻抗谱(EIS)结果及等效电路拟合结果:((a), (c), (e)) Nyquist图;((b), (d), (f)) Bode和Phase图
Figure 6. Electrochemical impedance spectroscopy (EIS) results and fitting results for the corrosion process of low-carbon steel specimens by different corrosive ions in the third simulated solution (ST): ((a), (c), (e)) Nyquist diagram; ((b), (d), (f)) Bode and Phase diagram
表 1 不同模拟液中腐蚀电化学阻抗谱(EIS)数据的等效电路拟合结果
Table 1 Equivalent electrical circuit fitting results of electrochemical impedance spectroscopy (EIS) data in different simulated solutions
Content/
(mol·L−1)Rs/
(Ω·cm2)CPE1, Q/
(S·sn·cm−2)CPE1,a
[0<a<1]R1/(Ω·cm2) CPE2, Q/
(S·sn·cm−2)CPE2,a
[0<a<1]Rct/
(Ω·cm2)Chi-squared CH-Cl− 0.01 65.42 0.0000917 0.8863 4164 0.0000714 0.4761 41280 5.62×10−4 0.02 40.35 0.0001129 0.8703 2597 0.0002508 0.4036 6510 1.85×10−3 0.03 42.19 0.0001079 0.8758 2195 0.0002016 0.3551 9236 7.96×10−4 0.05 33.03 0.0001247 0.8633 802.3 0.0004566 0.2367 19660 7.51×10−4 0.07 28 0.0001379 0.8521 752.2 0.0010090 0.3267 13790 6.27×10−4 0.1 23.6 0.0001617 0.83 298.7 0.0015650 0.3055 1665 6.81×10−4 CH-SO2−4 0.01 41.22 0.0001062 0.8848 4059 0.0000951 0.6181 16650 1.05×10−3 0.02 35.17 0.0001150 0.8848 1883 0.0002298 0.5316 6555 6.93×10−4 0.03 30.32 0.0001140 0.8887 1317 0.0002200 0.5174 5769 2.09×10−3 0.05 24.24 0.0001285 0.8705 1027 0.0003002 0.5019 6891 8.19×10−4 0.07 18.98 0.0001310 0.8709 605.9 0.0004202 0.4764 7953 3.39×10−3 0.1 16.46 0.0001365 0.8598 335.3 0.0005371 0.4666 8298 6.53×10−3 CH
Cl−+SO2−40.01 26.53 0.0001563 0.8879 4824 0.0000884 0.8907 26730 1.29×10−3 0.02 20.73 0.0001161 0.8732 1628 0.0001767 0.4851 5558 3.03×10−3 0.03 15.74 0.0001152 0.8735 1646 0.0002093 0.4884 6707 1.83×10−3 0.05 12.29 0.0001198 0.8693 1362 0.0002904 0.4951 7037 8.45×10−4 0.07 13.03 0.0001175 0.8771 565.2 0.0003434 0.4542 7912 1.83×10−3 0.1 11.07 0.0001478 0.8374 235 0.0005624 0.453 9741 4.18×10−3 LC-Cl− 0.01 32.04 0.0001148 0.8847 8330 0.0000563 0.6299 73860 3.93×10−4 0.02 25.3 0.0001290 0.8744 2978 0.0001182 0.6136 20830 5.60×10−4 0.03 24.19 0.0001079 0.8758 2195 0.0002016 0.3551 9236 7.96×10−4 0.05 23.1 0.0001176 0.8458 719.1 0.0002957 0.4679 12410 3.83×10−3 0.07 20.43 0.0001043 0.8391 379.3 0.0004010 0.4495 27850 3.01×10−3 0.1 18.96 0.0001411 0.7874 338.4 0.0004679 0.3499 9680 3.23×10−3 LC-SO2−4 0.01 30.1 0.0001085 0.8736 12400 0.0001089 0.4981 89150 6.82×10−4 0.02 25.22 0.0001202 0.8592 1608 0.0001916 0.4244 13390 9.59×10−4 0.03 23.07 0.0001673 0.8145 1621 0.0000909 0.4929 12360 2.51×10−3 0.05 20.76 0.0001310 0.8047 1110 0.0002258 0.4652 20660 8.88×10−4 0.07 19.5 0.0002658 0.7727 2373 0.0004917 0.4257 40920 1.52×10−3 0.1 14.82 0.0001614 0.7415 7872 0.0005338 0.3576 18148 1.16×10−3 LC
Cl−+SO2−40.01 23.06 0.0001348 0.8229 6727 0.0000550 0.5558 60790 4.27×10−3 0.02 22.16 0.0001216 0.8733 7205 0.0001543 0.5928 12610 2.06×10−3 0.03 18.79 0.0001121 0.8835 841 0.0001819 0.5644 11890 4.18×10−3 0.05 12.29 0.0001198 0.8693 1362 0.0002904 0.4951 7037 8.45×10−4 0.07 11.43 0.0001043 0.8391 379.3 0.0004010 0.4495 27850 3.01×10−3 0.1 10.37 0.0001018 0.8181 2699 0.0006246 0.4161 11730 4.13×10−3 ST-Cl− 0.01 5.391 0.0000566 0.9609 18140 0.0001331 0.6403 323900 5.83×10−3 0.04 5.112 0.0000465 0.9876 19410 0.0001591 0.6505 216900 7.50×10−3 0.07 4.982 0.0000389 0.982 9934 0.0001715 0.6763 141800 5.65×10−3 0.10 4.486 0.0001388 0.9657 1653 0.0002079 0.6374 193900 7.77×10−3 0.19 4.112 0.0001461 0.9329 1604 0.0001977 0.6628 173000 2.59×10−2 0.22 4.658 0.0001180 0.9443 2733 0.0004016 0.5089 16170 2.00×10−2 0.31 3.681 0.0001627 0.9025 2393 0.0004476 0.444 29290 2.54×10−2 0.40 4.152 0.0001806 0.9225 1345 0.0007194 0.5227 8297 2.98×10−2 ST-SO2−4 0.01 5.761 0.0000489 0.9533 45472 0.0002232 0.6262 898000 3.12×10−2 0.04 4.793 0.0000472 0.9437 32150 0.0002417 0.6331 840400 2.02×10−2 0.07 3.71 0.0000440 0.9333 12270 0.0002724 0.6245 314900 1.92×10−2 0.10 4.133 0.0000433 0.9126 11170 0.0002714 0.6367 339800 1.72×10−2 0.19 3.825 0.0002788 0.9491 1614 0.0000467 0.5169 445500 8.33×10−3 0.22 5.145 0.0002587 0.8349 2539 0.0005471 0.5214 17930 2.91×10−3 0.31 3.417 0.0000819 0.9798 836 0.0006337 0.5135 32580 1.98×10−2 0.40 3.221 0.0000762 0.9458 1027 0.0009938 0.4746 12670 3.14×10−2 ST
Cl−+SO2−40.01 5.634 0.0000442 0.9522 89602 0.0000362 0.6685 262700 1.72×10−2 0.04 4.987 0.0000429 0.9726 16280 0.0002398 0.6297 267200 1.04×10−2 0.07 5.009 0.0000435 0.9695 13440 0.0002551 0.6265 15990 4.26×10−3 0.10 4.637 0.0000544 0.9868 1703 0.0003090 0.6111 26560 7.15×10−3 0.19 4.223 0.0001823 0.8697 3961 0.0003349 0.551 21510 2.00×10−3 0.22 3.682 0.0006716 0.9053 1201 0.0009439 0.514 34670 1.32×10−2 0.31 3.418 0.0007192 0.9147 913 0.0011370 0.5202 16320 1.36×10−2 0.40 3.547 0.0009536 0.9461 906 0.0010946 0.5018 8690 2.43×10−2 Notes: Rs—Electrolyte resistance; R1—Passivation film resistance; Rct—Charge transfer resistance; Q, a—Parameters in the constant phase angle elements CPE1 and CPE2; Chi-squared is the chi-squared test result. 表 2 Cl−和SO2−4在Fe(100)表面的吸附能
Table 2 Adsorption energy of Cl− and SO2−4 adsorption on Fe(100) surface
Adsorption energy on Fe(100)/(kJ·mol−1) Top Bridge Hollow Cl− −449.896 −458.134 −363.154 SO2−4 −674.245 −691.320 −739.124 -
[1] 姚燕. 中国混凝土材料耐久性研究的新进展[J]. 中国水泥, 2002(12): 39-42. DOI: 10.3969/j.issn.1671-8321.2002.02.019 YAO Yan. New progress of concrete material durability research in China[J]. China Cement, 2002(12): 39-42(in Chinese). DOI: 10.3969/j.issn.1671-8321.2002.02.019
[2] CARNOT A, FRATEUR I, MARCUS P, et al. Corrosion mechanisms of steel concrete moulds in the presence of a demoulding agent[J]. Journal of Applied Electrochemistry, 2002, 32: 865-869. DOI: 10.1023/A:1020510506504
[3] 张伟平, 张誉, 刘亚芹. 混凝土中钢筋锈蚀的电化学检测方法[J]. 工业建筑, 1998(12): 21-25, 32. ZHANG Weiping, ZHANG Yu, LIU Yaqin. Electrochemical detection of corrosion of steel reinforcement in concrete[J]. Industrial Construction, 1998(12): 21-25, 32(in Chinese).
[4] DEHWAH H A F, AUSTIN S A, MASLEHUDDIN M. Chloride-induced reinforcement corrosion in blended cement concrete exposed to chloride-sulphate environments[J]. Magazine of Concrete Research, 2002, 54(4): 355-364.
[5] ALNPADU K O, TORII K. Chloride ingress and steel corrosion in cement mortars incorporating low-quality fly ashes[J]. Cement and Concrete Research, 2002, 32(6): 893-901. DOI: 10.1016/S0008-8846(02)00721-4
[6] LIU G J, SHEN F M, ZHANG Y S, et al. Reactive molecular dynamics study on carbon steel corrosion induced by chloride: Effects of applied potential and temperature[J]. Construction and Building Materials, 2024, 411: 134250. DOI: 10.1016/j.conbuildmat.2023.134250
[7] 刘国建, 张云升, 刘诚, 等. 模拟混凝土孔溶液中钢筋腐蚀与等效电路选取[J]. 材料导报, 2021, 35(14): 14072-14078. DOI: 10.11896/cldb.20040138 LIU Guojian, ZHANG Yunsheng, LIU Cheng, et al. Simulation of rebar corrosion in concrete pore solutions and equivalent circuit selection[J]. Materials Reports, 2021, 35(14): 14072-14078(in Chinese). DOI: 10.11896/cldb.20040138
[8] JIN Z Q, SUN W, ZHANG Y S, et al. Interaction between sulfate and chloride solution attack of concretes with and without fly ash[J]. Cement and Concrete Research, 2007, 37: 1223-1232. DOI: 10.1016/j.cemconres.2007.02.016
[9] TAMIMI A K, ABDALLA J A, SAKKA Z I. Prediction of long term chloride diffusion of concrete in harsh environment[J]. Construction and Building Materials, 2008, 22(5): 829-836. DOI: 10.1016/j.conbuildmat.2007.01.001
[10] EI-HAWARY M, AL-KHAIAT H, FEREIG S. Performance of epoxy-repaired concrete in a marine environment[J]. Cement and Concrete Research, 2000, 30(2): 259-266. DOI: 10.1016/S0008-8846(99)00242-2
[11] YU H F, DA B, MA H Y, et al. Durability of concrete structures in tropical atoll environment[J]. Ocean Engineering, 2017, 135: 1-10. DOI: 10.1016/j.oceaneng.2017.02.020
[12] YUE Y F, WANG J J, BASHEER P A M, et al. Raman spectroscopic investigation of Friedel's salt[J]. Cement and Concrete Composites, 2018, 86: 306-314. DOI: 10.1016/j.cemconcomp.2017.11.023
[13] HALEEM S M A E, WANEES S A E, BAHGAT A. Environmental factors affecting the corrosion behaviour of reinforcing steel. V. Role of chloride and sulphate ions in the corrosion of reinforcing steel in saturated Ca(OH)2 solutions[J]. Corrosion Science, 2013, 75: 1-15. DOI: 10.1016/j.corsci.2013.04.049
[14] HALEEM S M A E, WANEES S A E, AAL E E A E, et al. Environmental factors affecting the corrosion behavior of reinforcing steel II. Role of some anions in the initiation and inhibition of pitting corrosion of steel in Ca(OH)2 solutions[J]. Corrosion Science, 2010, 52(2): 292-302. DOI: 10.1016/j.corsci.2009.09.004
[15] MAES M, BELIE N D. Resistance of concrete and mortar against combined attack of chloride and sodium sulphate[J]. Cement and Concrete Composites, 2014, 53: 59-72. DOI: 10.1016/j.cemconcomp.2014.06.013
[16] XU Y Z, HE L M, YANG L J, et al. Electrochemical study of steel corrosion in saturated calcium hydroxide solution with chloride ions and sulfate ions[J]. Corrosion Science Section, 2018, 74(10): 1063-1082.
[17] CAO Z L, HIBINO M, GODA H. Effect of nitrite ions on steel corrosion induced by chloride or sulfate ions[J]. International Journal of Corrosion, 2013: 853730.
[18] YANG L J, XU Y Z, ZHU Y S, et al. Evaluation of interaction effect of sulfate and chloride ions on reinforcements in simulated marine environment using electrochemical methods[J]. International Journal of Electrochemical Science, 2016, 11: 6943-6958. DOI: 10.20964/2016.08.51
[19] STROH J, MENG B, EMMERLING F. Deterioration of hardened cement paste under combined sulphate-chloride attack investigated by synchrotron XRD[J]. Solid State Sciences, 2016, 56: 29-44. DOI: 10.1016/j.solidstatesciences.2016.04.002
[20] DONG Q, ZHENG H R, ZHANG L J, et al. Numerical simulation on diffusion-reaction behavior of concrete under sulfate-chloride coupled attack[J]. Construction and Building Materials, 2023, 405: 133237. DOI: 10.1016/j.conbuildmat.2023.133237
[21] DEHWAH H A F, MASLEHUDDIN M, AUSTIN S A. Long-term effect of sulfate ions and associated cation type on chloride-induced reinforcement corrosion in Portland cement concretes[J]. Cement and Concrete Composites, 2002, 24: 17-25. DOI: 10.1016/S0958-9465(01)00023-3
[22] TUMIDAJSKI P, CHAN G W. Effect of sulfate and carbon dioxide on chloride diffusivity[J]. Cement and Concrete Research, 1996, 26: 551-556. DOI: 10.1016/0008-8846(96)00019-1
[23] 宋立康, 王曙光, 徐锋, 等. 硫酸根离子对带裂缝混凝土中氯离子扩散性能的影响研究[J]. 混凝土, 2015(8): 26-30. DOI: 10.3969/j.issn.1002-3550.2015.08.007 SONG Likang, WANG Shuguang, XU Feng, et al. Study on the effect of sulfate ions on the diffusion properties of chloride ions in concrete with cracks[J]. Concrete, 2015(8): 26-30(in Chinese). DOI: 10.3969/j.issn.1002-3550.2015.08.007
[24] 左晓宝, 邱林峰, 汤玉娟, 等. 氯盐和硫酸盐侵蚀下水泥浆体中钢筋锈蚀过程[J]. 建筑材料学报, 2017, 20(3): 352-358, 372. DOI: 10.3969/j.issn.1007-9629.2017.03.006 ZUO Xiaobao, QIU Linfeng, TANG Yujuan, et al. Corrosion processes of steel reinforcement in cement paste under chloride and sulfate attack[J]. Journal of Building Materials, 2017, 20(3): 352-358, 372(in Chinese). DOI: 10.3969/j.issn.1007-9629.2017.03.006
[25] 刘国建, 朱航, 张云升, 等. 混凝土孔溶液中不同侵蚀离子对钢筋的腐蚀行为[J]. 硅酸盐学报, 2022, 50(2): 413-419. LIU Guojian, ZHU Hang, ZHANG Yunsheng, et al. Corrosion behavior of steel reinforcement by different aggressive ions in concrete pore solutions[J]. Journal of the Chinese Ceramic Society, 2022, 50(2): 413-419(in Chinese).
[26] LIU G J, LI M H, YANG L, et al. Electrochemical dielectric response of steel corrosion induced by chloride in simulated concrete pore solution[J]. Journal of Sustainable Cement-Based Materials, 2024, 13(6): 854-864. DOI: 10.1080/21650373.2024.2333257
[27] SHEN F M, LIU G J, LIU C, et al. Corrosion and oxidation on iron surfaces in chloride contaminated electrolytes: Insights from ReaxFF molecular dynamic simulations[J]. Journal of Materials Research and Technology, 2024, 29: 1305-1312. DOI: 10.1016/j.jmrt.2024.01.194
[28] LI W X, GUAN X D, SHI J J. Electrochemical behavior of zinc in alkali-activated fly ash solution[J]. Cement and Concrete Composites, 2024, 146: 105395. DOI: 10.1016/j.cemconcomp.2023.105395
[29] LI Z D, CHEN R N, GAO Y G, et al. Function of Cu-Sb or Al microalloying on the corrosion resistance of 9Cr steel exposed to simulated concrete pore solution[J]. Corrosion Science, 2024, 231: 111983. DOI: 10.1016/j.corsci.2024.111983
[30] MONTEMOR M F, CUNHA M F. Corrosion behavior of rebar in fly ash mortar exposed to carbon dioxide and chlorides[J]. Cement and Concrete Composites, 2002, 24(8): 45-53.
[31] 唐方苗, 徐晖, 陈雯, 等. 模拟混凝土孔隙液中钢筋电化学腐蚀行为及pH值的影响作用[J]. 功能材料, 2011, 42(2): 291-293, 297. TANG Fangmiao, XU Hui, CHEN Wen, et al. Simulation of electrochemical corrosion behavior of steel reinforcement in concrete pore fluids and the role of pH influence[J]. Journal of Functional Materials, 2011, 42(2): 291-293, 297(in Chinese).
[32] 翟海涛, 鲁道荣. 模拟混凝土孔隙液的pH值对钢筋腐蚀的Cl−质量分数的影响[J]. 合肥工业大学学报(自然科学版), 2009, 32(2): 186-189. ZHAI Haitao, LU Daorong. Effect of pH of simulated concrete pore fluid on Cl− mass fraction for rebar corrosion[J]. Journal of Hefei University of Technology (Natural Science), 2009, 32(2): 186-189(in Chinese).
[33] SHIN D M, HUR N Y, KIM W B. Study on increasing high temperature pH(T) to reduce iron corrosion products[J]. Corrosion Science and Technology, 2011, 10(5): 175-179.
[34] LIU L P, LI S L, GAO Z M, et al. Effects of chloride and pH on passivation characteristics of Q235 steel in simulated concrete pore solution[J]. International Journal of Electrochemical Science, 2022, 17(6): 220648. DOI: 10.20964/2022.06.51
[35] 钱如胜. 现代混凝土孔溶液离子演变规律及数值模拟[D]. 南京: 东南大学, 2018. QIAN Rusheng. Evolution law and numerical simulation of ionic evolution in modern concrete pore solution[D]. Nanjing: Southeast University, 2018(in Chinese).
[36] PAYNE M C, TETER M P, ALLAN D C, et al. Iterative minimization techniques for ab initio total-energy calculations: Molecular dynamics and conjugate gradients[J]. Reviews of Modern Physics, 1992, 64: 1045-1097. DOI: 10.1103/RevModPhys.64.1045
[37] CHEVARY J A, VOSKO S H, JACKSON K A, et al. Atoms, molecules, solids, and surfaces: Applications of the generalized gradient approximation for exchange and correlation[J]. Physical Review B, 1992, 46(11): 6671-6687. DOI: 10.1103/PhysRevB.46.6671
[38] VANDERBILT D. Soft self-consistent pseudopotentials in a generalized eigenvalue formalism[J]. Physical Review B, 1990, 41(11): 7892-7895. DOI: 10.1103/PhysRevB.41.7892
[39] MONKHORST H J, PACK J D. Special points for Brillouin-zone integrations[J]. Physical Review B, 1976, 13: 5188-5192. DOI: 10.1103/PhysRevB.13.5188
[40] 宋诗哲. 腐蚀电化学研究方法[M]. 北京: 化学工业出版社, 1988. SONG Shizhe. Methods of corrosion electrochemical studies[M]. Beijing: Chemical Industry Press, 1988(in Chinese).
-
其他相关附件
-
目的
钢筋混凝土结构因其优良的力学性能和耐久性,在现代建筑工程中得到广泛应用。然而,钢筋混凝土在使用过程中面临的主要问题之一是钢筋的腐蚀,这直接影响其使用寿命和结构安全。本文旨在揭示低碳钢在模拟混凝土孔隙溶液中,尤其是在不同pH值条件下,Cl和SO2-4单独及共同作用对其腐蚀行为的影响机制,深入探索这些离子的腐蚀效应及其相互作用。
方法本研究综合运用了电化学测试、X射线衍射(XRD)分析和密度泛函理论(DFT)计算等多种方法。通过在模拟混凝土孔隙溶液中进行腐蚀试验,分别在pH值为12.4、12.9和13.5的条件下,逐步增加Cl和SO2-4的浓度,并监测腐蚀电位、极化电阻、腐蚀电流密度和电化学阻抗谱等参数的变化,分析钢筋的腐蚀行为。同时,利用XRD分析腐蚀产物的成分,并通过DFT计算离子在铁表面的吸附能,以揭示腐蚀机制的微观细节。
结果试验结果显示,在不同pH值的模拟溶液中,随着腐蚀离子浓度的增加,低碳钢的开路电位(OCP)普遍呈现下降趋势。特别是在pH值较低的溶液中,Cl单独存在的情况下表现出较强的腐蚀性,能够迅速破坏钢筋表面的钝化膜,加速电化学反应,导致钢筋的腐蚀速率显著增加。然而,当Cl与SO2-4共存时,SO2-4的存在一定程度上抑制了Cl的腐蚀作用,由于这种竞争吸附作用使钢筋的整体腐蚀速率介于单独存在Cl和SO2-4时的水平之间。相比之下,在pH值较高的模拟溶液中,钢筋的耐腐蚀性显著提高,腐蚀速率显著降低。线性极化电阻测试进一步验证了这一结果,钢筋在高碱性溶液中的耐腐蚀性优于相对较低碱性条件下的情况。此外,电化学阻抗谱分析表明,随着腐蚀离子浓度增加,钢筋的电化学阻抗逐渐减小,反映出腐蚀过程的加剧。此外,XRD分析结果揭示了不同离子情况下腐蚀产物的主要成分相似,包括γ-FeOOH、α-FeOOH、FeO、FeO和Fe(OH)等。通过DFT计算结果进一步确认,Cl和SO2-4在Fe(100)表面均具有负吸附能,表明它们都能有效吸附在钢筋表面,尽管SO2-4的催化腐蚀效率要低于Cl,但它具有更强的吸附能力,使其在竞争吸附中占据优势地位。
结论本研究主要得出以下
结论首先,提高混凝土孔隙溶液的pH值可以有效减少钝化膜对Cl和SO2-4的吸附,从而降低钢筋的腐蚀速率。其次,低浓度的Cl已足以引发显著腐蚀,而SO2-4则需要较高浓度才能表现出明显的腐蚀性。当两者共存时,由于竞争吸附作用的存在,总体腐蚀速率介于单独存在时之间。最后,本研究创新性地提出了竞争吸附-催化腐蚀的两阶段反应模型,深入揭示了Cl和SO2-4在钢筋腐蚀过程中的复杂交互作用机制。Cl要通过破坏钝化膜加速腐蚀进程,而SO2-4则通过影响腐蚀产物的稳定性和分布来参与腐蚀过程。
-
钢筋混凝土结构中钢筋的腐蚀严重影响了结构的耐久性,其主要为电化学腐蚀过程,在某些特定环境下,钢筋表面的钝化膜会遭到破坏,从而导致钢筋腐蚀。其中,Cl-是引发钢筋腐蚀的常见原因,它能够破坏钢筋表面的钝化膜,加速电化学腐蚀过程。同时,SO2-4也可能与钢筋发生化学反应,进一步促进腐蚀的进展,而混凝土的pH值对钢筋的腐蚀速率也有显著影响。
本文旨在阐明低碳钢在不同pH值(12.4、12.9和13.5)的模拟混凝土孔隙溶液中由Cl-和SO2-4引发的腐蚀行为。通过综合运用电化学测试方法、X射线衍射法(XRD)和密度泛函理论(DFT)计算进行分析。最终提出了一个竞争吸附-催化腐蚀的两阶段反应机制模型,揭示了Cl-和SO2-4在钢筋腐蚀过程中的交互作用机制。该模型强调了竞争吸附在初始阶段的作用,以及两种离子在催化腐蚀阶段的不同催化效率。这一研究不仅为复杂环境下的钢筋腐蚀行为提供了深入的理解,也为混凝土结构的耐久性设计和腐蚀防护措施的制定提供了科学依据。
Cl-和SO2-4的竞争吸附及腐蚀过程的示意图





 下载:
下载: