Preparation of magnetic coconut shell biochar and its removal of tetracycline from water
-
摘要:
抗生素类药物在土壤和自然水体中的排放会危害到藻类及低等生物的生存,可能对生态环境带来持续性破坏。为此,本研究以四环素(TC)为研究对象,利用湛江本地特色农业废弃物椰壳为原料,以FeCl3和FeSO4为铁源,通过浸渍、共沉淀和水热合成等方法制备了磁性椰壳生物炭(MBC)。采用SEM、FTIR、XRD、BET、VSM、Zeta及XPS对样品表面形貌及化学结构进行了表征。研究了接触时间、初始TC浓度、pH值、反应温度及共存金属离子对MBC吸附TC的影响。结果表明,pH 4.0时,MBC对TC具有最佳吸附效果,且在24 h达到吸附饱和,饱和吸附量为36.40 mg·g−1,TC去除率达93.37%。高浓度Ca2+和Mg2+会显著降低了MBC对TC的吸附效果,而Na+的影响较小。吸附动力学符合拟二级动力学模型,等温吸附行为符合Langmuir模型,最大吸附容量在45℃时可达46.49 mg·g−1。温度升高有助于提高吸附容量,表明吸附过程为吸热反应。吸附机制主要涉及π-π相互作用、氢键和配位键的形成。MBC在重复利用性实验中表现出优良的稳定性,经过五次吸附-解吸循环后,去除率仍稳定在85.16%。表明磁性椰壳生物炭是一种高效、可重复利用的TC吸附材料,在养殖尾水、医药废水处理等领域具有较好的应用前景。
Abstract:The discharge of antibiotic drugs in soil and natural water bodies can endanger the survival of algae and lower organisms, and may bring continuous damage to the ecological environment. For this reason, in this study, magnetic coconut shell biochar (MBC) was prepared by impregnation, co-precipitation and hydrothermal synthesis using tetracycline (TC), a local speciality agricultural waste in Zhanjiang, as raw material, and FeCl3 and FeSO4 as iron sources. The surface morphology and chemical structure of the samples were characterised using SEM, FTIR, XRD, BET, VSM and XPS. The effects of contact time, initial TC concentration, pH, reaction temperature and different concentrations of metal ions on the adsorption of TC by MBC were investigated. The results showed that MBC had the best adsorption effect on TC at pH 4.0 and reached adsorption saturation at 24 h. The saturated adsorption amount was 36.40 mg·g−1, and the TC removal rate reached 93.37%. High concentrations of Ca2+ and Mg2+ significantly reduced the adsorption of TC by MBC, while the effect of Na+ was small. The adsorption kinetics conformed to the proposed secondary kinetic model, and the isothermal adsorption behaviour conformed to the Langmuir model, with the maximum adsorption capacity up to 46.49 mg·g−1 at 45℃. The increase in temperature contributed to the increase in the adsorption capacity, which indicated that the adsorption process was a heat-absorption reaction. The adsorption mechanism mainly involves π-π interactions, hydrogen bonding and ligand bonding formation.The MBC showed excellent stability in the reusability experiments, and the removal rate remained stable at 85.16% after five adsorption-desorption cycles. It is shown that magnetic coconut shell biochar is an efficient and reusable TC adsorbent material, which has a good application prospect in the fields of breeding tail water and pharmaceutical wastewater treatment.
-
Keywords:
- Magnetic /
- Coconut shell /
- Biochar /
- Adsorption /
- Tetracycline
-
近年来,抗生素类药物的使用越来越广泛。它们不仅在农业、水产等领域有助于增产增收,也在促进人体健康、预防细菌感染等方面发挥着至关重要的作用[1]。抗生素是用于治疗和预防细菌感染最广泛的一类药物,通常在动物体内的代谢不够完全[2],多达90%的口服剂量未能降解,作为活性化合物通过尿液和粪便排出体外。因此,抗生素在土壤和自然水体中的释放引起了科学界的广泛关注。抗生素在水生环境中对藻类和其他低等生物具有毒性,可能对生态可持续性造成长期影响[3]。即使在极低浓度下,抗生素也会对人类和动物造成急性和慢性毒性等不良反应,如细菌失衡、胃肠道不适,甚至肝损伤[4]。因此,必须采取有效措施去除水中的抗生素,以降低其对生态环境和人类健康的潜在风险。
目前,抗生素的去除主要采用电化学法[5]、吸附法、深度氧化法和反渗透法等[6]。吸附法因其简单操作和低能耗而成为常用的方法[7]。常见吸附材料,如金属有机骨架[8]、功能生物炭[9]、石墨烯[10]和碳纳米材料[11]已经应用于水中抗生素的处理。吸附法具有简单、安全、无二次污染、可行性高和运行成本低等许多优点[12],被认为是一种具有广泛前景的抗生素去除方法。
生物炭(BC)是一种多孔且富含碳的吸附材料[13]。BC因其吸附性好、来源广泛、成本效益高等特点,在污染物去除领域得到了广泛研究与应用。日常生活中一些常见的农林废弃物常被用作BC的制备原料,如甘蔗渣、玉米秸秆和核桃壳等[14]。然而,BC的吸附能力和分离效率存在一些不足之处。在污水处理后,BC颗粒很难与污水有效地分离。如果没有及时提取,大量被BC吸附的污染物可能会导致二次污染,这对BC的循环利用不利,限制了BC在水处理中的实际应用。过去,分离BC常采用过滤的方式,但通常会导致过滤膜堵塞,也会失去吸附材料[15]。因此,需要进一步改进BC的吸附能力和分离效率。现有研究发现,BC在吸附抗生素过程中表现出较好的吸附性能,但在污水处理后的分离效率低,容易造成二次污染。例如, Pandey等[16]指出,BC在处理含抗生素污水时,常出现吸附剂与污水难以有效分离的问题,影响了生物炭的循环利用。此外,Yao等[17]的研究表明,在不同pH值、温度和共存离子条件下,生物炭的吸附性能差异较大,限制了其在复杂废水处理中的应用。
为克服上述问题,近年来磁性生物炭因其具备磁性可分离特性和良好的吸附性能,成为研究热点。磁性改性不仅能显著提高BC的吸附能力,还能通过外加磁场实现吸附剂的高效分离和回收。重要的是,加载的磁性颗粒并不会显著改变污染物的亲和力[18]。同时,使用磁性生物炭有望增强对污染物的去除效果。例如,Liang等[19]通过将纳米铁锰氧化物负载于松木锯末生物炭上,制备了磁性生物炭,并证明其在吸附盐酸四环素方面具有良好性能。类似地, Zhou等[20]通过将FeCl₃预处理的澳洲坚果壳通过机械化学活化制备了磁性生物炭,并证明其在吸附重金属方面具有良好性能。Jiao等[21]的研究展示了Fe改性木质素基磁性生物炭在水中微塑料吸附和原位催化热降解方面的潜力,进一步表明磁性生物炭在环境污染治理中的广泛应用前景。Hang等[22]通过铁酸钾加速水热碳化制备了超顺磁性多孔生物炭,证明其在去除四环素方面表现出优异的性能。然而,这些研究也指出了磁性生物炭在实际应用中的一些问题,例如,磁性颗粒负载量不足、材料稳定性差和再生利用难度高等。
针对上述问题,本研究以湛江本地特色农业废弃物椰壳为原料,以FeCl3和FeSO4为铁源,通过NH3·H2O调节pH,经浸渍、共沉淀和水热等过程制备了磁性椰壳生物炭(MBC)。对制备的MBC进行了表征,研究其理化性质。以四环素(TC)为研究对象,考察了MBC对四环素(TC)的吸附动力学、吸附等温线和吸附热力学分析了吸附过程的潜在机制。同时,探究了pH值、温度及共存金属离子对吸附效果的影响并评估了MBC的重复利用性。本研究旨在通过改造农业废弃物资源为水体中抗生素的污染物的高效去除提供新的思路和方法,以促进农业废弃物的资源化利用和水环境治理。
1. 材料与方法
1.1 材料和试剂
椰子采自广东海洋大学校园内椰子树。分析试剂TC,纯度≥98% ,购自上海易恩化学技术有限公司,HCl购自哈尔滨市化学化工试剂厂,25% NH3·H2O、CH2H6O、FeCl3、FeSO4、NaOH,均购自中国上海麦克林生化科技有限公司。
1.2 生物炭的制备
从椰子中取出椰壳,用自来水和超纯水依次冲洗,70℃干燥,粉碎,过100目筛。将4 g椰壳粉和3.33 g FeCl3、1.83 g FeSO4与100 mL超纯水混合在500 mL烧杯中,用玻璃棒搅拌均匀后在磁性搅拌器中继续搅拌6 h (400 r/min);加入30 mL 25%NH3·H2O ,继续搅拌30 min,静置4 h;过滤,滤渣用乙醇洗涤3次,并用超纯水洗至中性;将滤渣转移至聚四氟乙烯内衬的不锈钢反应釜中,加入100 mL纯净水,温度设置200℃,密闭反应12 h,使其碳化;取出,过滤,将滤渣在70℃下烘干至恒重,制得磁性椰壳生物炭,命名为MBC。采用相同方法,以椰壳粉为原料制备未改性的原始椰壳生物炭(BC)。
1.3 表征方法
(1) SEM测试: 使用赛默飞Inspect F50场发射扫描电子显微镜观察样品表面形貌,分析BC和MBC的微观结构。
(2) FTIR测试:采用傅里叶变换红外光谱仪(Avatar360, USA),通过溴化钾压片法对BC和MBC吸附TC前后的样品进行红外光谱分析,波数范围
4000 ~400 cm−1,光学分辨率4 cm−1。(3) XRD测试:利用Rigaku SmartLab SE X射线衍射仪分析MBC的晶体结构,扫描范围2θ=5°~80°,激发波长λ=0.15 nm,扫描速率5°/min。
(4) BET测试:使用麦克ASAP2460全自动比表面积及孔隙度分析仪,通过氮气吸附-脱附法测定BC和MBC的总比表面积、总孔容和孔径,脱气温度200°C,时间12 h。
(5) VSM测试:采用Lake Shore 7404振动样品磁强计,在25℃、磁场强度7 T下,测量MBC的磁性,磁矩测量灵敏度5×10−8 emu。
(6) Zeta电位测试:使用Nano S90动态光散射纳米粒度仪测定MBC的Zeta电位,样品浓度1~5 mg·mL−1,分散介质电导率
0.0153 mS/cm,测试温度25℃,pH值中性。(7) XPS测试:利用赛默飞EscaLab 250 Xi X射线光电子能谱仪,分析MBC吸附TC前后表面的元素和价态分布,对C1s、O1s、N1s和Fe2p的精细谱进行分峰拟合,测试参数为全谱采集电压15 kV,灯丝电流5 mA,通能160 eV;精细谱电压15 kV,灯丝电流10 mA,通能40 eV,电荷校正以C1s=284.80 eV结合能为标准。
1.4 MBC吸附性能测试
将200 mg MBC加入40 mL不同浓度的污染物溶液中,置于100 mL锥形瓶中,在旋转摇床上以120 r/min的恒定转速,对TC进行批量吸附实验。考察pH、共存金属离子、接触时间、污染物TC浓度、反应温度等因素对MBC吸附TC的影响。在采样点,用0.45 μm微孔膜对水溶液进行快速过滤,用紫外-可见分光光度计(UV-1800,中国上海)在355 nm波长处测量溶液中TC的浓度。每次实验平行三次,并对平均值进行分析。同时进行了吸附动力学、吸附等温线和吸附热力学实验。由于吸附反应过程在
1560 min结束,因此在0~1560 min之间选取8个点来研究吸附动力学。由于吸附过程具有前期快、后期慢的特点,时间间隔的选择遵循前期密集采样、后期松散采样原则。采用平衡法计算t时刻生物炭对TC的去除率(η,%)和吸附量(qt, mg·g−1):η=C0−CtC0×100% (1) qt=(C0−Ct)Vm (2) 式中:η为去除率,C0 (mg·L−1),Ct (mg·L−1)、V (L)和m (g)分别表示初始TC浓度、t时刻的TC浓度、溶液体积和吸附剂用量,本实验中初始TC浓度为100~350 mg/L。
本研究采用拟一级动力学模型(3)、拟二级动力学模型 (4)、Elovich模型(5)、内扩散模型(6)和Boyd模型(7)对吸附过程中的实验数据进行拟合,拟合方程如下:
qt=qe(1−e−ktt) (3) qt=k2q2et1+k2qet (4) qt=kit0.5+Ci (5) qt=1βln(αβ)+1βlnt (6) Bt=−0.4977−ln(1−qtqe) (7) 式中,k1 (min−1)、k2 (g·mg−1·min−1)和kip (mg·g−1·min−0.5)分别为拟一级、拟二级和内扩散模型的速率常数, C是涉及厚度、边界层的常数。α和β是与吸附过程相关的常数。α 通常与初始吸附速率相关,而 β则与吸附过程的活化能相关。
采用Langmuir模型(8~9)、Freundlich模型(10)和Dubinin-Radushkevich模型(11~13)考察了MBC对TC的吸附过程,等温线方程如下:
qe=qmKLCe1+KLCe (8) RL=11+KLCe (9) qe=KFC1ne (10) qe=qmexp(−KDRε2) (11) ε=RTln(1+1Ce) (12) E=1√2KDR (13) 式中,qm (mg·g−1)为MBC对TC的平衡吸附量,Ce为吸附平衡时溶液中残留的TC浓度,KL (L·mg−1)和KF [mg·g−1/(L·mg−1)n]分别为Langmuir和Freundlich模型的吸附速率常数,KDR(mol2·kJ−2)为Dubinin-Radushkevich模型中与吸附能相关的常数,n为Freundlich模型中与吸附强度相关的常数,ε (J·mol−1)为Dubinin-Radushkevich模型的Polanyi势能,R (8.314 J·mol−1·K−1)为标准气体常数,T (K)为绝对温度,E (kJ·mol−1)为MBC表面的平均吸附自由能。
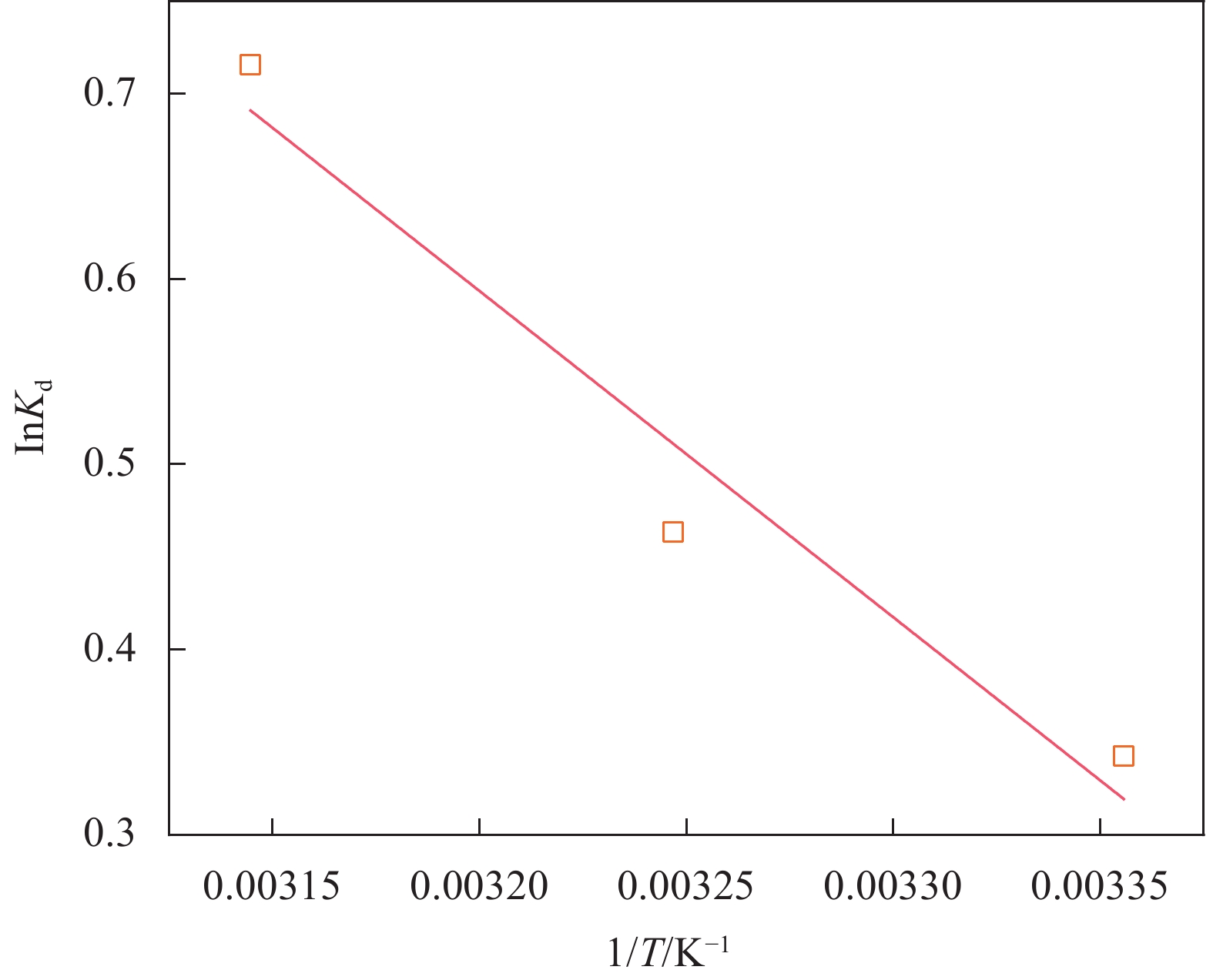
根据Van't Hoff方程,计算与吸附相关的热力学参数ΔG、ΔH、ΔS,具体公式如下:
ln(Kd)=−ΔGRT=ΔSR−ΔHRT (14) Kd=qeCe (15) 式中,Kd是吸附平衡时吸附质在固液两相中的分配系数。
2. 结果与讨论
2.1 生物炭的表征
2.1.1 BC和MBC的微观形貌
图1所示为所得BC的扫描电镜图。其中图1(a)为研磨前生物炭的SEM图,由图可以看出,限氧热解法制得的生物炭颗粒较大,呈管束状多孔结构,表面光滑。这是热解过程中,纤维素、半纤维素与木质素等有机成分脱水及残留水分挥发所导致的[23]。研磨后的生物炭粒径明显变小,但依然保持着光滑表面特征,如图1(b)所示。BC的多孔结构为其表面磁改性及吸附质的附着提供了充足的活性位点。经过Fe源修饰后,在图1(c1,c2)中可以观察到明显的固体颗粒附着在BC表面,这主要归因于Fe3O4的成核和晶体生长[24]。这些晶体排列紧密,在BC表面及间隙中还能观察到明显的微团聚现象[25],表明磁改性处理成功。均匀的颗粒分布和纳米级别的颗粒尺寸增加了生物炭的比表面积和吸附位点。图1(d1,d2)所示为磁改性后的生物炭(MBC)在吸附TC后的表面变化,由图可知,生物炭间隙中分布的Fe3O4晶体团簇明显减少,可能是TC中的羧基(—COOH)和羟基(—OH)基团与Fe3+形成络合物,导致Fe3O4部分溶解所致[26]。Fe3O4的催化活性使其在吸附过程中催化TC中的酚羟基(—OH)和胺基(—NH2)氧化生成有机酸等产物,这些产物与Fe3O4进一步反应,导致Fe3O4晶体团簇的减少[27,28]。此外,搅拌作用导致Fe3O4晶体脱落也可能是晶体团簇减少的原因。但生物炭表面依然附着有大量Fe3O4晶体,为该材料的二次利用提供了保障。
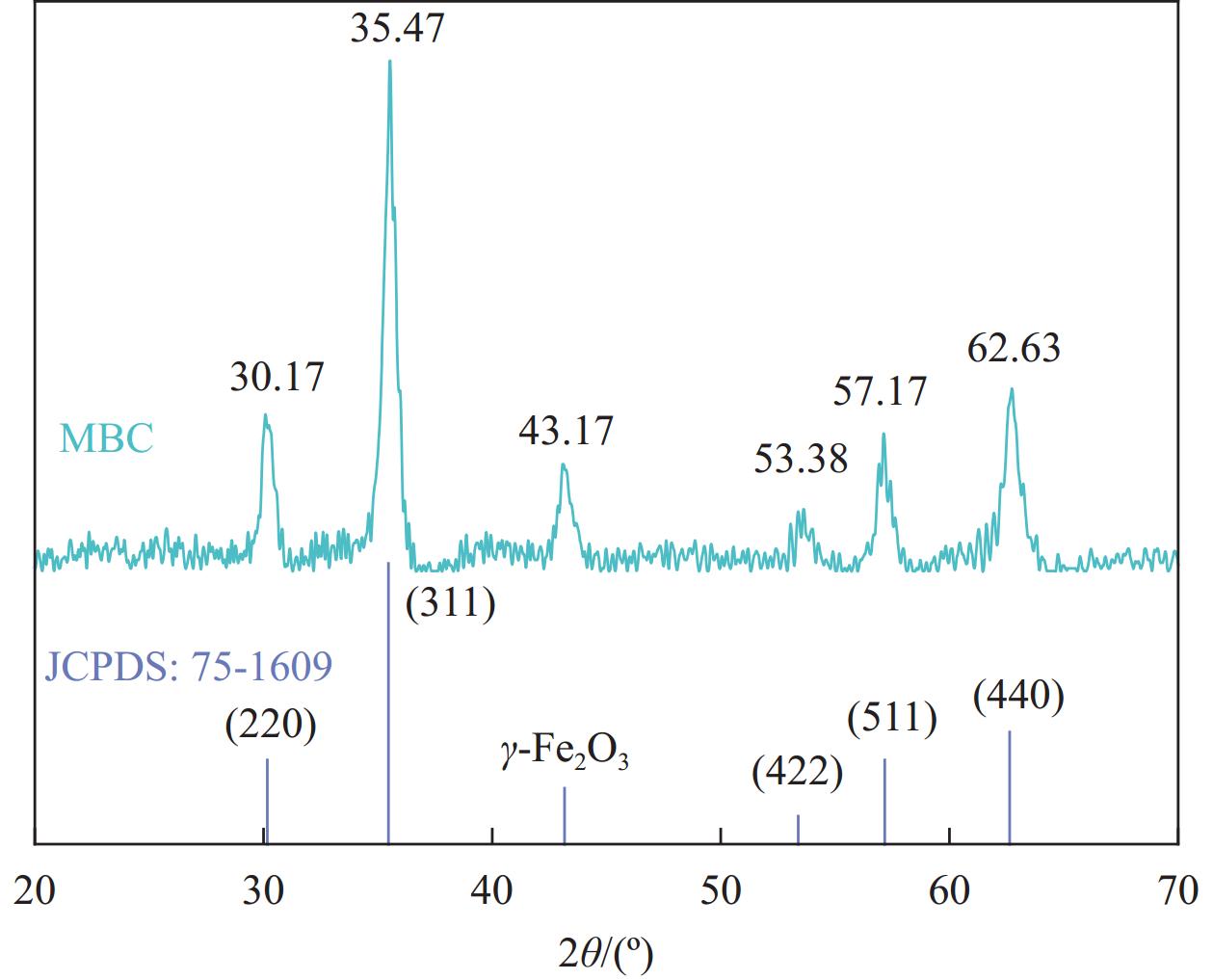
2.1.2 利用XRD分析MBC的结晶性能
图2是MBC的XRD谱图,图中2θ = 30.17°、35.47°、53.38°和57.16°处峰分别对应于Fe3O4的(220)、(311)、(422)和(511)晶面[29], 2θ = 43.17°处峰主要归属于γ-Fe2O3[30],表明材料表面附着的晶体主要为Fe3O4和γ-Fe2O3,这种混晶负载有望为MBC吸附TC提供更为丰富的吸附活性位点。
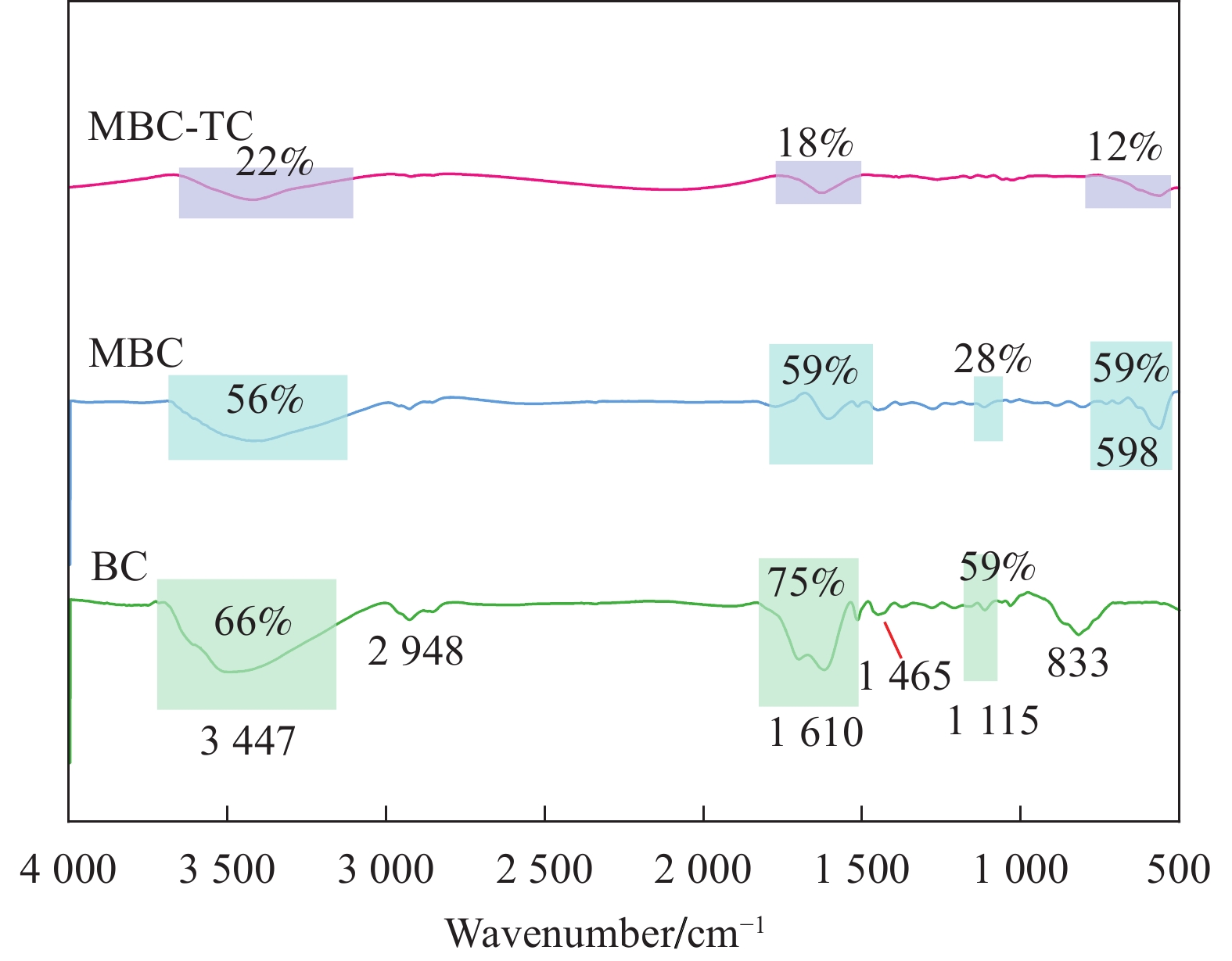
2.1.3 利用FTIR分析BC和MBC吸附TC前后的官能团
图3所示为生物炭材料的FT-IR光谱图。图中, BC在
3447 cm−1、2948 cm−1、1626 cm−1、1465 cm−1、1132 cm−1和833 cm−1等处显示出明显的特征吸收峰,分别对应于羟基(—OH,66%)、脂肪族C—H、C=C (75%)、C—H、C—O (59%)和芳香族C-H官能团,这些特征表明生物炭中富含多种含氧官能团,为TC提供了潜在的活性位点[31–33]。磁改性后的MBC不仅保留了上述特征峰型,还在593 cm−1处新增了一个强吸收峰(59%),该峰归属于Fe-O伸缩振动[34],表明铁氧化物成功掺杂至MBC中,是材料具备磁性的关键所在。MBC吸附TC前,3447 cm−1处的羟基(—OH)峰强度为56%,1610 cm−1处的C=C峰强度为59%,1115 cm−1处的C—O峰强度为28%。在吸附TC后,主要官能团的吸收峰强度明显降低,3447 cm−1处的羟基(—OH)峰强度降至22%,1610 cm−1处的C=C峰强度降至18%,表明TC分子通过氢键与羟基发生了强烈相互作用,导致游离羟基数量减少。此外,598 cm−1处的Fe-O峰强度从59%减弱至12%,进一步证实了铁氧化物在吸附过程中的重要作用[35]。2.1.4 BC和MBC吸附TC前后的N2吸附等温线分析
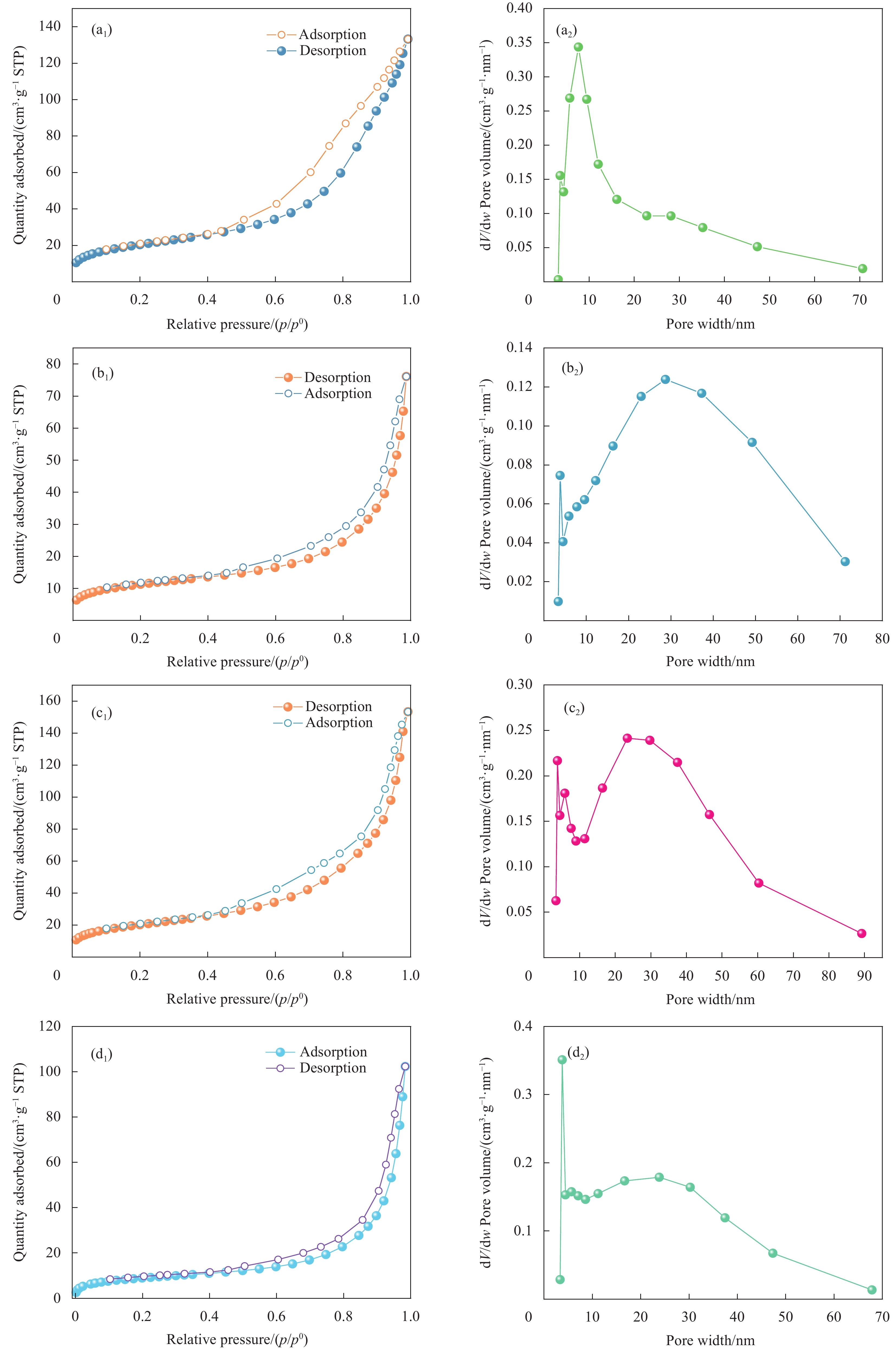
图4(a1~c1)是生物炭材料的N2吸附-脱附曲线图,BC在低相对压力(P/P0 < 0.1)时吸附量较小,此时主要是单层吸附,吸附拐点< 0.1 ;在中等相对压力范围内(0.1 < P/P0 < 0.8),随着相对压力增大,N2吸附量缓慢增加,且当P/P0 > 0.4,脱附曲线开始呈现典型的IV型等温线特征并带有滞后环,这是N2向孔内扩散的结果,表明材料具有介孔特征[36];当 P/P0 > 0.8时,吸附量迅速增加,这是由多层吸附所导致。降低相对压力,BC的吸附量亦随着迅速下降。MBC的N2吸-脱附曲线形状与BC基本一致,但在P/P0 = 1时的吸附量更小,表明MBC的总孔体积较小;MBC的脱附滞后量小于BC,表明MBC的平均孔径较大。吸附TC后的MBC曲线的形状与吸附前基本一致。
![]() 图 4 N2吸附-脱附曲线:(a1) BC;(b1) 吸附TC前的MBC;(c1) 吸附TC后的MBC;(d1) 吸附TC再生后的MBC与孔径分布图:(a2) BC;(b2) 吸附TC前的MBC;(c2) 吸附TC后的MBC;(d2) 吸附TC再生后的MBCFigure 4. N2 adsorption-desorption curves: (a1) BC; (b1) MBC before adsorption of TC; (c1) MBC after adsorption of TC; (d1) MBC after regeneration. Pore size distribution: (a2) BC; (b2) MBC before adsorption of TC; (c2) MBC after adsorption of TC; (d2) MBC after TC regeneration.
图 4 N2吸附-脱附曲线:(a1) BC;(b1) 吸附TC前的MBC;(c1) 吸附TC后的MBC;(d1) 吸附TC再生后的MBC与孔径分布图:(a2) BC;(b2) 吸附TC前的MBC;(c2) 吸附TC后的MBC;(d2) 吸附TC再生后的MBCFigure 4. N2 adsorption-desorption curves: (a1) BC; (b1) MBC before adsorption of TC; (c1) MBC after adsorption of TC; (d1) MBC after regeneration. Pore size distribution: (a2) BC; (b2) MBC before adsorption of TC; (c2) MBC after adsorption of TC; (d2) MBC after TC regeneration.利用吸-脱附曲线计算了材料孔径分布,结果如图4 (a2~d2)所示。BC的孔径主要分布在5~40 nm,10 nm左右的介孔分布最多,为0.35 cm3·g−1。MBC的孔径主要集中在5~70 nm,30 nm左右的孔分布最多,约为0.14 cm3·g−1。相较于BC,磁改性后的MBC总孔体积更小,平均孔径更大。这是因为Fe3O4或Fe2O3晶体在形成时易堵塞较小的介孔,导致BET法测得的孔体积偏小,孔径偏大[37]。MBC吸附TC后的总孔体积有所增加,而平均孔径略有减小,这可能是由于振荡实验使部分封堵介孔的晶体粒子脱落所致。再生后的 MBC 的 BET 数据表明,孔径主要集中在 5~70 nm,与吸附后的MBC基本一致,表明材料再生过程中孔结构未发生明显改变。再生后的 MBC 的总体孔体积略有减少,可能是再生过程中少部分结构发生了坍塌所致。但仍保留了主要的介孔结构,为材料的二次利用提供了保障。
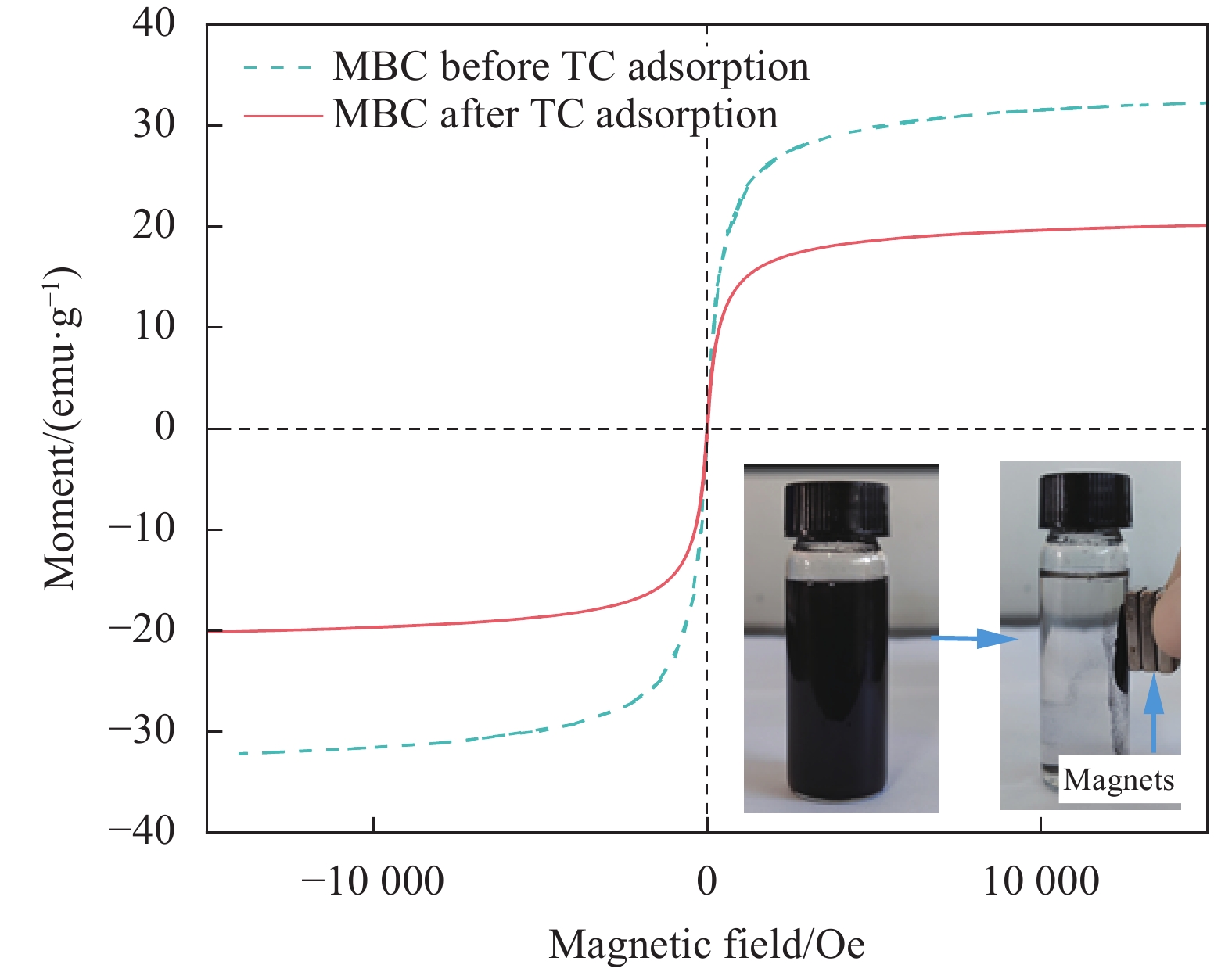
2.1.5 MBC的饱和磁化强度
图5所示为MBC吸附TC前后的磁滞回线。吸附前,MBC的饱和磁化强度为32.3 emu·g−1,矫顽力为10.7 Oe和剩磁为0.74 emu·g−1,这表明MBC具有超顺磁性,这是因为材料表面负载了磁性Fe3O4纳米粒子的缘故。基于纯Fe3O4纳米粒子的饱和磁化强度 65.2 emu/g[38],计算出材料表面Fe3O4纳米粒子的负载量为49.5%。吸附TC后,MBC的饱和磁化强度下降至20.3 emu/g。磁化强度的下降可能是材料表面吸附了TC导致磁粒子的质量分数降低所致,也可能是吸附实验导致部分磁粒子脱落所致。尽管MBC在吸附TC后磁性有所减弱,其依然具备超顺磁性特征,因此,吸附TC后MBC可以通过磁力进行回收[39]。将MBC回收后水体可以恢复至澄清透明,如图5所示。该性能为磁性生物炭在水中污染物去除领域的应用奠定了良好的基础。
2.2 MBC去除TC的实验研究
2.2.1 溶液pH的影响
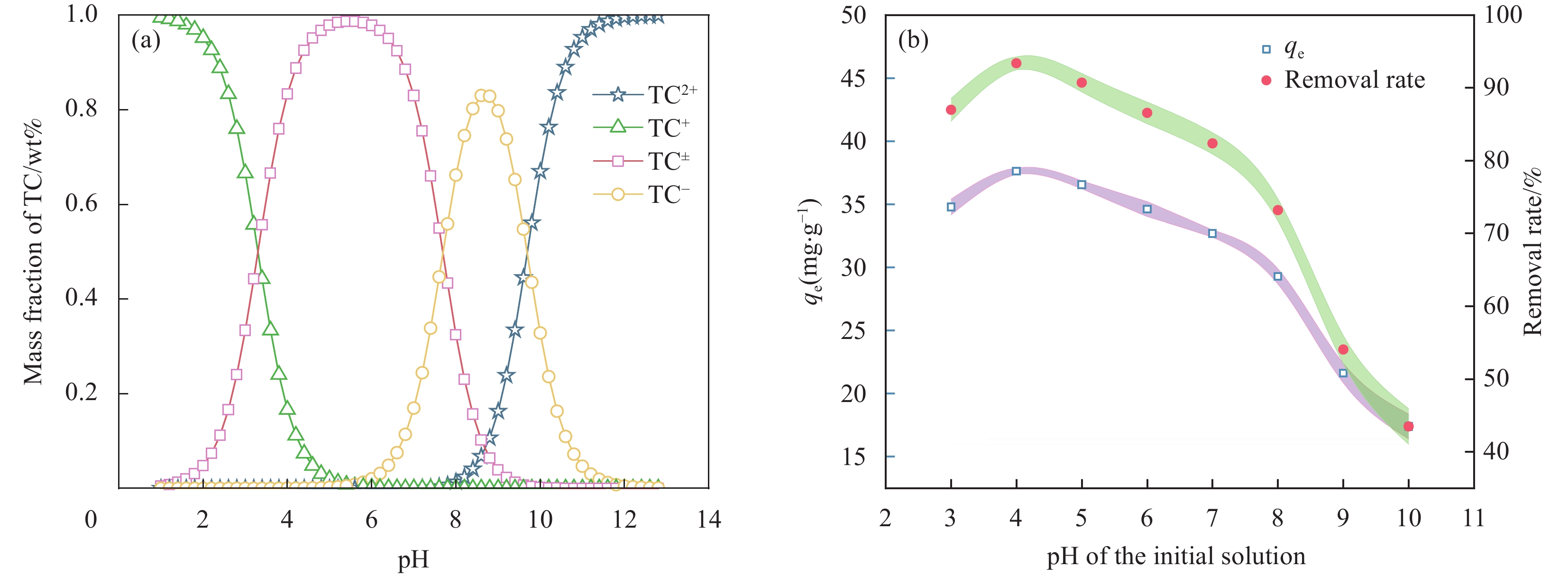
溶液pH是影响材料吸附性能的关键因素,因为pH会直接影响到吸附剂与吸附质表面的电位,也会影响到部分吸附质的型体分布,进而影响到吸附剂与吸附质之间的静电作用[40]。TC是一种具有多种官能团的亲水性两性分子。TC的不同解离常数(pKa = 3.30、7.68和9.68)决定了它在不同pH的水溶液中存在四种型体:阳离子(TC+)、分子(TC±)和阴离子(TC−和TC2−)[41],如图6(a)所示。pH = 4时, MBC对TC的吸附量最高,为37.62 mg·g−1,吸附率为93.37%。这是因为MBC的表面ζ电位为−20.00±0.70 mV,而酸性条件下TC中的叔氨基易质子化为铵离子,并通过正负电荷的静电作用而被MBC吸附。TC分子结构中含有大量含氧基团,可通过氢键作用与MBC表面结合。吸附TC后,MBC的表面ζ电位增加至−17.97±0.49 mV。随着溶液酸性增强,MBC的吸附效率略有下降,这是质子氢与铵离子在MBC表面竞争吸附的结果。随着溶液pH的增加,TC在溶液中的分布以阴离子型体为主,这些阴离子与MBC表面发生排斥,导致吸附量和TC去除率逐渐下降,如图6(b)所示。
2.2.2 共存金属离子的影响
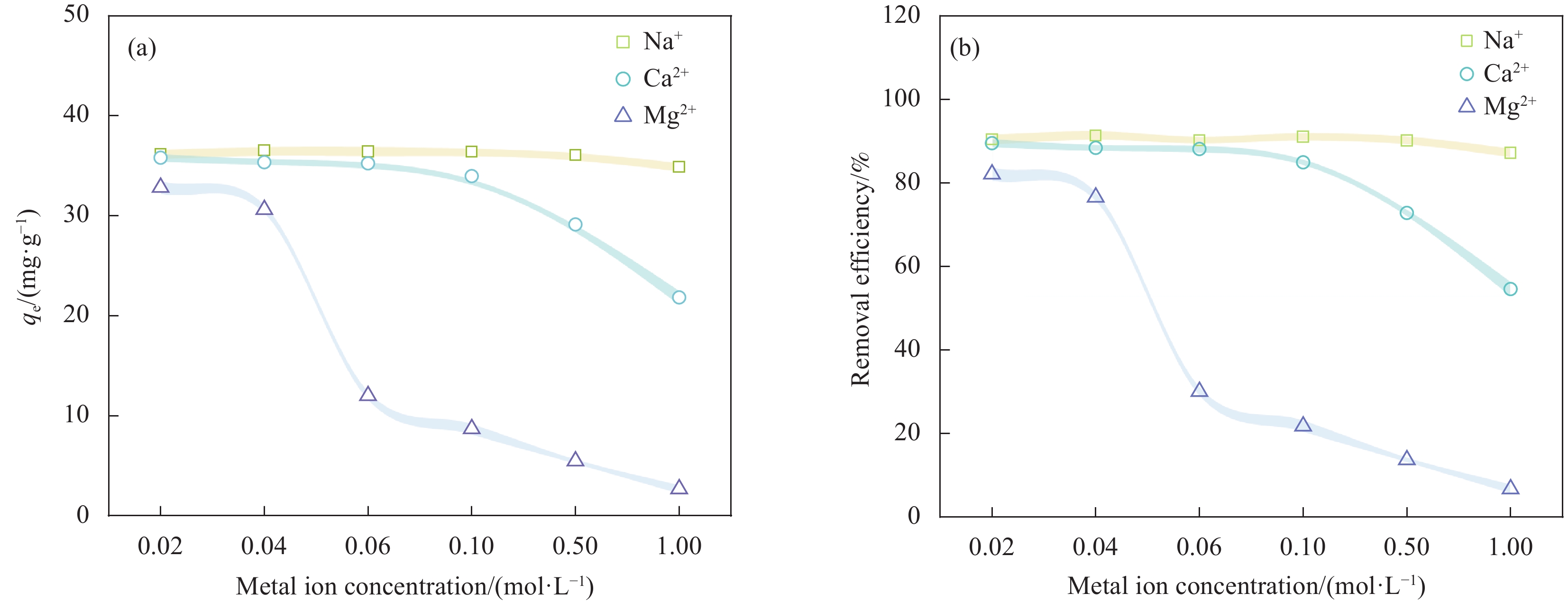
在最佳pH 4.0下,探究了Na+、Ca2+和Mg2+三种金属离子的竞争作用对MBC吸附TC的影响,结果如图7所示。对于Na+,随着浓度由0.02 mol/L增大到1.0 mol/L时,其对MBC吸附TC几乎无影响,去除率始终维持在90%左右。对于Ca2+,在0.02 mol/L浓度下,吸附量下降为35.80 mg·g−1,去除率下降为88.50%;在1 mol/L浓度时,吸附量降至21.83 mg·g−1,去除率降至54.58%。对于Mg2+,其影响最为显著,在0.02 mol/L浓度下,吸附量为32.83 mg·g−1,TC去除率为82.10%;在1 mol/L浓度下,吸附量仅为2.69 mg·g−1,TC去除率降至6.73%。表明,随着金属离子浓度的增加,二价金属离子(Ca2+和Mg2+)易与MBC表面的含氧基团发生强烈的络合竞争[42],导致吸附位点被占据,进而影响MBC对TC吸附去除效率。
2.2.3 动力学分析
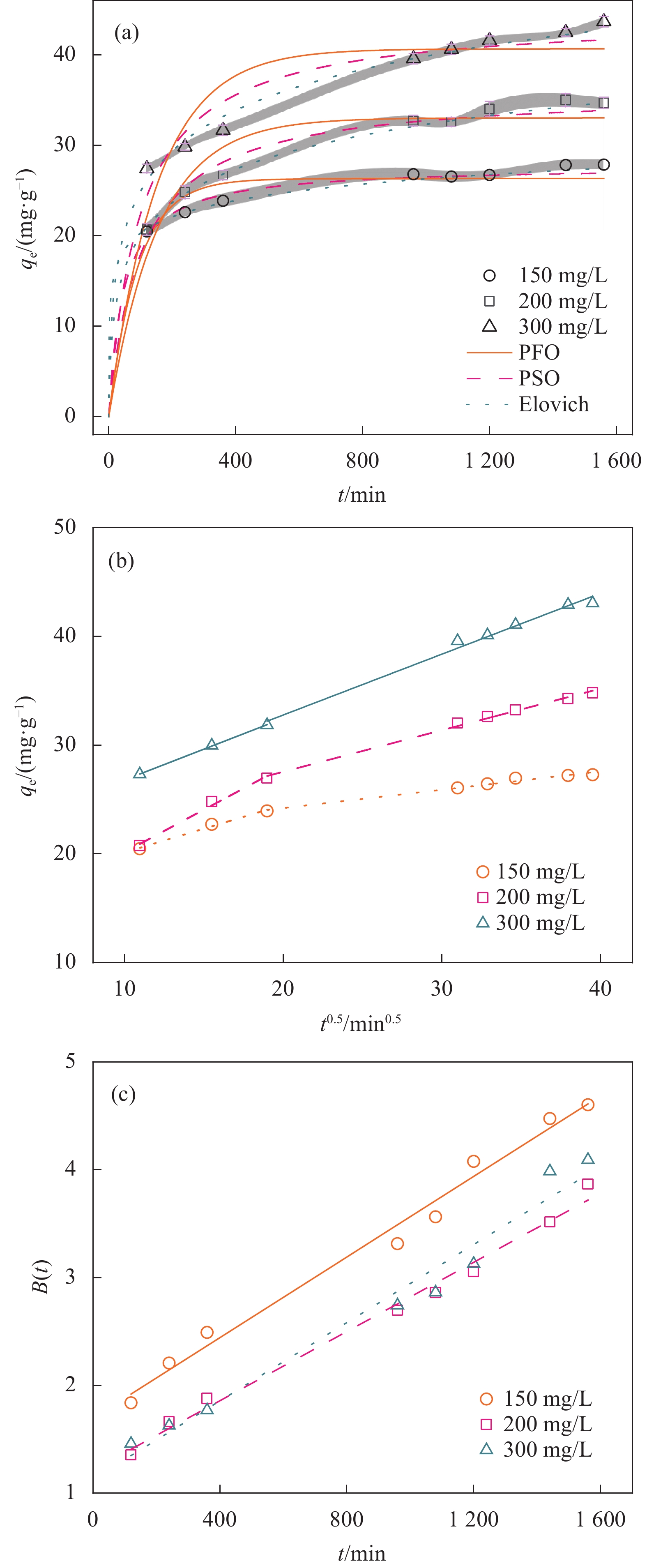
通过间歇性实验探究了MBC对TC的吸附动力学行为,结果如图8(a)所示。MBC对TC的吸附呈现先快后慢的特征,前2 h内的吸附速率较快,4 h后吸附速率减缓,直至24 h后继续延长接触时间对吸附量几乎无影响。利用拟一级、拟二级和Elovich动力学模型对实验数据进行非线性拟合,结果如图8(a)所示,拟合参数列于表1。
表 1 MBC吸附TC的动力学参数Table 1. Kinetic parameters of TC adsorption onto MBCAdsorption kinetics Parameters 150/(mg·L−1) 200/(mg·L−1) 300/(mg·L−1) Values R2 Values R2 Values R2 Experimental qe/(mg·g−1) 27.3 — 34.8 — 43.0 — PFO model k1/(min−1) 0.0109 0.981 0.00645 0.972 0.00655 0.947 qe/(mg·g−1) 26.3 33.0 40.8 PSO model k2/(g·mg−1·min−1) 7.67×10−4 0.998 2.74×10−4 0.994 2.31×10−4 0.981 qe/(mg·g−1) 27.7 36.0 44.3 Elovich model α/ (g·mg−1·min−2) 61.7 0.992 2.12 0.999 2.87 0.982 β/ (mg·g−1·min−1) 0.383 0.185 0.153 IPD model ki1/(mg−1·g−1min−0.5) 0.437 0.985 0.781 0.982 0.566 0.999 C1/(mg·g−1) 15.8 12.4 21.1 ki2/(mg−1·g−1min−0.5) 0.169 0.978 0.382 0.993 0.559 0.986 C2/(mg·g−1) 20.8 19.9 21.6 Notes: qe: Amount of TC adsorbate at equilibrium k1: Rate constant of the pseudo-first-order adsorption
k2: Rate constant of the pseudo-second-order adsorption α: Initial adsorption rate of the Elovich model
β: Desorption constant of the Elovich model ki1: Intraparticle diffusion rate constant at the first stage
C1: Boundary layer thickness in the intraparticle diffusion model at the first stage
ki2: Intraparticle diffusion rate constant at the second stage R2: Correlation coefficient
C2: Boundary layer thickness in the intraparticle diffusion model at the second stage由表1可知,拟二级模型和Elovich模型都适合描述动力学实验参数,而拟二级动力学模型的R2最高,为0.981~0.998,且其qe,cal与qe,exp更加接近,表明TC在MBC表面的吸附主要是化学吸附[43]。拟二级动力学模型是一种特殊的Langmuir动力学模型,它假设吸附质浓度随时间是恒定的,吸附剂上的吸附位点数等于吸附平衡时吸附质数量[44]。随着初始TC浓度增加,吸附速率常数k2从7.67×10−4 g·mg−1·min−1下降至2.31×10−4 g·mg−1·min−1,这是因为在较高浓度下,TC对吸附表面活性位点的竞争更加激烈[45]。Elovich模型认为吸附剂表面是不均匀的,在表面覆盖率较低时,吸附过程与解吸过程之间的相互作用不会显著影响吸附动力学[46]。Elovich的参数α和β分别表示初始吸附速率和解吸系数,在所有浓度下,参数α均远高于参数β,表明TC与MBC存在较强的吸附作用,而解吸速率则很低,符合化学吸附的特征。
为了探究影响吸附作用的速率控制步骤,利用内扩散模型和Boyd模型对动力学数据进行拟合,结果如图8(b)(c)所示,拟合结果列于表1。由图8(b)可知,内扩散模型在达到吸附平衡前主要为两段式,这是因为MBC内部分布着很多的小孔,TC向小孔内扩散时速率较低所致。第一段拟合线未过零点,表明内扩散不是唯一速控步骤,MBC对TC的吸附速率受多个步骤影响[47]。由图8(c)可知,Boyd模型的拟合线在三种初始TC浓度下均未过零点,表明TC的传质过程中存在着液膜外扩散步骤[48]。
2.2.4 等温线分析
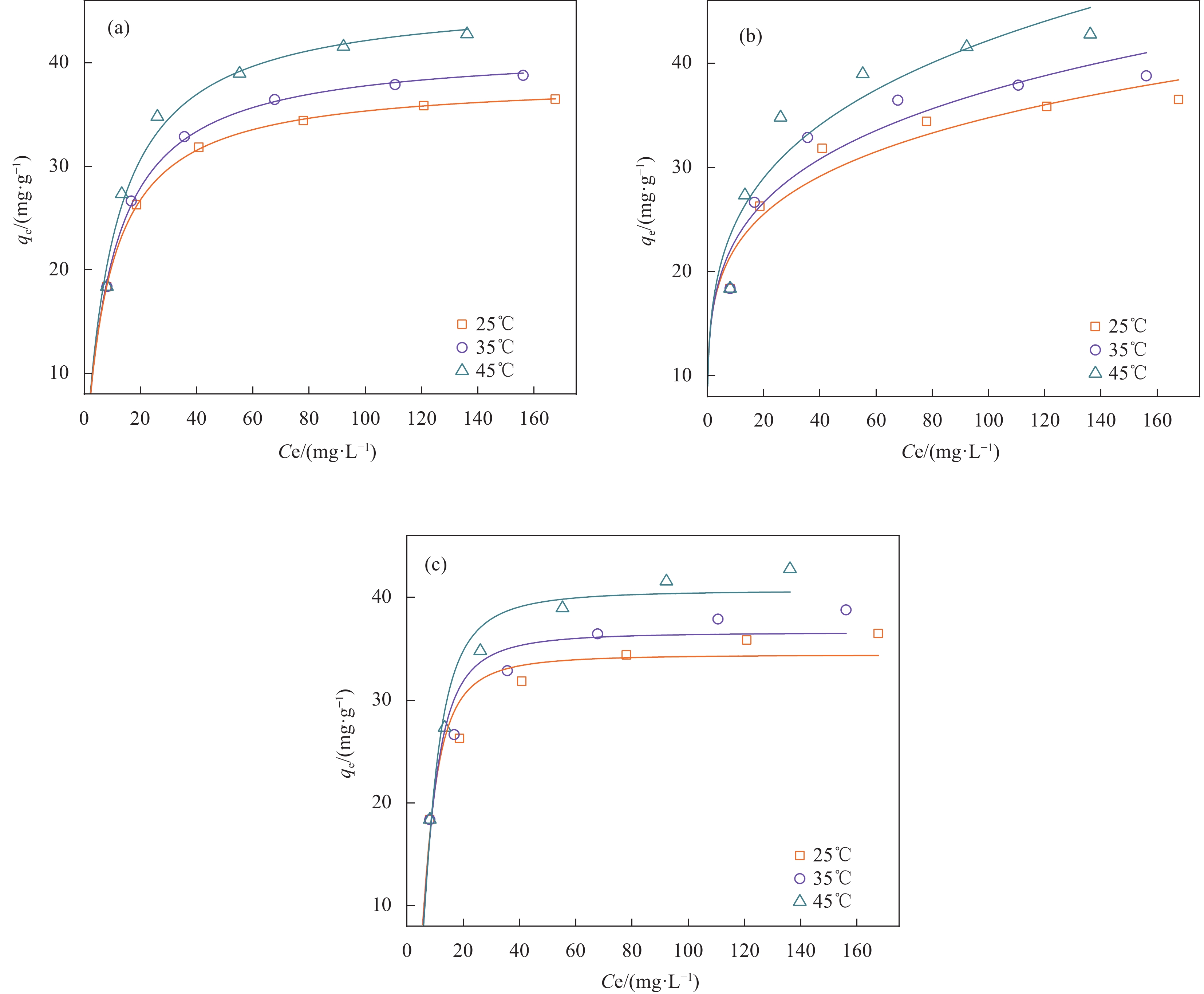
吸附等温线模型可用于阐释MBC与TC初始浓度之间的关系以及TC在吸附过程中的行为[40]。利用Langmuir、Fruendlich和Dubinin-Radushkevich等温线模型对实验数据进行非线性拟合,结果如图9所示,拟合参数列于表2。MBC对TC的平衡吸附量随着初始浓度的增加而增加,可见,溶液中TC含量的增加会增强其在MBC表面位点的结合作用。25℃、35℃、45℃时,MBC对TC的最大平衡吸附量分别为36.49、38.78、42.76 mg·g−1。
表 2 MBC吸附TC的等温线参数Table 2. Isotherm parameters of TC adsorption onto MBC at different temperaturesAdsorption isotherm Parameters 25℃ 35℃ 45℃ Values R2 Values R2 Values R2 Langmuir qm/(mg·g−1) 38.42 0.9999 41.42 0.9994 46.49 0.9933 KL/(L·mg−1) 0.1148 0.1036 0.0967 RL 0.5183 0.5438 0.5609 Freundlich n 5.194 0.9743 4.760 0.9683 4.286 0.9548 KF/[mg·g−1/(L·mg−1)n] 14.33 14.19 14.40 Dubinin-Radushkevich qm/(mg·g−1) 34.42 0.9721 36.58 0.9727 40.67 0.9853 KDR/(mol2·kJ−2) 8.455 8.857 9.328 E/(kJ·mol−1) 0.2432 0.2376 0.2315 Notes: Langmuir Model: qm: Theoretical maximum adsorption capacity, KL: Langmuir constant, RL: Langmuir separation factor; Freundlich Model: n: Freundlich intensity parameter, KF: Freundlich constant; Dubinin-Radushkevich Model: qm: Theoretical maximum adsorption capacity, KDR: Dubinin-Radushkevich constant, E: Mean free energy of adsorption. 由表2可知,Langmuir等温线模型(R2 =
0.9933 ~0.9999 )能更好地描述MBC对TC的吸附行为。Langmuir模型认为TC在MBC表面的吸附是单层吸附。理论上,MBC对TC的单层吸附最大量为38.42 mg·g−1 (25℃)、41.42 mg·g−1 (35℃)和46.49 mg·g−1 (45℃),体现了MBC对TC良好的吸附潜力。Langmuir吸附因子RL可用于评估吸附过程的可行性,根据RL值大小可将吸附过程分为不利吸附(RL > 1)、线性吸附(RL = 1)、有利吸附(0 < RL < 1)和不可逆吸附(RL = 0)[49]。经计算,不同温度下的RL值分别为:0.5183 ~0.04942 (25℃)、0.5438 ~0.05824 (35℃)和0.5609 ~0.07058 (45℃),可见,本文设置的实验条件对MBC吸附TC是有利的。Dubinin-Radushkevich模型是一种经验性模型,它认为吸附剂表面是不均匀的,表面能呈高斯分布,利用平均表面能的大小可以经验性判断吸附机制[48]。Dubinin-Radushkevich等温线模型拟合的R2 =
0.9721 ~0.9853 ,因此该模型亦能较好地描述MBC对TC的吸附机制。经计算,不同温度下MBC对TC的平均吸附自由能为0.23~0.24 kJ·mol−1,表明吸附过程主要是物理作用[45]。2.2.5 热力学分析
利用热力学参数ΔG、ΔH和ΔS可确定吸附过程的自发性质,其中ΔH和ΔS通过范特霍夫曲线的斜率和截距算得,如图10所示,计算结果列于表3。由表3可知,所有温度下的ΔG均为负值,且温度越高,ΔG越负,表明实验条件下MBC对TC的吸附是自发可行的[50],升高温度有利于吸附,与等温线实验结果相符。ΔG处于−20~0 kJ·mol−1范围,表明该吸附过程主要是物理作用[51]。
表 3 MBC吸附TC的热力学参数Table 3. Thermodynamic parameters of MBC adsorbed TCTemperature/K Kd ΔG/
(kJ·mol−1)ΔH/
(kJ·mol−1)ΔS
(J·K−1·mol−1)298 1.408 −0.85 14.65 51.80 308 1.589 −1.19 318 2.046 −1.89 Notes: Kd: Equilibrium constant of adsorption, ΔG: Gibbs free energy change, ΔH: Enthalpy change, ΔS: Entropy change ΔH值为14.65 kJ·mol−1,表明吸附过程是吸热的[52]。因此,TC分子在与MBC表面结合时需要吸收热量,升高温度有利于TC与吸附剂之间的结合,从而促进吸附过程。ΔS值为51.80 J·mol−1·K−1,为正值,说明吸附过程导致固液界面随机性增加,吸附TC的自由度增强。
2.2.6 MBC的重复利用
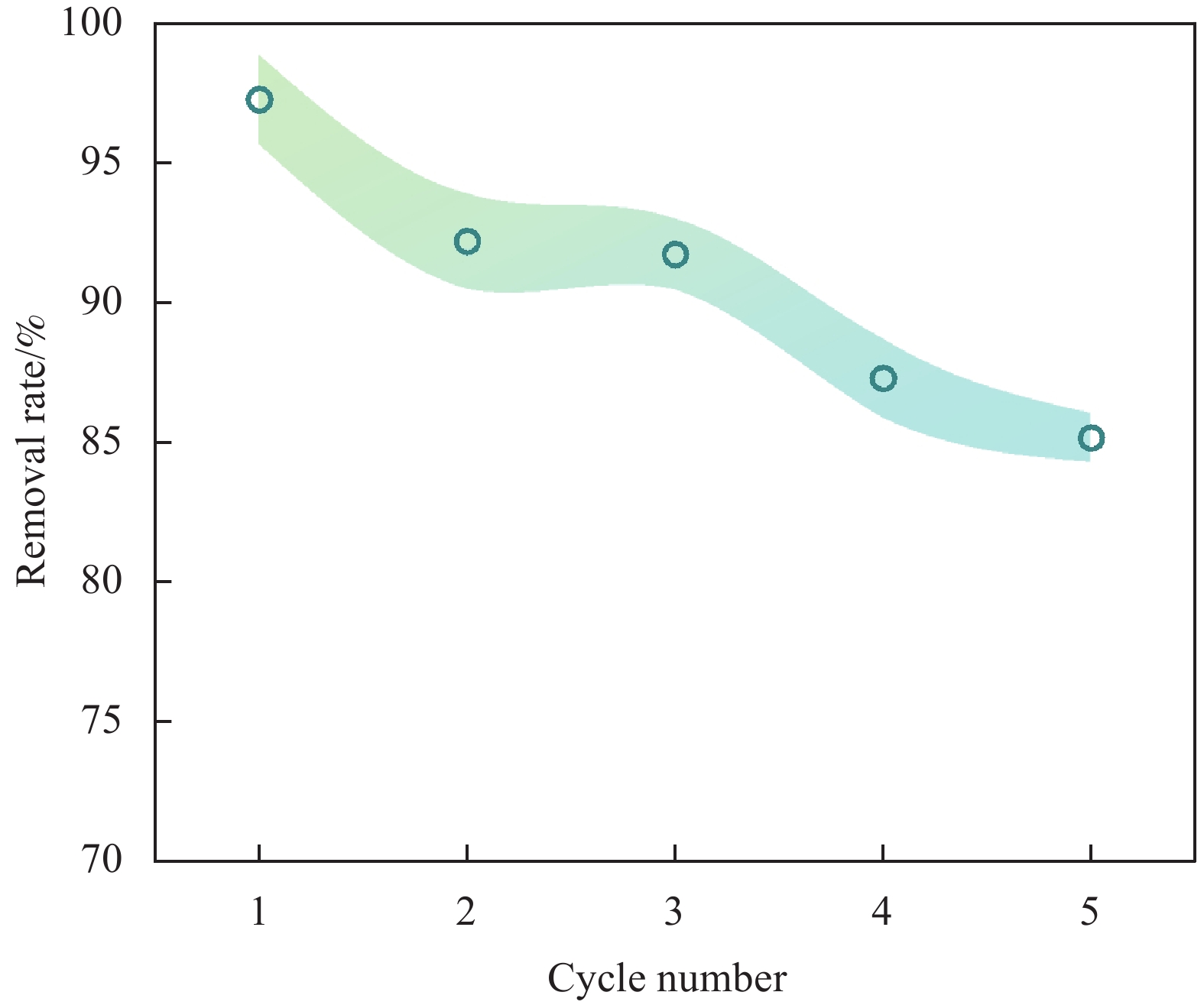
在35℃、120 r/min下,用CH3OH和0.1 mol·L−1 HCl (v∶v = 9∶1)的混合溶液解吸TC[53]。CH3OH作为有机溶剂,可以有效溶解吸附剂表面的有机污染物如四环素分子;与此同时,HCl作为强酸,能够溶解无机物,并破坏吸附剂表面的弱化学键(如离子键和氢键),从而去除微小颗粒[54,55]。这两种溶液共同作用,能够全面清理和扩展吸附剂的孔隙结构,提高解吸效率,以评估MBC的回收效果。解吸时间为12 h。解吸后,用纯净水洗涤MBC,并于70℃下干燥至恒重,即可回收MBC。经过5次吸附/解吸循环, MBC对TC的去除率维持在85.16%,如图11所示,这是因为在CH3OH和HCl的再生过程中会形成更多的孔隙结构来维持吸附能力[56]。可见,即使经过多次重复使用,MBC吸附TC的性能依然较为理想。因此,MBC复合材料是一种有效的、可重复使用的TC吸附材料,并展现出较好的实际应用潜力。
3. 吸附机制分析
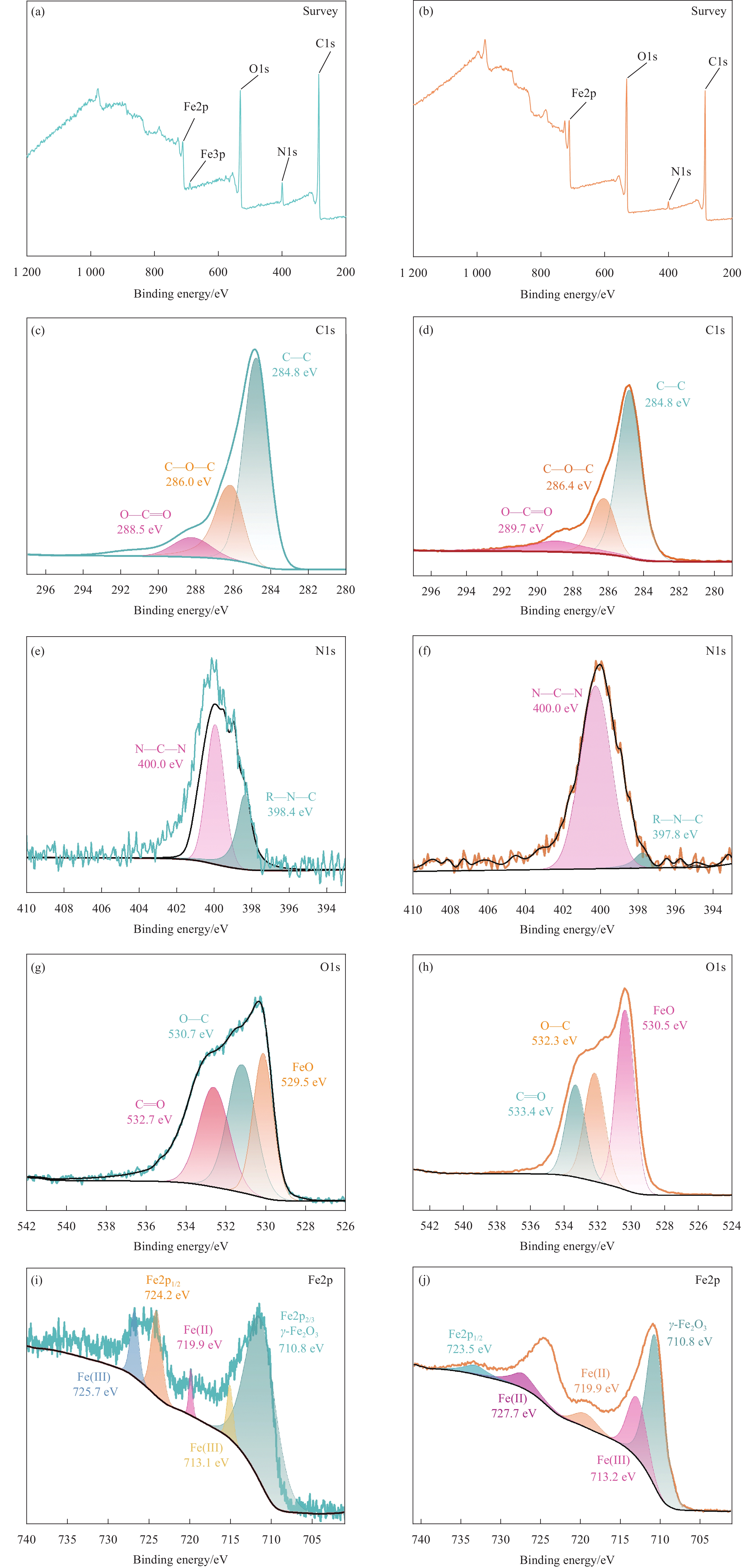
MBC可以通过物理作用和化学作用两种方式吸附TC。高比表面积表明MBC具有丰富的活性位点,因此能够有效吸附TC。孔体积的增加可以进一步增强物理吸附的可能性。而MBC表面的负电位则有利于促进化学吸附。为了进一步阐释MBC对TC的吸附机制,对吸附前后的MBC进行XPS分析,结果如图12所示。
C1s能谱显示,MBC在吸附前后,表面C1s的化学状态发生了变化。吸附前的峰主要在285 eV左右,代表C—C和C—H键。吸附后,峰的强度明显降低,表明TC分子的芳香环结构与MBC表面的碳基芳香结构发生了π-π相互作用[57]。O1s能谱中,吸附前MBC表面的羧基(C=O)和羟基(C—OH)峰位于531 eV和533 eV。吸附后,羧基的峰强度显著增加,表明TC分子中的羧基和酚羟基与MBC表面的含氧官能团发生了氢键或配位键作用[39,58]。N1s能谱进一步揭示了MBC和TC之间的化学相互作用。吸附前,MBC表面几乎没有检测到氮的存在。吸附后,400 eV处的氮峰明显增强,显示出TC分子中的氨基或其他含氮基团通过化学键与MBC结合,形成稳定的络合物[59]。Fe2p能谱显示,MBC中的铁在吸附TC前后也发生了显著变化。吸附后,Fe的特征峰强度增强,峰位置也发生了轻微变化,表明Fe与TC分子中的含氧或含氮基团形成了配位络合[60]。在XPS全谱中,可以清楚地观察到MBC在吸附TC前后,表面化学组成的显著变化。这些变化表明TC分子中N、O通过与MBC表面的含C、O和Fe结构进行复杂的化学相互作用[61],包括氢键作用、配位键形成和π-π相互作用,从而实现高效吸附[62,63]。
结合SEM,吸附前MBC表面结构相对平整,而吸附后,MBC表面覆盖了一层颗粒状物质,验证了TC成功被吸附在MBC表面。FT-IR光谱的变化也表明,吸附前后MBC表面的官能团发生了显著变化,支持了XPS关于化学结合的结论。
此外,热力学分析表明,MBC吸附TC是一个自发的吸热过程(ΔG负值和ΔH正值),且是熵增的过程(ΔS正值)。这表明吸附过程不仅在热力学上是有利的,还显示出MBC对TC的吸附是一个复杂的多步化学反应过程。pH效应研究进一步说明了MBC在不同pH条件下通过静电吸引来实现对TC的吸附。
综上所述,MBC吸附TC的机制主要涉及π-π相互作用、氢键和配位键形成、表面络合和静电相互作用等化学吸附机制,同时存在物理吸附和孔隙填充。这些相互作用受化学结合和物理吸附共同影响,使得MBC对TC具有高效的吸附性能和良好的应用前景。这些分析不仅揭示了MBC吸附TC的内在机制,还为MBC的应用和进一步的性能优化提供了重要的理论依据。
4. 结 论
(1) 本研究通过以湛江本地特色农业废弃物——椰壳为原料,采用FeCl3和FeSO4作为铁源,利用NH3·H2O调节pH,并通过浸渍、共沉淀和水热合成法制得了磁性椰壳生物炭(MBC),该材料表现出优异的孔隙结构和大的比表面积。
(2) 吸附实验结果表明,MBC的吸附过程符合Langmuir等温线和伪二阶动力学模型,且热力学分析证实吸附过程为自发的吸热反应。MBC对四环素(TC)的优异吸附性能主要归因于多种作用机制的协同效应,包括液膜扩散、孔隙内扩散、表面络合、氢键和π-π堆积作用。MBC在中性至微酸性条件下表现出最佳的吸附效果,高浓度的二价金属离子如Ca2+和Mg2+会显著降低吸附效能,而Na+的影响则较小。
(3) 在稳定性与可重复使用性方面,MBC在5次吸附-解吸循环后依然保持良好的稳定性和可重复使用性。本研究不仅为铁基生物炭在水中抗生素污染物的吸附提供了重要的理论基础和实践参考,还为废弃椰壳的资源化利用提供了一种可行的方法。
-
图 4 N2吸附-脱附曲线:(a1) BC;(b1) 吸附TC前的MBC;(c1) 吸附TC后的MBC;(d1) 吸附TC再生后的MBC与孔径分布图:(a2) BC;(b2) 吸附TC前的MBC;(c2) 吸附TC后的MBC;(d2) 吸附TC再生后的MBC
Figure 4. N2 adsorption-desorption curves: (a1) BC; (b1) MBC before adsorption of TC; (c1) MBC after adsorption of TC; (d1) MBC after regeneration. Pore size distribution: (a2) BC; (b2) MBC before adsorption of TC; (c2) MBC after adsorption of TC; (d2) MBC after TC regeneration.
表 1 MBC吸附TC的动力学参数
Table 1 Kinetic parameters of TC adsorption onto MBC
Adsorption kinetics Parameters 150/(mg·L−1) 200/(mg·L−1) 300/(mg·L−1) Values R2 Values R2 Values R2 Experimental qe/(mg·g−1) 27.3 — 34.8 — 43.0 — PFO model k1/(min−1) 0.0109 0.981 0.00645 0.972 0.00655 0.947 qe/(mg·g−1) 26.3 33.0 40.8 PSO model k2/(g·mg−1·min−1) 7.67×10−4 0.998 2.74×10−4 0.994 2.31×10−4 0.981 qe/(mg·g−1) 27.7 36.0 44.3 Elovich model α/ (g·mg−1·min−2) 61.7 0.992 2.12 0.999 2.87 0.982 β/ (mg·g−1·min−1) 0.383 0.185 0.153 IPD model ki1/(mg−1·g−1min−0.5) 0.437 0.985 0.781 0.982 0.566 0.999 C1/(mg·g−1) 15.8 12.4 21.1 ki2/(mg−1·g−1min−0.5) 0.169 0.978 0.382 0.993 0.559 0.986 C2/(mg·g−1) 20.8 19.9 21.6 Notes: qe: Amount of TC adsorbate at equilibrium k1: Rate constant of the pseudo-first-order adsorption
k2: Rate constant of the pseudo-second-order adsorption α: Initial adsorption rate of the Elovich model
β: Desorption constant of the Elovich model ki1: Intraparticle diffusion rate constant at the first stage
C1: Boundary layer thickness in the intraparticle diffusion model at the first stage
ki2: Intraparticle diffusion rate constant at the second stage R2: Correlation coefficient
C2: Boundary layer thickness in the intraparticle diffusion model at the second stage表 2 MBC吸附TC的等温线参数
Table 2 Isotherm parameters of TC adsorption onto MBC at different temperatures
Adsorption isotherm Parameters 25℃ 35℃ 45℃ Values R2 Values R2 Values R2 Langmuir qm/(mg·g−1) 38.42 0.9999 41.42 0.9994 46.49 0.9933 KL/(L·mg−1) 0.1148 0.1036 0.0967 RL 0.5183 0.5438 0.5609 Freundlich n 5.194 0.9743 4.760 0.9683 4.286 0.9548 KF/[mg·g−1/(L·mg−1)n] 14.33 14.19 14.40 Dubinin-Radushkevich qm/(mg·g−1) 34.42 0.9721 36.58 0.9727 40.67 0.9853 KDR/(mol2·kJ−2) 8.455 8.857 9.328 E/(kJ·mol−1) 0.2432 0.2376 0.2315 Notes: Langmuir Model: qm: Theoretical maximum adsorption capacity, KL: Langmuir constant, RL: Langmuir separation factor; Freundlich Model: n: Freundlich intensity parameter, KF: Freundlich constant; Dubinin-Radushkevich Model: qm: Theoretical maximum adsorption capacity, KDR: Dubinin-Radushkevich constant, E: Mean free energy of adsorption. 表 3 MBC吸附TC的热力学参数
Table 3 Thermodynamic parameters of MBC adsorbed TC
Temperature/K Kd ΔG/
(kJ·mol−1)ΔH/
(kJ·mol−1)ΔS
(J·K−1·mol−1)298 1.408 −0.85 14.65 51.80 308 1.589 −1.19 318 2.046 −1.89 Notes: Kd: Equilibrium constant of adsorption, ΔG: Gibbs free energy change, ΔH: Enthalpy change, ΔS: Entropy change -
[1] MOUSSAVI G, ALAHABADI A, YAGHMAEIAN K, et al. Preparation, characterization and adsorption potential of the NHCl-induced activated carbon for the removal of amoxicillin antibiotic from water[J]. Chemical Engineering Journal, 2013, 217: 119-128. DOI: 10.1016/j.cej.2012.11.069
[2] SECONDES M F N, NADDEO V, BELGIORNO V, et al. Removal of emerging contaminants by simultaneous application of membrane ultrafiltration, activated carbon adsorption, and ultrasound irradiation[J]. Journal of Hazardous Materials, 2014, 264: 342-349. DOI: 10.1016/j.jhazmat.2013.11.039
[3] SAMARGHANDI M R, AL-MUSAWI T J, MOHSENI-BANDPI A, et al. Adsorption of cephalexin from aqueous solution using natural zeolite and zeolite coated with manganese oxide nanoparticles[J]. Journal of Molecular Liquids, 2015, 211: 431-441. DOI: 10.1016/j.molliq.2015.06.067
[4] MIAO J, WANG F, CHEN Y, et al. The adsorption performance of tetracyclines on magnetic graphene oxide: A novel antibiotics absorbent[J]. Applied Surface Science, 2019, 475: 549-558. DOI: 10.1016/j.apsusc.2019.01.036
[5] IMWENE K O, NGUMBA E, KAIRIGO P K. Emerging technologies for enhanced removal of residual antibiotics from source-separated urine and wastewaters: A review[J]. Journal of Environmental Management, 2022, 322: 116065. DOI: 10.1016/j.jenvman.2022.116065
[6] KRASUCKA P, PAN B, SIK Ok Y, et al. Engineered biochar – A sustainable solution for the removal of antibiotics from water[J]. Chemical Engineering Journal, 2021, 405: 126926. DOI: 10.1016/j.cej.2020.126926
[7] Syranidou E, Kalogerakis N. Interaction of microplastics, antibiotics and antibiotic resistant genes within WWTPs[J]. Science of The Total Environment, 2022, 804: 150141. DOI: 10.1016/j.scitotenv.2021.150141
[8] XIONG W, ZENG G, YANG Z, et al. Adsorption of tetracycline antibiotics from aqueous solutions on nanocomposite multi-walled carbon nanotube functionalized MIL-53(Fe) as new adsorbent[J]. Science of The Total Environment, 2018, 627: 235-244. DOI: 10.1016/j.scitotenv.2018.01.249
[9] YANG H, YU H, WANG J, et al. Magnetic porous biochar as a renewable and highly effective adsorbent for the removal of tetracycline hydrochloride in water[J]. Environmental Science and Pollution Research, 2021, 28(43): 61513-61525. DOI: 10.1007/s11356-021-15124-6
[10] NGOC TRI N, HO D Q, TRAN GIA BAO N, et al. The adsorption of tetracycline, ciprofloxacin on reduced graphene oxide surfaces: Role of intermolecular interaction[J]. Chemical Physics, 2024, 579: 112207. DOI: 10.1016/j.chemphys.2024.112207
[11] WEI J, LIU Y, LI J, et al. Adsorption and co-adsorption of tetracycline and doxycycline by one-step synthesized iron loaded sludge biochar[J]. Chemosphere, 2019, 236: 124254. DOI: 10.1016/j.chemosphere.2019.06.224
[12] GAO F, XU Z, DAI Y. Removal of tetracycline from wastewater using magnetic biochar: A comparative study of performance based on the preparation method[J]. Environmental Technology & Innovation, 2021, 24: 101916.
[13] ZHAO W, CUI Y, SUN X, et al. Corn stover biochar increased edible safety of spinach by reducing the migration of mercury from soil to spinach[J]. Science of The Total Environment, 2021, 758: 143883. DOI: 10.1016/j.scitotenv.2020.143883
[14] WANG Y, JIANG B, WANG L, et al. Hierarchically structured two-dimensional magnetic microporous biochar derived from hazelnut shell toward effective removal of p-arsanilic acid[J]. Applied Surface Science, 2021, 540: 148372. DOI: 10.1016/j.apsusc.2020.148372
[15] LIU L, FANG W, YUAN M, et al. Metolachlor-adsorption on the walnut shell biochar modified by the fulvic acid and citric acid in water[J]. Journal of Environmental Chemical Engineering, 2021, 9(5): 106238. DOI: 10.1016/j.jece.2021.106238
[16] PANDEY D, SINGH S, DUTTA K, et al. Biobased Nanotechnology for Green Applications [M]. Cham: Springer Nature Switzerland AG, 2021: 619-639.
[17] YAO Y, GAO B, INYANG M, et al. Biochar derived from anaerobically digested sugar beet tailings: Characterization and phosphate removal potential[J]. Bioresource Technology, 2011, 102(10): 6273-6278. DOI: 10.1016/j.biortech.2011.03.006
[18] BOMBUWALA DEWAGE N, LIYANAGE A S, SMITH Q, et al. Fast aniline and nitrobenzene remediation from water on magnetized and nonmagnetized Douglas fir biochar[J]. Chemosphere, 2019, 225: 943-953. DOI: 10.1016/j.chemosphere.2019.03.050
[19] ZAHEDIFAR M, SEYEDI N, SHAFIEI S, et al. Surface-modified magnetic biochar: Highly efficient adsorbents for removal of Pb(ΙΙ) and Cd(ΙΙ)[J]. Materials Chemistry and Physics, 2021, 271: 124860 . DOI: 10.1016/j.matchemphys.2021.124860
[20] ZHOU J, HE Y, HUANG L, et al. Preparation of magnetic biochar from macadamia nutshell pretreated by FeCl3-assisted mechanochemical activation for adsorption of heavy metals FeCl3[J]. Journal of Environmental Chemical Engineering, 2024, 12(4): 113122. DOI: 10.1016/j.jece.2024.113122
[21] JIAO Y, WANG S, SUN B, et al. Adsorption efficiency and in-situ catalytic thermal degradation behaviour of microplastics from water over Fe-modified lignin-based magnetic biochar[J]. Separation and Purification Technology, 2025, 353: 128468. DOI: 10.1016/j.seppur.2024.128468
[22] HANG J, GUO Z, ZHONG C, et al. A super magnetic porous biochar manufactured by potassium ferrate-accelerated hydrothermal carbonization for removal of tetracycline[J]. Journal of Cleaner Production, 2024, 435: 140470. DOI: 10.1016/j.jclepro.2023.140470
[23] MEI Y, XU J, ZHANG Y, et al. Effect of Fe-N modification on the properties of biochars and their adsorption behavior on tetracycline removal from aqueous solution[J]. Bioresource Technology, 2021, 325: 124732. DOI: 10.1016/j.biortech.2021.124732
[24] MELLITI E, TOUATI K, VAN DER BRUGGEN B, et al. Effect of Fe2+ ions on gypsum precipitation during bulk crystallization of reverse osmosis concentrates[J]. Chemosphere, 2021, 263: 127866. DOI: 10.1016/j.chemosphere.2020.127866
[25] HAN J, SONG Y, LI H, et al. Preparation of novel magnetic porous biochar and its adsorption mechanism on cerium in rare earth wastewater[J]. Ceramics International, 2023, 49(6): 9901-9908. DOI: 10.1016/j.ceramint.2022.11.165
[26] HANG J, GUO Z, ZHONG C, et al. A super magnetic porous biochar manufactured by potassium ferrate-accelerated hydrothermal carbonization for removal of tetracycline[J]. Journal of Cleaner Production, 2024, 435: 140470. DOI: 10.1016/j.jclepro.2023.140470
[27] YANG Y, YIN S, YANG D, et al. Carboxyl Fe3O4 magnetic nanoparticle-based SPE and HPLC method for the determination of six tetracyclines in water[J]. Analytical and Bioanalytical Chemistry, 2019, 411(2): 507-515. DOI: 10.1007/s00216-018-1475-y
[28] JAAFARZADEH N, KAKAVANDI B, TAKDASTAN A, et al. Powder activated carbon/Fe3O4 hybrid composite as a highly efficient heterogeneous catalyst for Fenton oxidation of tetracycline: degradation mechanism and kinetic[J]. RSC Advances, 2015, 5(103): 84718-84728. DOI: 10.1039/C5RA17953J
[29] HASANPOUR A, NIYAIFAR M, ASAN M, et al. Synthesis and characterization of FeO and ZnO nanocomposites by the sol-gel method[J]. Journal of Magnetism and Magnetic Materials, 2013, 334: 41-44. DOI: 10.1016/j.jmmm.2013.01.016
[30] ZHAO H, LANG Y. Adsorption behaviors and mechanisms of florfenicol by magnetic functionalized biochar and reed biochar[J]. Journal of the Taiwan Institute of Chemical Engineers, 2018, 88: 152-160. DOI: 10.1016/j.jtice.2018.03.049
[31] MIMMO T, PANZACCHI P, BARATIERI M, et al. Effect of pyrolysis temperature on miscanthus (Miscanthus × giganteus) biochar physical, chemical and functional properties[J]. Biomass and Bioenergy, 2014, 62: 149-157. DOI: 10.1016/j.biombioe.2014.01.004
[32] WANG M, ZHAO Z, ZHANG Y. Magnetite-contained biochar derived from fenton sludge modulated electron transfer of microorganisms in anaerobic digestion[J]. Journal of Hazardous Materials, 2021, 403: 123972. DOI: 10.1016/j.jhazmat.2020.123972
[33] AYIANIA M, SMITH M, HENSLEY A J R, et al. Deconvoluting the XPS spectra for nitrogen-doped chars: An analysis from first principles[J]. Carbon, 2020, 162: 528-544. DOI: 10.1016/j.carbon.2020.02.065
[34] AHMED J, FAISAL M, JALALAH M, et al. An efficient amperometric catechol sensor based on novel polypyrrole-carbon black doped α-FeO nanocomposite[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2021, 619: 126469. DOI: 10.1016/j.colsurfa.2021.126469
[35] MA D, YANG Y, LIU B, et al. Zero-valent iron and biochar composite with high specific surface area via K2FeO4 fabrication enhances sulfadiazine removal by persulfate activation[J]. Chemical Engineering Journal, 2021, 408: 127992. DOI: 10.1016/j.cej.2020.127992
[36] WANG Q, ZHANG Z, XU G, et al. Magnetic porous biochar with nanostructure surface derived from penicillin fermentation dregs pyrolysis with KFeO activation: Characterization and application in penicillin adsorption[J]. Bioresource Technology, 2021, 327: 124818. DOI: 10.1016/j.biortech.2021.124818
[37] PAL D, MAITI S K. Abatement of cadmium (Cd) contamination in sediment using tea waste biochar through meso-microcosm study[J]. Journal of Cleaner Production, 2019, 212: 986-996. DOI: 10.1016/j.jclepro.2018.12.087
[38] LI Z T, LIN B, JIANG L W, et al. Effective preparation of magnetic superhydrophobic FeO/PU sponge for oil-water separation[J]. Applied Surface Science, 2018, 427: 56-64. DOI: 10.1016/j.apsusc.2017.08.183
[39] AFZAL M Z, SUN X F, LIU J, et al. Enhancement of ciprofloxacin sorption on chitosan/biochar hydrogel beads[J]. Science of The Total Environment, 2018, 639: 560-569. DOI: 10.1016/j.scitotenv.2018.05.129
[40] WANG Z, SHEN D, SHEN F, et al. Phosphate adsorption on lanthanum loaded biochar[J]. Chemosphere, 2016, 150: 1-7. DOI: 10.1016/j.chemosphere.2016.02.004
[41] TANG L, YU J, PANG Y, et al. Sustainable efficient adsorbent: Alkali-acid modified magnetic biochar derived from sewage sludge for aqueous organic contaminant removal[J]. Chemical Engineering Journal, 2018, 336: 160-169. DOI: 10.1016/j.cej.2017.11.048
[42] LIU S, XU W hua, LIU Y guo, et al. Facile synthesis of Cu(II) impregnated biochar with enhanced adsorption activity for the removal of doxycycline hydrochloride from water[J]. Science of The Total Environment, 2017, 592: 546-553. DOI: 10.1016/j.scitotenv.2017.03.087
[43] MARTINS A C, PEZOTI O, CAZETTA A L, et al. Removal of tetracycline by NaOH-activated carbon produced from macadamia nut shells: Kinetic and equilibrium studies[J]. Chemical Engineering Journal, 2015, 260: 291-299. DOI: 10.1016/j.cej.2014.09.017
[44] GAO Y, YUE Q, XU S, et al. Preparation and evaluation of adsorptive properties of micro-mesoporous activated carbon via sodium aluminate activation[J]. Chemical Engineering Journal, 2015, 274: 76-83. DOI: 10.1016/j.cej.2015.03.055
[45] PEZOTI O, CAZETTA A L, BEDIN K C, et al. NaOH-activated carbon of high surface area produced from guava seeds as a high-efficiency adsorbent for amoxicillin removal: Kinetic, isotherm and thermodynamic studies[J]. Chemical Engineering Journal, 2016, 288: 778-788. DOI: 10.1016/j.cej.2015.12.042
[46] SEN GUPTA S, BHATTACHARYYA K G. Kinetics of adsorption of metal ions on inorganic materials: A review[J]. Advances in Colloid and Interface Science, 2011, 162(1): 39-58.
[47] ZHOU L, ZHANG G, ZENG Y, et al. Endogenous iron-enriched biochar derived from steel mill wastewater sludge for tetracycline removal: Heavy metals stabilization, adsorption performance and mechanism[J]. Chemosphere, 2024, 359: 142263. DOI: 10.1016/j.chemosphere.2024.142263
[48] ALHUJAILY A, MAO Y, ZHANG J, et al. Facile fabrication of Mg-Fe-biochar adsorbent derived from spent mushroom waste for phosphate removal[J]. Journal of the Taiwan Institute of Chemical Engineers, 2020, 117: 75-85. DOI: 10.1016/j.jtice.2020.11.034
[49] PATHAK P D, MANDAVGANE S A. Preparation and characterization of raw and carbon from banana peel by microwave activation: Application in citric acid adsorption[J]. Journal of Environmental Chemical Engineering, 2015, 3(4): 2435-2447. DOI: 10.1016/j.jece.2015.08.023
[50] CUI Z, XU G, ORMECI B, et al. A novel magnetic sludge biochar was prepared by making full use of internal iron in sludge combining KMnO4-NaOH modification to enhance the adsorption of Pb (Ⅱ), Cu (Ⅱ) and Cd(Ⅱ)[J]. Environmental Research, 2023, 236: 116470. DOI: 10.1016/j.envres.2023.116470
[51] SRIVASTAVA V, SHARMA Y C, SILLANPÄÄ M. Application of nano-magnesso ferrite (n-MgFeO) for the removal of Co ions from synthetic wastewater: Kinetic, equilibrium and thermodynamic studies[J]. Applied Surface Science, 2015, 338: 42-54. DOI: 10.1016/j.apsusc.2015.02.072
[52] LIU X J, LI M F, MA J F, et al. Chitosan crosslinked composite based on corncob lignin biochar to adsorb methylene blue: Kinetics, isotherm, and thermodynamics[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2022, 642: 128621. DOI: 10.1016/j.colsurfa.2022.128621
[53] ALIYU M, ABDULLAH A H, TAHIR M I B. Adsorption tetracycline from aqueous solution using a novel polymeric adsorbent derived from the rubber waste[J]. Journal of the Taiwan Institute of Chemical Engineers, 2022, 136: 104333. DOI: 10.1016/j.jtice.2022.104333
[54] WANG S, CHEN Y, GE S, et al. Adsorption characterization of tetracycline antibiotics on alkali-functionalized rice husk biochar and its evaluation on phytotoxicity to seed germination[J]. Environmental Science and Pollution Research, 2023, 30(58): 122420-122436. DOI: 10.1007/s11356-023-30900-2
[55] WANG K, YAO R, ZHANG D, et al. Tetracycline Adsorption Performance and Mechanism Using Calcium Hydroxide-Modified Biochars[J]. Toxics, 2023, 11(10): 841. DOI: 10.3390/toxics11100841
[56] JANG H M, KAN E. A novel hay-derived biochar for removal of tetracyclines in water[J]. Bioresource Technology, 2019, 274: 162-172. DOI: 10.1016/j.biortech.2018.11.081
[57] INYANG M, DICKENSON E. The potential role of biochar in the removal of organic and microbial contaminants from potable and reuse water: A review[J]. Chemosphere, 2015, 134: 232-240. DOI: 10.1016/j.chemosphere.2015.03.072
[58] SAIKIA N, DEKA R C. Density functional study on noncovalent functionalization of pyrazinamide chemotherapeutic with graphene and its prototypes[J]. New Journal of Chemistry, 2014, 38(3): 1116-1128. DOI: 10.1039/c3nj00735a
[59] MAO H, WANG S, LIN J Y, et al. Modification of a magnetic carbon composite for ciprofloxacin adsorption[J]. Journal of Environmental Sciences, 2016, 49: 179-188. DOI: 10.1016/j.jes.2016.05.048
[60] MA D, YANG Y, LIU B, et al. Zero-valent iron and biochar composite with high specific surface area via K2FeO4 fabrication enhances sulfadiazine removal by persulfate activation[J]. Chemical Engineering Journal, 2021, 408: 127992. DOI: 10.1016/j.cej.2020.127992
[61] YANG X, LUO K, PI Z, et al. Insight to the mechanism of tetracycline removal by ball-milled nanocomposite CeO/FeO/Biochar: Overlooked degradation behavior[J]. Separation and Purification Technology, 2023, 307: 122703. DOI: 10.1016/j.seppur.2022.122703
[62] MOHAN D, SARSWAT A, OK Y S, et al. Organic and inorganic contaminants removal from water with biochar, a renewable, low cost and sustainable adsorbent - A critical review[J]. Bioresource Technology, 2014, 160: 191-202. DOI: 10.1016/j.biortech.2014.01.120
[63] WANG J, CHEN Z, CHEN B. Adsorption of Polycyclic Aromatic Hydrocarbons by Graphene and Graphene Oxide Nanosheets[J]. Environmental Science & Technology, 2014, 48(9): 4817-4825.
-
其他相关附件
-
本文图文摘要
点击下载
-
-
目的
抗生素类药物(如,四环素(TC))在日常生产、生活中的广泛使用,导致了其在土壤和自然水体中的长期排放,对藻类及低等生物的生存构成了威胁,并可能对生态环境带来持续性破坏。传统的生物炭吸附材料在去除抗生素过程中普遍存在着分离效率低、易造成二次污染等缺陷,为此,本文制备了一种磁性椰壳生物炭多孔材料,以实现水中四环素的高效去除及材料的重复利用。
方法以湛江特色废弃物椰壳为生物质原料,经清洗、干燥、粉碎、过筛后与FeCl和FeSO混合,通过浸渍、氨水共沉淀及水热碳化等过程,制备了一种磁性椰壳生物炭(MBC)。利用SEM、FT-IR、XRD、BET、VSM、XPS和Zeta电位仪等对MBC的物理化学结构与性质进行了表征。利用吸附实验探究了pH值、温度及共存金属离子等因素对MBC吸附TC的影响,通过吸附动力学、吸附等温线和热力学实验考察了MBC对TC的吸附行为及相关机制,通过吸附-解析循环实验考察了MBC对TC的吸附稳定性与再生能力。
结果表征结果显示,MBC材料具有丰富的孔隙,MBC的总孔体积为0.006841 cm/g,比表面积为16.3638 m/g,并附着了大量磁性FeO和-FeO混晶,不仅为吸附提供了丰富的位点,也赋予了材料磁回收能力;材料表面Zeta电位低至-20.00±0.70 mV,具有对正电位点的吸附能力。吸附实验结果显示,pH 4.0时,MBC对TC的吸附效果最佳,在24 h可达到吸附饱和,饱和吸附量为36.40 mg·g,TC去除率达93.37%。因素探究实验结果显示,MBC对TC的吸附过程受多种因素影响:ϕ溶液pH越高,MBC对TC的吸附量越低。κ二价金属离子Ca和Mg的存在会显著降低MBC对TC的吸附效率。λ升高温度有利于提高MBC对TC的吸附量。动力学实验结果显示,MBC对TC的吸附行为符合伪二阶动力学模型,表明吸附主要受化学吸附控制。吸附等温实验结果显示,MBC对TC的吸附行为符合Langmuir等温线模型,表明吸附过程以单分子层吸附为主,MBC对TC的最大单分子层吸附容量可达到46.49 mg·g (45℃)。热力学实验结果显示,MBC对TC的吸附过程是自发的吸热反应,随着温度升高,自发性更显著;吸附会导致固-液界面无序度的增加。吸附-解析循环实验结果显示,MBC在经过5次吸附-解吸循环后,仍能保持85.16%的TC去除率,表明材料具有良好的稳定性和再生能力,吸附位点的不可逆损耗可能是导致材料吸附性能下降的主要原因。
结论磁性椰壳生物炭具有丰富的孔隙结构、大的比表面积和负Zeta电位,能高效吸附水中的TC,吸附过程以单分子层的化学吸附为主,是一种自发的吸热反应。吸附过程中存在受液膜扩散、内扩散、表面络合、氢键和π-π堆积等作用。磁性椰壳生物炭是一种高效、可重复利用的TC吸附材料,有望应用于养殖尾水与医药废水的净化。
-
抗生素类药物在土壤和自然水体中的排放会对生态环境造成严重危害,危及藻类及低等生物的生存,并可能对人类和动物健康带来长期风险。抗生素在水生环境中,即使在极低浓度下,也会对人类和动物产生急性和慢性毒性,导致细菌失衡、胃肠道不适,甚至肝损伤。因此,必须采取有效措施去除水中的抗生素,以降低其对生态环境和人类健康的潜在风险。
为解决这一问题,本研究创新性地利用湛江本地特色农业废弃物椰壳为原料,采用FeCl₃和FeSO₄作为铁源,通过浸渍、共沉淀和水热合成方法制备了磁性椰壳生物炭(MBC)。这种方法不仅有效利用了本地资源,展示了生态友好的原材料选择和制备过程的创新性。MBC对TC具有显著的吸附效果,尤其是在pH 4.0时吸附效果最佳,吸附过程符合Langmuir等温线和伪二阶动力学模型,最大吸附容量在45°C时可达46.49 mg·g-1。此外,MBC在重复利用性实验中表现出优良的稳定性,经过五次吸附-解吸循环后,去除率仍稳定在85.16%。
通过本研究,不仅展示了MBC在水中TC去除方面的巨大潜力,还为农业废弃物的高值化利用提供了新的思路。这些创新性研究和亮点展示为未来水处理技术的发展和推广奠定了坚实的基础。研究表明,磁性椰壳生物炭是一种高效、可重复利用的TC吸附材料,在养殖尾水、医药废水处理等领域具有广阔的应用前景。
(a) TC的型体分布;(b) pH对MBC吸附TC的影响






 下载:
下载: