Preparation and properties of polycaprolactone-gelatin-bioglass-based asymmetrically infiltrated sandwich-structured composite membranes
-
摘要:
伤口愈合时敷料不仅需要提供止血作用,还需吸收过多的渗出物为伤口提供一个相对湿润又不过于干燥的环境。因此,本研究利用静电纺丝技术设计了一种三明治结构且具有不对称润湿性的Janus复合膜,外层为聚己内酯(PCL)纳米纤维膜,内层为明胶(Gel)和PCL混合的纳米纤维膜(PCL/Gel),而负载无机生物玻璃(BG)的纳米纤维膜(PCL/Gel-BG)作为中间层。对Janus复合膜形貌、结构以及力学、溶胀率、止血等性能进行了系统研究与探讨分析。结果表明:Janus复合膜力学性能、孔隙率等均符合医用敷料要求;此外,其溶胀率可高达990%能吸收大量渗出液,同时外层可以抗水和血液的渗透能防止伤口过度脱水;且在体外的血液吸收率、凝血指数、凝血时间测试中还表现出比传统医用纱布更优的止血能力,有望作为新型创面敷料应用于伤口愈合领域。
Abstract:Effective wound dressings must possess hemostatic functions and the ability to absorb excess exudate, maintaining a relatively moist but not overly dry environment for optimal healing. In this study, an asymmetric wettability Janus composite membrane with a sandwich structure was designed using electrospinning technology. The outer layer consists of a polycaprolactone (PCL) nanofibrous membrane, the inner layer is a composite nanofibrous membrane (PCL/Gel) containing a blend of gelatin (Gel) and PCL, while the intermediate layer is a composite nanofibrous membrane (PCL/Gel-BG) loaded with inorganic bioglass (BG). The morphology, structure, mechanics, swelling rate, hemostatic properties and other relevant properties of the Janus composite membranes were systematically studied and analyzed. The results show that the mechanical properties and porosity of the Janus composite membrane meet the requirements for medical dressings. Moreover, it displays a remarkable swelling rate of up to 990%, enabling efficient absorption of exudate. Additionally, its outer layer demonstrates excellent resistance to water and blood penetration, effectively preventing excessive wound dehydration. Furthermore, in vitro tests evaluating blood absorption rate, coagulation index, and clotting time reveal superior hemostatic ability compared to traditional medical gauze. Consequently, the Janus composite membrane holds great potential as an innovative wound dressing in the field of wound healing.
-
Keywords:
- electrospinning /
- Janus membranes /
- wound dressing /
- nanofibre /
- polycaprolactone /
- gelatin /
- bioglass.
-
随着柔性电子技术的快速发展,人们对传统硬质电子材料的需求已经不仅仅局限于传统的形状和功能。柔性可折叠、耐弯折等特性成为了人们日常生活中对电子产品的追求。因此,新型柔性电子材料的开发成为了当前材料研究领域的热点。在这方面,高分子材料具有多种优势,如柔性、质量轻、耐腐蚀等特性。其中,导电高分子融合了金属材料和聚合物材料的优异性能,具备出色的导电性和柔性,是一种含有共轭分子结构的高分子聚合物。近年来,这种材料已经广泛应用于智能纺织[1-2]领域,实现智能化的新型纺织品,从而具备温度感知、生物监测、运动追踪等功能。在先进传感器[3-4]领域,用于检测环境参数、生物信号等信息。在能源器件[5-6]领域,用于存储和转换能量的电子器件,包括柔性电池、柔性超级电容器等。在电子皮肤[7-8]领域,模拟人类皮肤的感知和反应能力,能够感知外界环境和生理信号,并做出相应的反应。
导电高分子的发现[9]打破了人们对高分子材料是绝缘体的传统认知,其主链具有高度共轭的结构,这类共轭结构使电子能够在分子内部自由运动形成高度离域的电子云[10]。典型的导电高分子包含聚乙炔(PA)、聚噻吩(PTh)、聚吡咯(PPy)等。PTh为常见的导电聚合物,其衍生材料如聚(3, 4-乙烯二氧噻吩)(PEDOT)、聚(3, 4-乙烯二氧噻吩):聚(苯乙烯磺酸盐)(PEDOT:PSS)都是目前最常见的导电高分子。其中,根据导电高分子的应用形式,可分为印刷型[11–15]、薄膜型[16–20]、纤维型导电高分子。
由于纤维在柔性、可织造等方面有着先天的优势,近年来PEDOT:PSS基纤维的研究成为了柔性电子领域的热点,湿法纺丝工艺成本低、效率高,能够制备出连续可纺的纤维,是目前制备PEDOT:PSS基纤维的主要方法。针对湿法纺丝制备PEDOT:PSS纤维,由于绝缘非晶PSS链段包裹着导电PEDOT胶体颗粒,因此近年来如何在PEDOT:PSS纤维固化成型时除去多余的PSS绝缘组分受到了关注,科研人员从分子结构角度出发,开发了众多湿法纺丝工艺,通过解离PEDOT和PSS,改善PEDOT的取向结构,促进电荷运输,实现高导电率。此外,尽可能的实现高效制备也是研究人员追求的目标。除了PEDOT:PSS纤维的制备,湿法纺制PEDOT:PSS复合纤维也成为了当下的热点,通过和其他材料复合纺制的纤维能够有效提高纤维的柔韧性和强度等其他性能。本文主要对从湿法纺丝工艺的纺丝液设计、凝固浴调控、后处理优化3个方面提升PEDOT:PSS基纤维性能的研究现状进行归纳总结,并对其未来在柔性电子等领域应用的挑战和前景进行了展望,为以后的研究提供参考。
1. PEDOT:PSS材料
1.1 PEDOT:PSS
聚(3, 4-乙烯二氧噻吩):聚(苯乙烯磺酸盐)(PEDOT:PSS),是由PEDOT和PSS两种聚合物络合形成的,属于聚噻吩的衍生物,分子结构式如图1所示,PEDOT是由乙烯二氧噻吩(EDOT)单体通过聚合反应得到的,主链结构是由EDOT单元构成的,具有共轭的π电子结构,由于π电子可以在整个共轭体系中自由运动,从而促进电子的传输和电导率的提高[10];主链共轭的噻吩结构,加上噻吩环上二氧桥的空间位阻作用使其呈现刚性不溶于部分有机溶剂。在聚合反应过程中,PEDOT处于部分氧化状态,分子链带正电荷,形成共轭π电子体系,使PEDOT分子链显电正性。PSS是由对苯乙烯磺酸发生聚合反应得到的,由于主链为可以内旋的C—C键,所以整个PSS分子链表现出优异的柔性,其中苯环对位取代的—SO3H基团具有亲水性并呈现电负性,可以与PEDOT发生静电相互作用,使PEDOT能够稳定地分散在水或者其他溶剂中,形成PEDOT:PSS分散液。其中PEDOT:PSS水分散液具有很强的环境稳定性,其电导率可以在室温下保持几年而无明显下降[21],这种稳定性使PEDOT:PSS在实际应用中更加可靠,使其在柔性电子器件领域拥有广泛的应用前景,成为了时下科研领域流行的导电高分子。
1.2 PEDOT:PSS基纤维的制备方法
目前常见的导电纤维制造方法可分为熔融纺丝[22]、溶液纺丝[23]和静电纺丝[24]等,其中溶液纺丝分为湿法纺丝[25]和干法纺丝[26]。对于PEDOT:PSS基纤维而言,由于其刚性的PEDOT分子主链,在快速溶剂挥发过程中无法形成均匀和连续的纤维,使PEDOT:PSS纤维不适用熔融纺丝和干法纺丝制备。由于PEDOT:PSS可以制备成水分散液,这使 PEDOT:PSS能够运用湿法纺丝和静电纺丝来制备连续纤维以获得具有优异综合性能的PEDOT:PSS基纤维。
1.2.1 湿法纺丝技术
湿法纺丝技术分为纺丝液、凝固浴、后处理等工艺,工艺示意图如图1所示,其中,纺丝液是通过将PEDOT:PSS悬浮液与适当的添加剂和溶剂混合,并进行搅拌和均匀分散,以获得可纺性良好的PEDOT:PSS溶液;凝固浴是湿法纺丝过程中用于凝固或固化从纺丝喷头挤出的PEDOT:PSS溶液的一种液体介质,其成分、温度和其他工艺参数的调节对纤维的性质具有显著影响;后处理是指对收集成连续纤维进行后续的技工处理,如溶液处理、拉伸、热处理等,以进一步改善其性能。以上各个工艺环节的调整均对制备成型的PEDOT:PSS基纤维性能有一定程度的影响。湿法纺丝技术可广泛应用于大规模生产连续的PEDOT:PSS基纤维,通过湿法纺丝制备的PEDOT:PSS基纤维通常呈现连续纤维的形态,其直径一般处于微米级水平。相较于其他纺丝方法,湿法纺丝技术在连续大规模制备PEDOT:PSS基纤维方面具有显著优势。近年来,科研人员对湿法纺丝工艺的研究充满了极大的兴趣,并正在进一步探索其在柔性电子器件领域的应用潜力。
1.2.2 其他方法
除了湿法纺丝,静电纺丝[27]是最常用的PEDOT:PSS基纤维制备工艺之一。需要注意的是,静电纺丝制备的纤维丝经过辊筒缠绕后,通常以纤维膜或纤维毡的形式存在,而不是单个纤维的形态。其旨在生产具有高比表面积的功能性纤维,以提升能源器件的性能效率。此外,研究人员还开发了许多新颖的工艺来提升PEDOT:PSS基纤维的性能,像水热合成法[28]、化学反应法[29]、原位聚合法[30]等特殊方法来制备PEDOT:PSS基纤维。可以预见,随着研究的不断深入,制备PEDOT:PSS基纤维的方法也将变得更加多样化。不同的制备方法会影响PEDOT:PSS基纤维的形貌、结构和性能,因此选择合适的制备方法对于个性化应用的要求至关重要。
2. 提升湿法纺丝PEDOT:PSS基纤维性能的研究
2.1 纺丝液的设计
目前,通过湿法纺丝技术制备的本征型PEDOT:PSS纤维的性能一般都较差,因此纺丝液的设计对于PEDOT:PSS基纤维最后的结构和性能有着很大的影响。在湿法纺丝过程中,一般纺丝液的设计主要从纺丝液浓度、成分选择和工艺参数等方面展开。
为了提升纤维的综合性能,研究人员通过将其他聚合物与PEDOT:PSS纺丝液进行混合共纺,得到了一系列性能良好的纤维。例如,与传统的PEDOT:PSS纺丝液相比,如图2(d)所示,Gao等[31]在PEDOT:PSS纺丝液加入聚乙烯醇(PVA)和乙二醇(EG)制备出的PVA/EG/PEDOT:PSS复合纤维,引入聚乙烯醇(PVA)和乙二醇(EG),通过对纺丝液中PVA(0wt%~30wt%)和EG(0wt%~15 wt%)含量的改变,纤维的拉伸强度和断裂伸长率在20wt%PVA和10wt%EG时达到最佳,最佳拉伸强度达到了210 MPa,且断裂伸长率也能够达到26%。此方法的缺陷是纤维导电性并未提升,这与纺丝液中加入非导电聚合物有关,此外,如图2(a)所示,Wang等[32]在PEDOT:PSS纺丝液中加入海藻酸钠(SA)凝胶作为改性剂,制备出核壳结构的SA/PEDOT:PSS复合纤维,提高了纤维的稳定性和耐久性。通过在纺丝液中添加不同比例的SA,纤维的导电性和力学性能也存在差异。但是共混得到的复合纺丝液也有局限性,最主要的缺点是复合纺丝液中的非导电组分严重降低了纤维的导电性。
为了避免导电性能的降低,研究者们尝试向PEDOT:PSS纺丝液中添加导电填料来提升纤维的导电性能,例如,Xu等[35]通过在纺丝液中添加单壁碳纳米管(SWCNT)使SWCNT/PEDOT:PSS复合纤维的电导率提高到了
2982 S/cm,如图2(b)所示,Wang等[33]通过引入芳纶纳米纤维(ANF)和过渡金属碳氮化物(MXene)使制备出MXene/PEDOT:PSS/ANF复合纤维的导电率达到了736.8 S/cm。 康鑫湲等[36]向PVA/PEDOT:PSS纺丝液中中添加了10wt%的EG,使PEDOT主特征峰红移,主链发生苯醌转变,从而导致导电性的提升。如图2(c)所示,Wen等[34]向PEDOT:PSS纺丝液中加入碲纳米线(TeNWs)悬浮液,使TeNWs均匀地分布在Te/PEDOT:PSS复合纤维上,致使纤维的电导率提高到了1438 S/cm。此外,Wu等[37]通过向纺丝液中引入二甲基亚砜(DMSO),由于DMSO的极性基团可以和PEDOT链发生偶极-偶极或者偶极-电荷作用致使复合纤维的导电率达到了4464 S/cm。但是这些策略均未展示出PEDOT:PSS优异的强导电性,并且由于导电填料的添加,破坏了PEDOT:PSS的连续结构,从而降低了纤维的力学性能。此外,常见的纺丝工艺参数也会影响纤维的成型和性能,比如对纺丝针头的大小和类型(同轴纺丝[38]、多轴纺丝[39]等),注射的速度和角度(水平、垂直)等的调节。由此可见,通过对纺丝液添加不同组分并未同时提高纤维的可拉伸性和导电性,这也是纺丝液设计方法的缺陷,所以需要配合后续工艺使纤维的综合性能达到最大化的提升。
2.2 凝固浴的调控
湿法纺丝制备PEDOT:PSS纤维的过程中,凝固浴的调控对纤维的性能起着关键性的作用。凝固浴是指纺丝液进入后在其中发生凝固和固化的介质,它可以通过调节化学成分、温度、时间等参数来控制纤维的形貌和性能。
目前,研究者们对凝固浴的调控有着极大的热情,通过凝固浴成分设计来提升导电纤维综合性能的策略越来越普遍。当今最常见的凝固浴配方为丙酮-异丙醇(At-IPA)溶液、乙醇-水(EtOH-H2O)溶液、硫酸(H2SO4)溶液、水-金属离子等体系。如图3(d)所示,Wang等[40]使用EtOH-H2O凝固浴并加入了Cu2+制备出仿生绒毛阵列的PEDOT:PSS基纤维,绒毛阵列的产生与浸入凝固浴的时间相关,使其具有良好的耐久性,并对反复的外部变形表现出优异的稳定性,为进一步的应用提供了足够的保证。Gao等[41]也利用了EtOH-H2O凝固浴体系加入Li+,与PSS进行静电络合。有趣的是,在Li+辅助下合成的PEDOT:PSS基纤维具有超过50%的断裂伸长率和优异的导电性,合成的纤维显示出良好的灵敏度和高电容,这也为可穿戴电子产品的发展提供了新的灵感。采用的EtOH-H2O凝固浴的研究人员考虑到更绿色、更环保的制备方法,为后续湿法纺丝工艺的可持续性策略开拓了新路径。Gao等[31]采用At-IPA凝固浴体系中加入Li+,提高了纤维的强度和纺丝的连续性。如图3(b)所示,Zhang等[42]采用H2SO4凝固浴体系,H2SO4可以快速去除PSS非导电成分并提高PEDOT链的取向,有利于有效的分子内和分子间的电荷传输,导致电导率高达
3828 S/cm。此外,如图3(c)所示,Gao等[43]利用水和金属离子Fe3+无溶剂凝固浴体系,少量的Fe3+促进纤维的固化,从而获得高强度和高拉伸性的PEDOT:PSS基纤维。然而,At-IPA凝固浴使PEDOT:PSS纤维快速固化成型但相分离效应过于剧烈,容易造成纤维截面异形;H2SO4凝固浴制备的纤维导电性高但存在环境污染和安全问题;EtOH-H2O凝固浴虽然环境污染小,但是往往需要添加额外的辅助成型剂才能达到固化成型的效果;水-金属离子体系凝固浴环保且能够制备出力学性能优异的纤维,但导电性有待提高。通过研究人员不断的探索,在未来将会开发出越来越多的凝固浴。表 1 后处理策略提升湿法纺丝纤维性能的方法和机制Table 1. Approaches and mechanisms of post-treatment to enhance the performance of wet-spun fibersPost-treatment strategy Common method Principles of performance enhancement Solution treatment Ethylene glycol (EG), H2SO4, Ethanol (EtOH)/H2O, N, N-dimethylformamide (DMF), Dimethyl sulfoxide (DMSO) Removal of residual polymers, organic solvents, and non-conductive components of polystyrene sulfonate (PSS) to improve fiber crystallinity and surface flatness Tensile treatment Physical tensile Align the main chains of poly(3, 4-ethylenedioxythiophene) (PEDOT) and PSS in the direction of the fiber axis, reduce defects, and improve the conductivity and thermal stability of the fibers Heat treatment Heating or insulation treatment Heating promotes the orderly arrangement of fiber molecular chains, improves the intermolecular packing density, and increases the crystallinity of fibers, changing the structure and morphology of fibers Light treatment UV or infrared light exposure Improvement of fiber conformation and fiber surface morphology to promote charge transport and carrier generation, further improving fiber conductivity and stability 2024年,如图3(a)所示,Wang等[44]开发了N, N-二甲基乙酰胺(DMAc)/H2O/甲基磺酸(MSA)凝固浴体系,复合纤维的电导率达到了
4128 S/cm。然而,仅仅在凝固浴中添加各种添加剂和辅助成型剂,还不能同时提升复合纤维的导电性和可拉伸性等综合性能,对于柔性电子器件应用的需求仍有较大差距。针对凝固浴温度的调节尚未报道,适当的凝固浴温度有利于纤维的快速固化,从而得到致密的纤维结构,也是未来研究的热点问题。如何实现导电性和可拉伸性兼具的纤维仍是研究者们探索的问题。总而言之,合理的凝固浴可以调控纤维的形貌和微观结构,提升导电性能和力学性能等方面,仍是当今PEDOT : PSS基纤维最具研究热点和潜力的问题。2.3 后处理的优化
后处理工艺是湿法纺丝PEDOT:PSS基纤维制备过程中的一个关键步骤,对纤维的最终性能有着决定性的影响。后处理也是提升纤维导电性最常见的策略之一,主要分为溶液处理、拉伸(取向处理)、热处理、光照刺激等方法。
2.3.1 溶液处理
溶液处理是最常见的手段,其中常见的溶液包括乙二醇(EG)、硫酸(H2SO4)、乙醇(EtOH)和水、N, N-二甲基甲酰胺(DMF)和二甲基亚砜(DMSO)等。采用溶液后处理优化的浓度越高,处理效果可能越明显[44],溶液后处理会诱导PEDOT的主链由苯式结构转变为醌式结构,醌式结构呈现出伸展的卷曲状结构,这种结构大大增加了分子链的局部有序性,显著降低了载流子沿PEDOT链迁移的势垒,有利于载流子的迁移,从而提高导电性(表1)。
2020年,Wen等[45]通过对纤维进行H2SO4后处理,制备出了具有高强度、大断裂应变和高韧性的PEDOT:PSS纤维,此外,纤维的导电性达到了
4029.5 S/cm,不可否认这与湿法纺丝硫酸后处理的工艺有关。如图4(a)、图4(b)所示,在H2SO4处理后,通过下式:![]() 图 4 H2SO4处理PEDOT:PSS纤维增强的机制[45]:(a) 湿法纺丝PEDOT:PSS纤维硫酸后处理工艺;(b)纤维经H2SO4处理前后的应力-应变曲线;(c) H2SO4处理前后PEDOT:PSS纤维的S2p XPS图谱;在900~
图 4 H2SO4处理PEDOT:PSS纤维增强的机制[45]:(a) 湿法纺丝PEDOT:PSS纤维硫酸后处理工艺;(b)纤维经H2SO4处理前后的应力-应变曲线;(c) H2SO4处理前后PEDOT:PSS纤维的S2p XPS图谱;在900~1700 cm−1 (d)和1380 ~1480 cm−1 (e)波数范围内H2SO4处理前后PEDOT:PSS纤维的拉曼光谱;未处理(f)和H2SO4处理(g)的PEDOT:PSS纤维的广角X射线散射(WAXS)图谱;(h) PEDOT:PSS纤维中PEDOT链堆积排列示意图Figure 4. Mechanism of performance enhancement of PEDOT:PSS fiber after H2SO4 post-treatment[45]: (a) Post-treatment of wet-spun PEDOT:PSS fibers with H2SO4; (b) Stress-strain curves of fibers before and after treatment with H2SO4; (c) S2p XPS spectra of the PEDOT:PSS fiber before and after H2SO4 treatment; Raman spectra of the PEDOT : PSS fiber before and after H2SO4 treatment in the wavenumber ranges of 900-1700 cm−1 (d) and1380 -1480 cm−1 (e); Wide-angle X-ray scattering (WAXS) patterns of untreated (f) and H2SO4-treated (g) PEDOT:PSS fibers; (h) Schematic diagram of the chain packing alignment of PEDOT in the PEDOT:PSS fiberPSS−+H2SO4→PSSH+HSO−4 (1) PEDOT:PSS中的PSS大量耗尽。对于PEDOT:PSS纤维,H2SO4处理使拉伸强度和断裂应变大大提高,表现出389.5 MPa的高拉伸强度和30.5%的大断裂应变。如图4(c)所示,通过PEDOT峰归一化,PSS的S2p XPS强度在H2SO4处理后表现出显著下降。PSS/PEDOT原子比从2.54降低到1.63,表明绝缘性PSS链的有效去除。如图4(d)所示,H2SO4处理后,纤维的拉曼谱带从
1432 cm−1移动到1426 cm−1,意味着PEDOT噻吩环从苯结构到醌结构的构象变化,醌结构的共轭长度更长,有助于电子在分子内和分子间的传输,使在PEDOT链中形成更多的载流子,从而进一步增强导电性。如图4(f)~图4(h)所示,垂直方向的散射矢量分量qz = 0.116 nm−1处的宽峰归属于随机分布PSS的无定形晕,H2SO4处理前,它在纤维中是明显的,但在处理后变得几乎不可观察,再次证实了由H2SO4处理诱导的PSS含量的显著降低。在qz = 0.175 nm−1处的峰归因于相邻PEDOT链之间的π电子堆积,经H2SO4处理后,更加光亮,形状更佳。这些都被认为是H2SO4后处理增强纤维导电性和力学性能的关键因素。此外,Xiao等[46] 通过原位聚合法制得的纺丝液进行湿法纺丝工艺,使用H2SO4后处理后,电导率达到了980 S/cm。Pan等[47]为了改善PEDOT:PSS纤维的导电性,用EG和H2SO4依次处理,除去了绝缘PSS链,纤维显示出了676.59 S/cm的电导率。由此可见,溶液处理通过去除残余的聚合物和有机溶剂,并去除PSS非导电组分来改善纤维中PEDOT分子的结晶度和表面平整度,进而提高纤维内部载流子的传输效率达到导电性能的改善。
2.3.2 拉伸(取向处理)
拉伸处理是对PEDOT:PSS基纤维进行物理拉伸,通常根据需要调控的力学性能和取向性来选择合适的拉伸范围和速度。Sarabia-Riquelme等[48]将通过IPA凝固浴的纤维在DMSO浴中进行拉伸处理,其中DMSO诱导了PEDOT链之间更强的π-π相互作用,施加的拉伸使PEDOT和PSS链的主链在纤维轴方向上对齐,这种协同效应导致在室温下的电导率约为
2000 S/cm和约15.5 GPa的杨氏模量。如图5(a)~图5(c)所示,PEDOT:PSS膜的2D WAXS图案不显示任何优选取向的迹象,表明聚合物链的随机取向。然而,在纤维的2D WAXS图案中,可以观察到指示结晶平面的择优取向的特征弧,并且在较高拉伸比下变得更加明显,如图5(d)所示,交替的PEDOT和PSS的(100)片层堆叠峰随着纤维的拉伸比提升,该峰的强度越来越高,表明拉伸在纤维形成期间诱导了更高的结晶有序度。如图5(e)所示,PEDOT链通过重叠π轨道并保持平面结构而面对面地结晶堆叠。图5(f)~图5(g)所示,薄膜样品显示出平面图案,表明没有优先取向,而纤维样品在0°和180°处观察到的峰表明平行于纤维轴方向的(100)和(020)平面的择优取向。随着拉伸的增加,峰的强度也增加,表明在较高的施加拉伸下更明显的取向。如图5(h)~图5(i)所示,一方面,DMSO诱导的PEDOT的π-π堆积距离的缩短增加了电导率,但没有增加凝固浴样品中的取向;另一方面,拉伸诱导的取向有效地对齐PEDOT和PSS链沿着纤维轴,导致电导率和杨氏模量相当线性的增加;同样表明通常电导率最高的纤维在拉伸时也是最硬的,见图5(j)。同样,Wang等[44]将PEDOT:PSS纺丝液泵入DMAc/H2O/MSA凝固浴体系,进行20%的热拉伸后制备出的纤维电导率达到了4128 S/cm。![]() 图 5 拉伸对湿纺PEDOT:PSS纤维性能的影响[48]:(a) PEDOT:PSS膜;(b)对PEDOT:PSS纤维进行拉伸; (c)进一步拉伸的WAXS分析;(d) 归一化强度(相对于PSS宽峰)与2θ的关系;(e) PEDOT:PSS晶体结构的示意图;(100)反射(f)和(020)反射(g)的方位角的函数;电导率(h)、杨氏模量(i)与聚合物链取向的关系;(j) 电导率与杨氏模量的关系ψ—Azimuth angleFigure 5. Effect of drawing on the properties of wet-spun PEDOT:PSS fibers[48]: 2D WAXS pattern of PEDOT:PSS film (a), drawing on PEDOT:PSS fibers (b), further drawing (c), normalized intensity (concerning the PSS broad hump) versus 2θ ; (e) Scheme of the PEDOT:PSS crystal structure intensity as a function of azimuthal angle for (100) reflections (f) and (020) reflections (g) correlation; Electrical conductivity (h) and Young’s modulus (i) versus polymer chain orientation; (j) Correlation between electrical conductivity versus Young's modulus
图 5 拉伸对湿纺PEDOT:PSS纤维性能的影响[48]:(a) PEDOT:PSS膜;(b)对PEDOT:PSS纤维进行拉伸; (c)进一步拉伸的WAXS分析;(d) 归一化强度(相对于PSS宽峰)与2θ的关系;(e) PEDOT:PSS晶体结构的示意图;(100)反射(f)和(020)反射(g)的方位角的函数;电导率(h)、杨氏模量(i)与聚合物链取向的关系;(j) 电导率与杨氏模量的关系ψ—Azimuth angleFigure 5. Effect of drawing on the properties of wet-spun PEDOT:PSS fibers[48]: 2D WAXS pattern of PEDOT:PSS film (a), drawing on PEDOT:PSS fibers (b), further drawing (c), normalized intensity (concerning the PSS broad hump) versus 2θ ; (e) Scheme of the PEDOT:PSS crystal structure intensity as a function of azimuthal angle for (100) reflections (f) and (020) reflections (g) correlation; Electrical conductivity (h) and Young’s modulus (i) versus polymer chain orientation; (j) Correlation between electrical conductivity versus Young's modulus拉伸处理工艺的原理就是通过施加外力来使纤维发生塑性变形,在拉伸过程中,纤维内部的分子链沿着拉伸方向取向排列,进而增加分子间的相互作用力来提高纤维的导电性和力学性能。对PEDOT:PSS基纤维而言,拉伸后纤维内部的分子进一步紧密排列,从而减少缺陷,改善纤维的导电性和热稳定性。
2.3.3 热处理
在湿法纺丝工艺中,热处理也是重要的后处理工艺之一,是将PEDOT:PSS基纤维置于一定温度下加热或者保温处理的过程。一般热处理温度为30~50℃,保温时间需要根据调控的热稳定性和结晶度来选择合适的温度和处理时间。对纤维进行热处理的过程中,纤维受热促进了分子链的有序排列,改善了分子间的堆积密度并提高了纤维的结晶度,改变了纤维的结构和形貌。Wang等[49]在EtOH-H2O-Cu2+凝固浴制备具有稳定核壳结构的纤维,在30℃下静置6~12 h后,纤维表面出现籽晶生长和纹理状结构,最终形成特殊的类织构结构。通过控制热处理温度和时间,可以使PEDOT:PSS纤维的晶粒尺寸和分布等变化,进而调控纤维的力学性能和导电性能。
2.3.4 光照刺激
光照刺激在湿法纺丝工艺中也是一种常见的后处理步骤,通过调节红外烘灯的温度和照射时间及样品到烘灯的距离,通常温度在30~50℃,距离为20~50 cm,根据需要调控热电性能和表面性质,选择合适的光照强度和照射时间。紫外光或者红外光刺激改善了PEDOT:PSS基纤维的构象,改变了纤维表面的形貌,促进了电荷的运输和载流子的产生,进一步改善纤维的导电性能和稳定性。
目前,通过多项后处理工艺的配合来提升纤维的电导率是更常见的,Wang等[50]通过EtOH-H2O-Cu2+凝固浴体系和羟基脲溶液两步处理结束后进行保温和在红外烘灯的处理,获得了三层核壳复合结构的纤维,电导率高达5.2×104 S/cm。如图6(a)~图6(c)所示,温度对PEDOT:PSS基纤维有着显著的影响,用红外灯照射纤维,发现纤维的电阻发生了变化。同时,纤维的电阻变化随红外灯的距离而变化。除电阻变化外,纤维电阻的响应时间随红外灯的开/关而变化,此外,如图6(d)~图6(e)所示,在红外灯的周期性开关状态下,纤维的电阻信号是准确和可重复的,得益于纤维对温度的传感和响应,PEDOT:PSS基纤维有望在仿生手臂领域表现出巨大的潜力。同时,Wang等[49]通过EtOH-H2O-Cu2+凝固浴制备出的复合纤维进行保温和在红外烘灯的处理下获得了具有织构的核-壳结构。其中,核壳结构纤维的相分离在凝固浴中同步完成,而晶种的产生和类织构结构的生长是在红外灯下干燥形成的,进一步的保温处理,最终形成了特殊的纹理状结构。令人惋惜的是,热处理和光照刺激的这些工艺一般只能提升纤维的导电性,而不能改善纤维的可拉伸性。这是由于PEDOT:PSS基纤维在纺丝过程中内部的分子链已经排列完成,很难再调整分子链的取向,只能改善分子链的结构,这是热处理和光照刺激工艺的局限性。
![]() 图 6 (a) 红外灯照射PEDOT:PSS基纤维图示;(b) 纤维在不同距离下的电阻变化(ΔR/R0);(c)纤维电阻变化的响应时间;(d) 纤维在相同距离(D = 20 cm、T = 50℃)红外灯的100次周期性开/关下的传感性能;(e) 纤维用于仿生手臂感知压力和温度的概念应用[49]Figure 6. (a) Demonstration of PEDOT:PSS-based fibers irradiated by infrared lamp; (b) Resistance changes (ΔR/R0) of fibers at different distances; (c) Response time of fibers resistance change; (d) Sensing performance of composite fibers during 100 lamp on-off cycles at the same distance (D = 20 cm, T = 50℃); (e) Fibers are used for concept application of bionic arms sensing pressure and temperature[49]
图 6 (a) 红外灯照射PEDOT:PSS基纤维图示;(b) 纤维在不同距离下的电阻变化(ΔR/R0);(c)纤维电阻变化的响应时间;(d) 纤维在相同距离(D = 20 cm、T = 50℃)红外灯的100次周期性开/关下的传感性能;(e) 纤维用于仿生手臂感知压力和温度的概念应用[49]Figure 6. (a) Demonstration of PEDOT:PSS-based fibers irradiated by infrared lamp; (b) Resistance changes (ΔR/R0) of fibers at different distances; (c) Response time of fibers resistance change; (d) Sensing performance of composite fibers during 100 lamp on-off cycles at the same distance (D = 20 cm, T = 50℃); (e) Fibers are used for concept application of bionic arms sensing pressure and temperature[49]由此可见,通过湿法纺丝制备纤维时,纺丝液设计、凝固浴调控、后处理3个工艺都是至关重要的环节,通过这3个工艺相互配合,才能进一步提升纤维的综合性能。纺丝液设计的优化可以确保纤维本身的稳定性和可纺性,合理的凝固浴调控可以促进纤维结构的固化和成型,适当的后处理则进一步提升纤维的综合性能。只有这样,湿法纺丝纤维的性能才能够得到最大化的提升,以满足柔性电子领域的需求和应用要求,从而拓展其在柔性电子器件领域中的应用前景。
3. PEDOT:PSS基纤维在柔性电子器件中的应用
3.1 可穿戴电子织物
随着柔性电子技术的迅速发展,PEDOT:PSS基纤维被证明在柔性电子领域具有重要的潜在应用,可穿戴电子[51]也成了研究的热门方向,电子织物为穿戴者提供各种功能,如健康监测[52]、通信应用[53]等。Gao等[43]采用At-IPA-Fe3+凝固浴体系制备出牢固可编的PEDOT:PSS基纤维,通过引入铁离子,纤维的最大拉伸断裂强度为
1263.1 MPa,获得了高强度、高导电性的PEDOT:PSS基纤维,其优异的力学性能促进了其在电子织物中的应用,并使织物能够承受恶劣的机械环境,也可以用来传输信息,将其编织到织物中。Wen等[45]采用连续湿法纺丝工艺制备PEDOT:PSS基纤维,再用H2SO4一步处理。室温下功率因数达到了147.8 μW/(m·K–2), 塞贝克系数为19.2 μV/K,还表现出389.5 MPa的高抗拉强度和305%的大突发应变,使纤维在先进的可穿戴织物中的应用有很大的希望。这些方法通过优化每一步工艺制备的高拉伸导电纤维的同时,也增加了成本。可穿戴电子织物面临的挑战是在保持高导电性的同时,要有一定的耐久性并且要降低电子织物的功耗,还要确保在使用过程的安全性。为了解决上述的问题,研究人员还需要探索材料改性的新方法,例如添加稳定的纺丝成型剂或者通过表面改性来提高PEDOT:PSS基纤维的稳定性和耐久性;为了避免纤维受到环境因素的影响,可以开发新型的柔性封装技术来有效应对PEDOT:PSS基纤维在柔性电子织物中的挑战以促进相关领域的进一步发展。未来随着个性化需求的增加,智能化的可穿戴电子织物将成为未来重要的发展趋势。
3.2 纤维基柔性传感器
纤维基柔性传感器具有高度的柔韧性和可塑性,能够适应各种复杂的曲面结构并实现个性化应用。Chen等[54]利用纺丝液垂直泵入EtOH-H2O-H3PO4凝固浴体系制备出高度可拉伸和弹性的PEDOT:PSS螺旋纤维,具有较高的伸长率(>950%)、优异的导电性(650 S/cm)和即使在变形高达400%时仍具有显著的弹性,使可穿戴传感器成为可能。Chen等[55] 采用1-乙基-3-甲基咪唑二氰胺(EMM:DCA)/PEDOT : PSS (ED/P)纺丝原液从微针挤出到异丙醇(IPA)凝固浴后用H2SO4后处理制备出ED/P复合纤维,ED/P纤维具有更高的电导率(
4288 S/cm)、拉伸强度(956 MPa)和更低的杨氏模量(3.8 GPa),功率因数达到85.5 μW/(m·K–2),可用于热电(TE)器件和温度传感器,具有优异的性能和广泛的应用前景。纤维基柔性传感器虽然前景广阔,但仍存在诸多问题,如柔性传感器的灵敏度和使用的稳定性与耐久性及与其他电子设备集成的兼容性。为了解决目前存在的问题,通过调控纤维的结构和取向来改进纤维的导电性,并对纤维和电极材料之间的界面进行优化,减小接触电阻来提升电学性能。未来,纤维基传感器会更加轻薄、智能、安全,更加全面的为人们监测人体生理信号、运动参数等,在医疗保健、工业应用等领域具有广泛的应用前景。
3.3 纤维基超级电容器
纤维基超级电容器有着高功率密度、优异的导电性能和良好的温度适应性。Wang等[44]将PEDOT:PSS纺丝液泵入DMAc/H2O/MSA凝固浴体系,再进行20%的热拉伸后浸泡在H2SO4后用DMAc洗涤制备出的纤维,在10 A/cm3时的体积电容为188.5 F/cm3,在
3000 A/cm3时的功率密度为3.58×105 mW/cm3,在1000 A/cm3的超高电流密度下,充放电循环寿命超过200万次,并且经过100万次循环后,电容保持率仅损失11%,集成的微型超级电容器阵列可以在4.5 cm2的小面积内产生134.9 V的高输出电压。Huang等[56]采用湿法纺丝和溶液反应合成了镍钴层状双氢氧化物(NiCo-LDH)包覆水性聚氨酯(WPU)/PEDOT:PSS纤维的可缝合核壳纤维电极,所制备的LDH/PEDOT:PSS纤维无论在干态(1237.3 S/cm)还是湿态(1018.7 S/cm)都具有很大的电导率,表现出高电容(1 A/g时为188.5 F/g)和长寿命(10000 次循环后电容保持率为94%),显示出极好的柔性,在变形下具有稳定的电容行为。这些特性表明LDH/PEDOT:PSS纤维具有稳定的高性能能量存储的潜力,以支持可穿戴电子设备。纤维基超级电容器通常采用高表面积的纳米材料等作为电极材料,通过纤维结构实现大表面积和灵活性的结合,其能量密度和功率密度相对较低及在长时间使用过程中出现的电容量衰减、循环寿命下降等问题,其稳定性和耐久性不足成为制约其商业化应用的重要因素。针对当前面临的挑战,研究人员可以通过设计纳米结构的PEDOT:PSS纤维电极来增加比表面积,提高储能能力和电荷传输速率。这种设计使超级电容器可以与纺织品相融合,实现柔性、轻质、舒适的特性,从而拓展了超级电容器在可穿戴电子设备和智能纺织品中的应用潜力。
4. 结论与展望
聚(3, 4-乙烯二氧噻吩):聚(苯乙烯磺酸盐)(PEDOT:PSS)作为当下应用最广泛的导电高分子而备受科研人员的关注,由于具有导电性高、可加工性好等特点,被认为是未来最有发展潜力的导电高分子。本文综述了近年来湿法纺丝PEDOT:PSS基纤维的制备与应用。随着湿法纺丝工艺的不断改良和创新,PEDOT:PSS基纤维在柔性电子领域的应用会极大的拓展。然而,湿法纺丝制备的PEDOT:PSS基纤维存在可拉伸性差、截面不规则、导电稳定性差等问题,无法满足柔性电子器件领域高灵敏度、快速响应等需求。在未来可以从以下几个方面展开研究:
(1)开发更高效、更绿色的纺丝液和凝固浴及纺丝添加剂,提升纤维性能的同时需要更加注重对环境的影响;
(2)借助计算机模拟计算,考虑湿法纺丝工艺参数和成本等因素,设计研发纤维的智能化制造,助力实现智能纺织品产业的可持续发展;
(3)重点发展功能性纤维,如防水、防火、抗菌等功能,以满足未来消费者对智能穿戴产品的个性化需求。
相信在未来科研人员对湿法纺丝工艺探索的不断深入,湿法纺丝PEDOT:PSS基纤维的性能将会得到全面的提升,应用场景和领域也会进一步拓展。
-
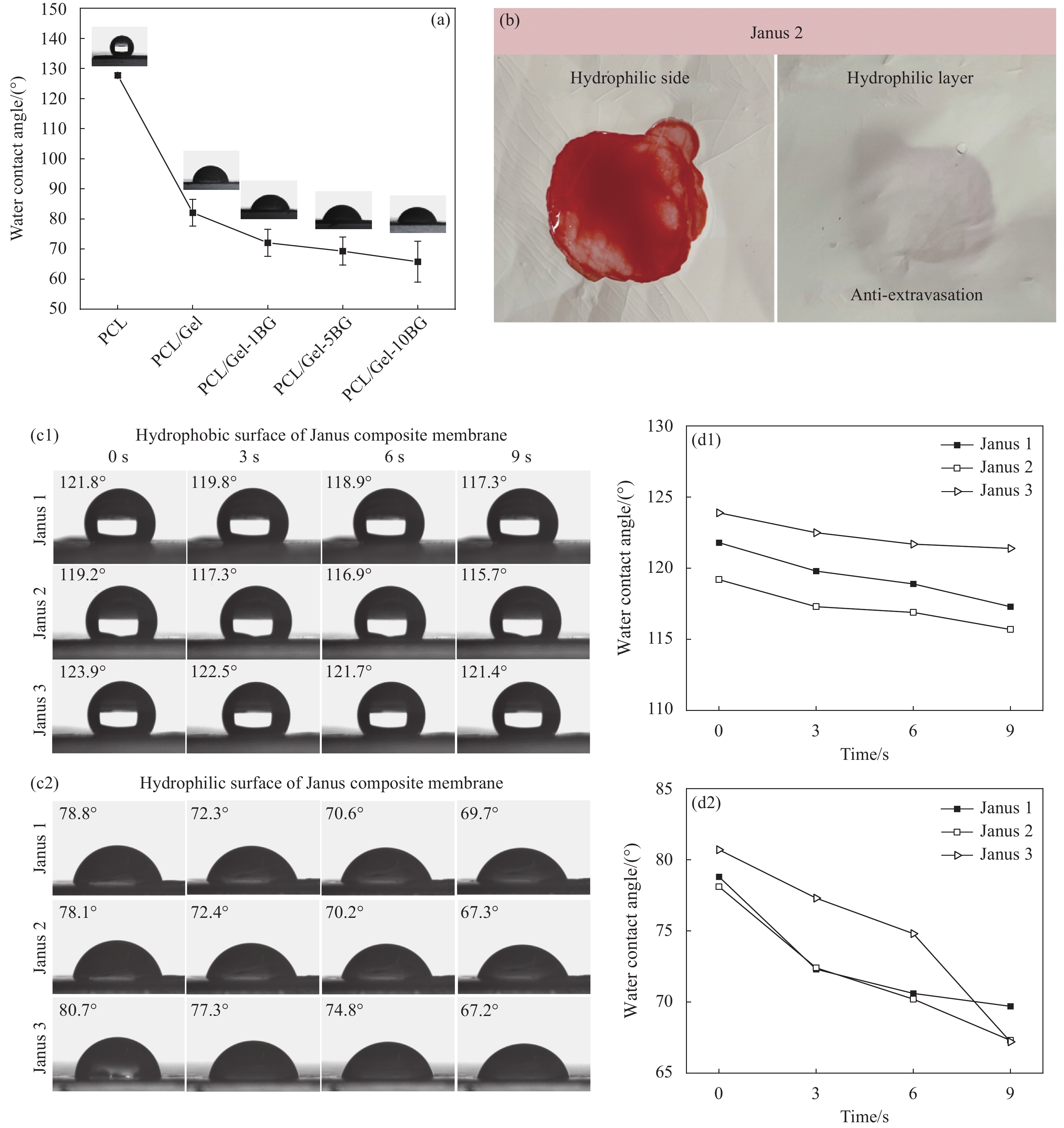
图 6 不同纳米纤维膜润湿性(a); Janus2复合膜的血液渗透性(b); Janus复合膜疏水面(c)和亲水面(d)水接触角以及渗透性
Figure 6. Wettability of different nanofiber membranes (a); Blood permeability of Janus2 composite membrane (b); Hydrophobic (c) and hydrophilic (d) water contact Angle and permeability behavior of different Janus composite membranes
表 1 不同Janus复合膜的组成
Table 1 Composition of different Janus composite membranes
Sample Outer layer Inter layer Inner layer Janus1 PCL PCL/Gel-1G PCL/Gel Janus2 PCL PCL/Gel-5BG PCL/Gel Janus3 PCL PCL/Gel-10BG PCL/Gel Notes: PCL—Polycaprolactone; Gel—Gelatin 表 2 不同纳米纤维膜的静电纺丝条件
Table 2 Electrostatic spinning conditions for different nanofibre membranes
Solution Needle-Collector
Distance/cmVoltage/
kVFlow Rate/
(mL·h−1)PCL 12 20 3.5 PCL/Gel 15 15 0.4 PCL/Gel-1BG 15 15 0.4 PCL/Gel-5BG 15 15 0.4 PCL/Gel-10BG 15 15 0.4 -
[1] CHAMBERS E S, VUKMANOVIC-STEJIC M. Skin barrier immunity and ageing[J]. Immunology, 2020, 160(2): 116-125. DOI: 10.1111/imm.13152
[2] 张天蔚, 刘方, 田卫群. 促皮肤创面愈合新型敷料研究现状与进展[J]. 生物医学工程学杂志, 2019, 36(6): 1055-1059+1068. DOI: 10.7507/1001-5515.201811023 ZHANG T W, LIU F, TIAN W Q. Research Status and Progress on New Dressings for Promoting Skin Wound Healing[J]. Journal of Biomedical Engineering, 2019, 36(6): 1055-1059+1068(in Chinese). DOI: 10.7507/1001-5515.201811023
[3] KIM H J, PARK J, KIM S K, et al. Autophagy: Guardian of Skin Barrier[J]. Biomedicines, 2022, 10(8): 1817. DOI: 10.3390/biomedicines10081817
[4] CIOCE A, CAVANI A, CATTANI C, et al. Role of the Skin Immune System in Wound Healing[J]. Cells, 2024, 13(7): 624. DOI: 10.3390/cells13070624
[5] PATRICK A L, CHEN-CHARPENTIER B. Building erudition in the wound healing process: an inflammation model analysis[J]. International Journal of Computer Mathematics, 2024: 1–20.
[6] LAN J Z, SHI L X, XIAO W Y, et al. An enhanced fractal self-pumping dressing with continuous drainage for accelerated burn wound healing[J]. Frontiers in Bioengineering and Biotechnology, 2023, (11): 1188782.
[7] SAITO1 C T M H, BERNABÉ2 P F E, OKAMOTO3 T, et al. Evaluation of tissue response to periodontal dressings: histological study in tooth sockets of rats[J]. Journal of Applied Oral Science, 2008, 16(3): 219-25. DOI: 10.1590/S1678-77572008000300011
[8] NYGREN E, GEFEN A. Little news is good news? What is missing in the recently published EN 13726: 2023 test standard for wound dressings[J]. International Wound Journal, 2024, 3(21): e14787.
[9] BOATENG J, CATANZANO O. Advanced Therapeutic Dressings for Effective Wound Healing—A Review[J]. Journal of Pharmaceutical Sciences, 2015, 104(11): 3653-3680. DOI: 10.1002/jps.24610
[10] SHEOKAND B, VATS M, KUMAR A, et al. Natural polymers used in the dressing materials for wound healing: Past, present and future[J]. Journal of Applied Polymer Science, 2023, 61(14): 1389-1414. DOI: 10.1002/pol.20220734
[11] Chen Fan, Qing Xu, Ruiqi Hao, et. al. Multifunctional wound dressings based on silicate bioactive materials[J]. Biomaterials, 2022, 287.
[12] BOATENG J, CATANZANO O. Advanced Therapeutic Dressings for Effective Wound Healing—A Review[J]. Journal of Pharmaceutical Sciences, 2015, 104(11): 3653-3680. DOI: 10.1002/jps.24610
[13] LI X N, WANG X N, ZHENG L X, et al. Smart Janus textiles for biofluid management in wearable applications[J]. IScience, 2024, 27(3): 2589-0042.
[14] HOU L, LIU J, LI D, et al. Electrospinning Janus Nanofibrous Membrane for Unidirectional Liquid Penetration and Its Applications[J]. Chemical Research in Chinese Universities, 2021, 37: 337-354. DOI: 10.1007/s40242-021-0010-4
[15] 刘思彤, 金丹, 孙东明, 等. 静电纺丝制备Janus微纳米纤维研究进展[J]. 复合材料学报, 2024, 41(5): 2321-2332. LIU Sitong, JIN Dan, SUN Dongming, et al. Advances in the preparation of Janus micro and nanofibres by electrostatic spinning[J]. Acta Materiae Compositae Sinica, 2024, 41(5): 2321-2332(in Chinese).
[16] ZHANG Z, LI W, LIU Y, et al. Design of a biofluid-absorbing bioactive sandwich-structured Zn–Si bioceramic composite wound dressing for hair follicle regeneration and skin burn wound healing[J]. Bioactive materials, 2021, 6(7): 1910-1920. DOI: 10.1016/j.bioactmat.2020.12.006
[17] ZHANG M, CHU L, CHEN J, et al. Asymmetric wettability fibrous membranes: Preparation and biologic applications[J]. Composites Part B: Engineering, 2024, 269: 1359-8368.
[18] Woodruff M A, Hutmacher D H. The return of a forgotten polymer—Polycaprolactone in the 21st century[J]. Progress in Polymer Science, 2010, 35(10): 1217-1256. DOI: 10.1016/j.progpolymsci.2010.04.002
[19] Nair L S, Laurencin C T. Biodegradable polymers as biomaterials[J]. Progress in Polymer Science, 2007, 32(8-9): 762-798. DOI: 10.1016/j.progpolymsci.2007.05.017
[20] SASMAL P K, GANGULY S. Polymer in hemostasis and follow-up wound healing[J]. Applied Polymer, 2023, 140(9).
[21] DEMIR A U, AHI Z B, SANCAKLI A, et al. A comparative study of gelatin-based nanofiber and sponge wound dressings[J]. Journal of Bioactive and Compatible Polymers, 2024, 39(3): 145-161 DOI: 10.1177/08839115241241297
[22] ZAHID S, SHAH A T, JAMAL A, et al. Biologcal behavior of bioactive glasses and their compsites[J]. RSC Advances, 2016, 6(74): 70197-70214. DOI: 10.1039/C6RA07819B
[23] OSTOMEL T A, SHI Q, STUCKY G D. Oxide Hemostatic Activity[J]. Journal of the Am-erican Chemical Society, 2006, 128(26): 8384-8385. DOI: 10.1021/ja061717a
[24] BOKOV D, JALIL A T, CHUPRADIT S, et al. Nanomaterial by Sol-Gel Method: Synthesis and Application[J]. Advances in Materials Science and Engineering, 2021.
[25] CORREIA T R, ANTUNES B P, CASTILHO P H, et al. A bi-layer electrospun nanofiber membrane for plasmid DNA recovery from fermentation broths[J]. Separation and Purification Technology, 2013, 112: 20-25. DOI: 10.1016/j.seppur.2013.03.049
[26] LIU J, XIE X, WANG T, et al. Promotion of Wound Healing Using Nanoporous Silk Fibroin Sponges[J]. ACS Applied Materials & Interfaces, 2023, 15(10): 12696-12707.
-
其他相关附件
-
本文图文摘要
点击下载
-
-
目的
伤口愈合时敷料不仅需要提供止血作用,还需吸收过多的渗出物为伤口提供一个相对湿润又不过于干燥的环境。而传统纱布敷料的功能较为单一,无法为伤口提供良好的愈合环境。所以需要开发具有止血、能屏蔽外界有害微生物、能吸收大量渗出液等多个协同功能的敷料。
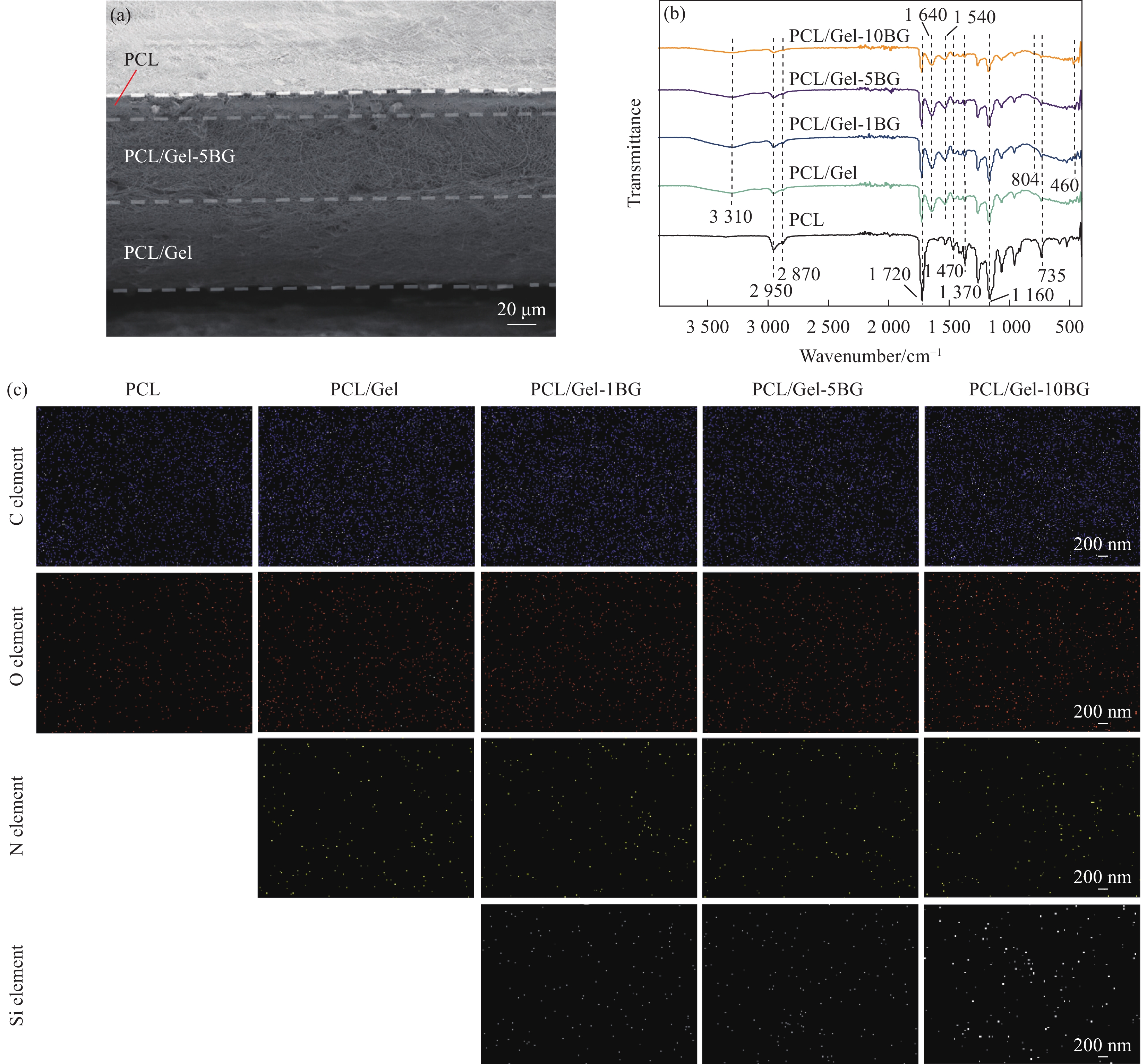
方法复合膜的制备主要由三个步骤组成:(1)采用微乳液-溶胶凝胶法合成生物玻璃纳米颗粒BG;(2)利用甲酸(FA)与乙酸(AA)混合溶液FA:AA (70:30 v/v)作为溶剂制备纯聚己内酯(PCL)、聚己内酯/明胶混合溶液(PCL/Gel)以及掺入不同生物玻璃的混合溶液(PCL/Gel-BG(1%、5%、10%))五种静电纺丝液;(3)将纺丝液通过静电纺丝技术以及逐层叠加法得到三明治结构的Janus复合膜,其中外层为PCL纳米纤维膜,中间层为负载BG的纳米纤维膜(PCL/Gel-BG),内层为PCL/Gel纳米纤维膜。通过SEM、FTIR、EDS等生物玻璃及复合膜形貌和结构进行了表征,测试了Janus复合膜力学性能、孔隙率、溶胀率以及渗透性等,通过对比传统止血纱布的血液吸收率、止血时间、凝血指数等测试探究了其止血性能。
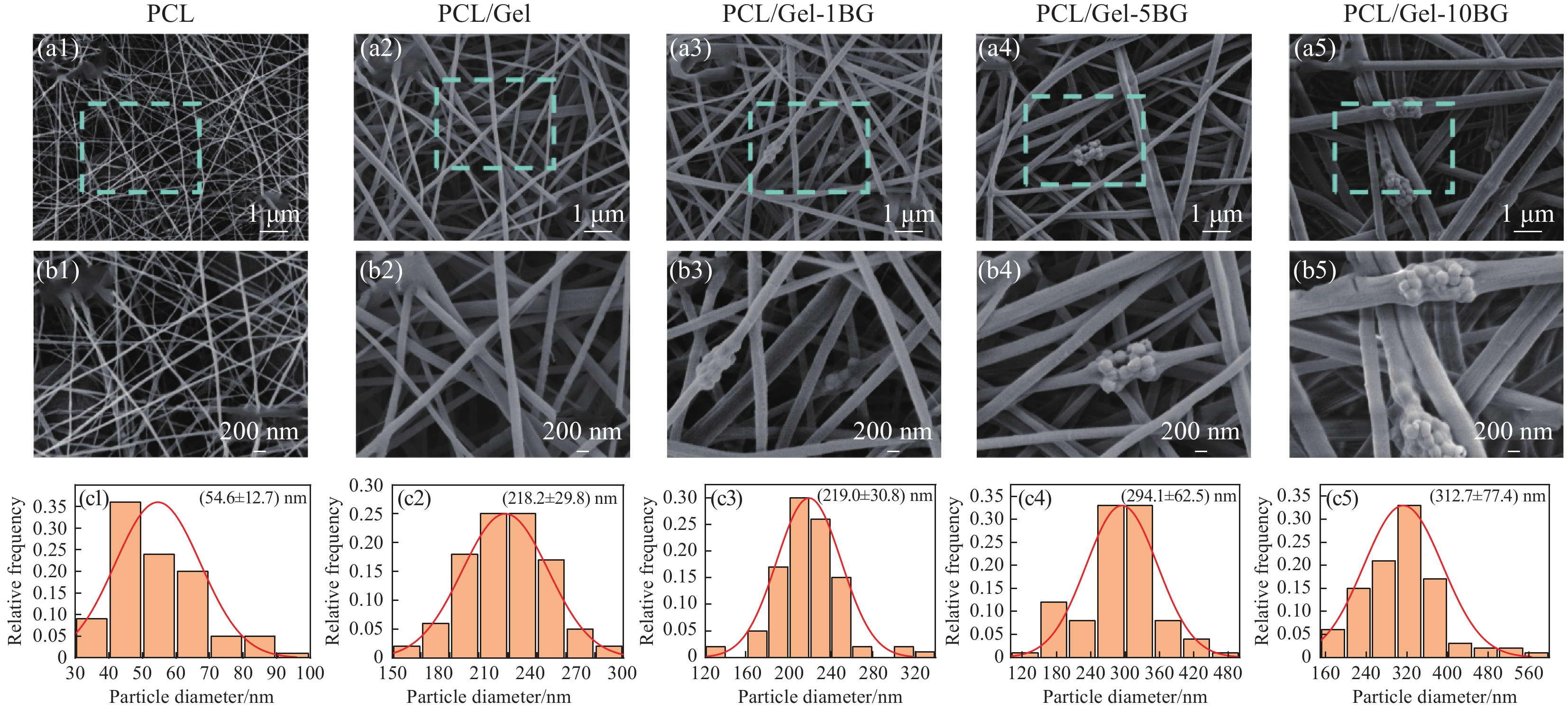
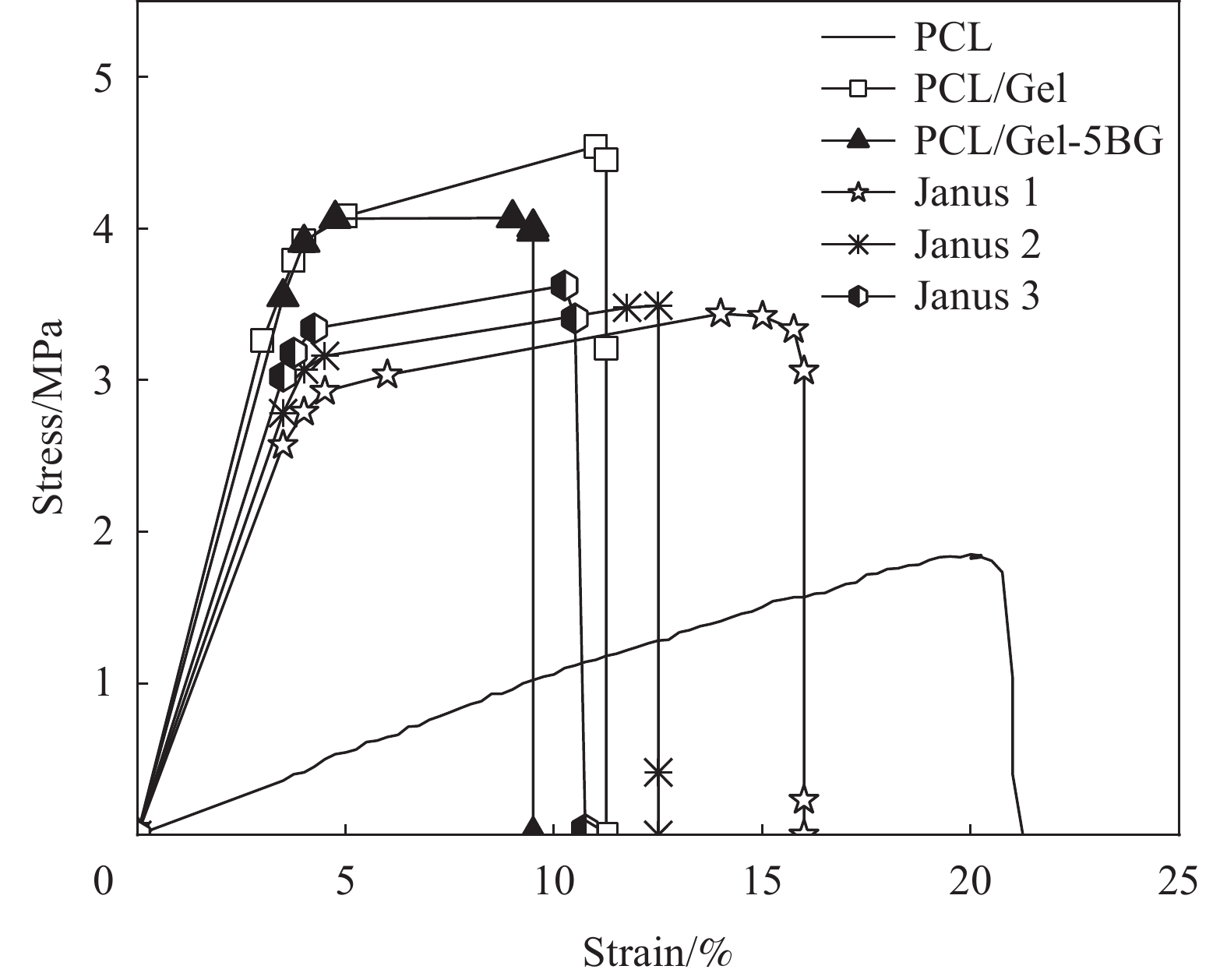
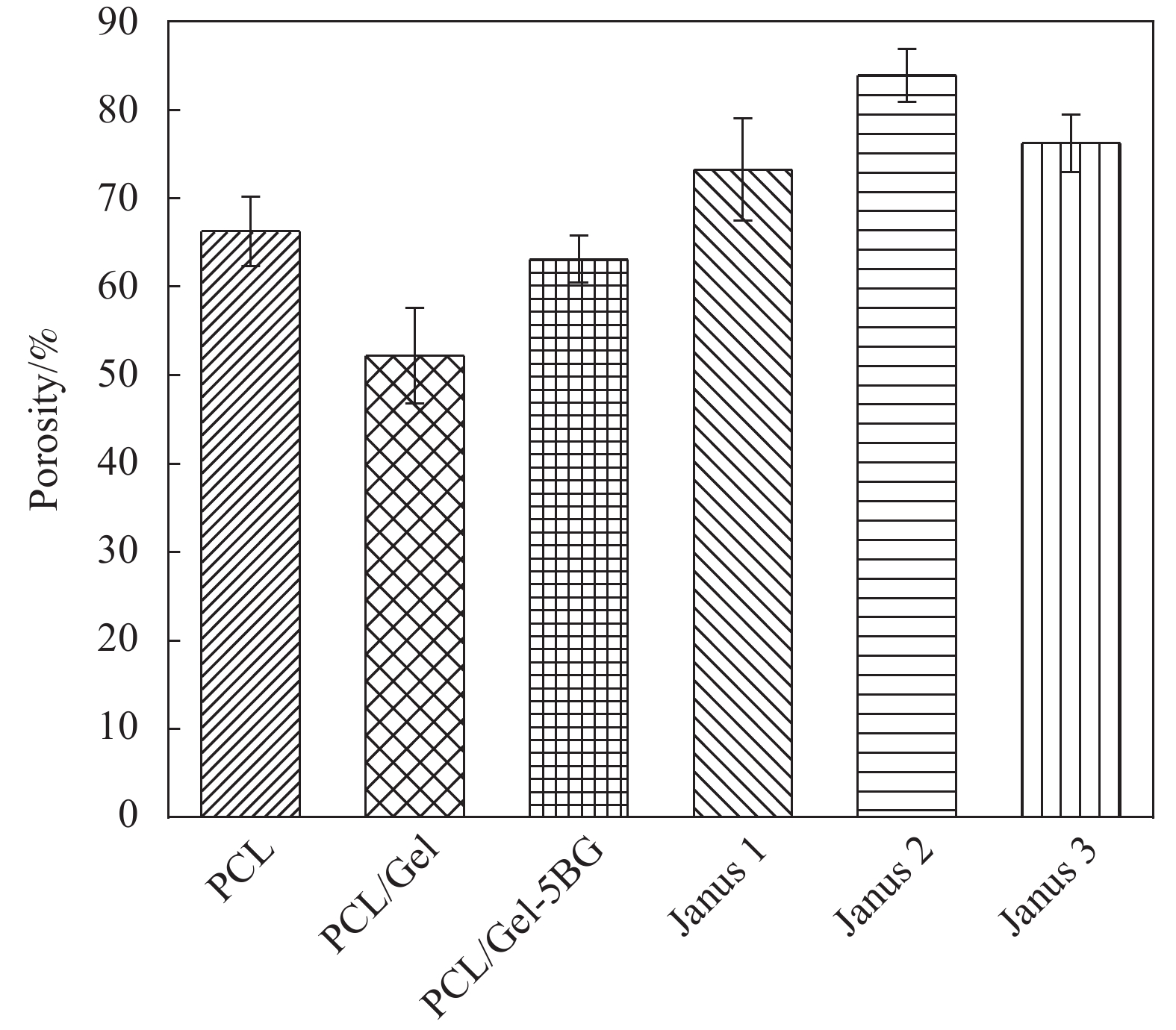
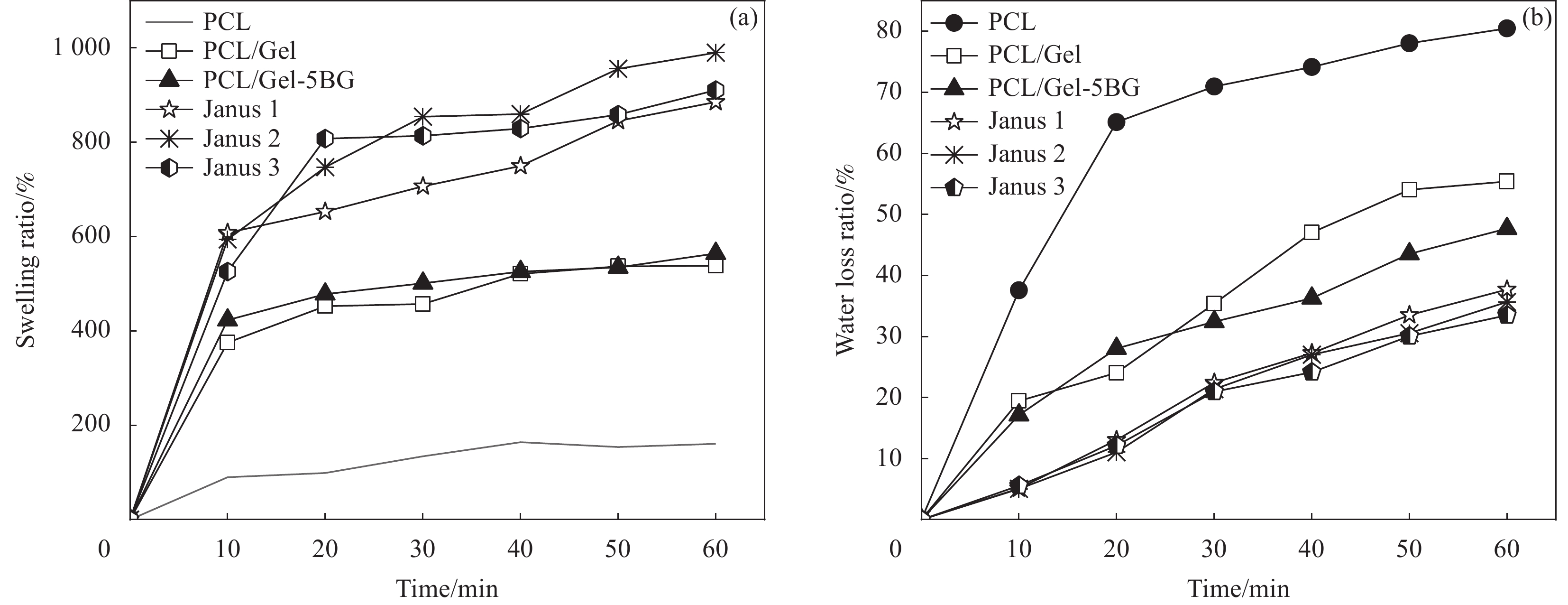
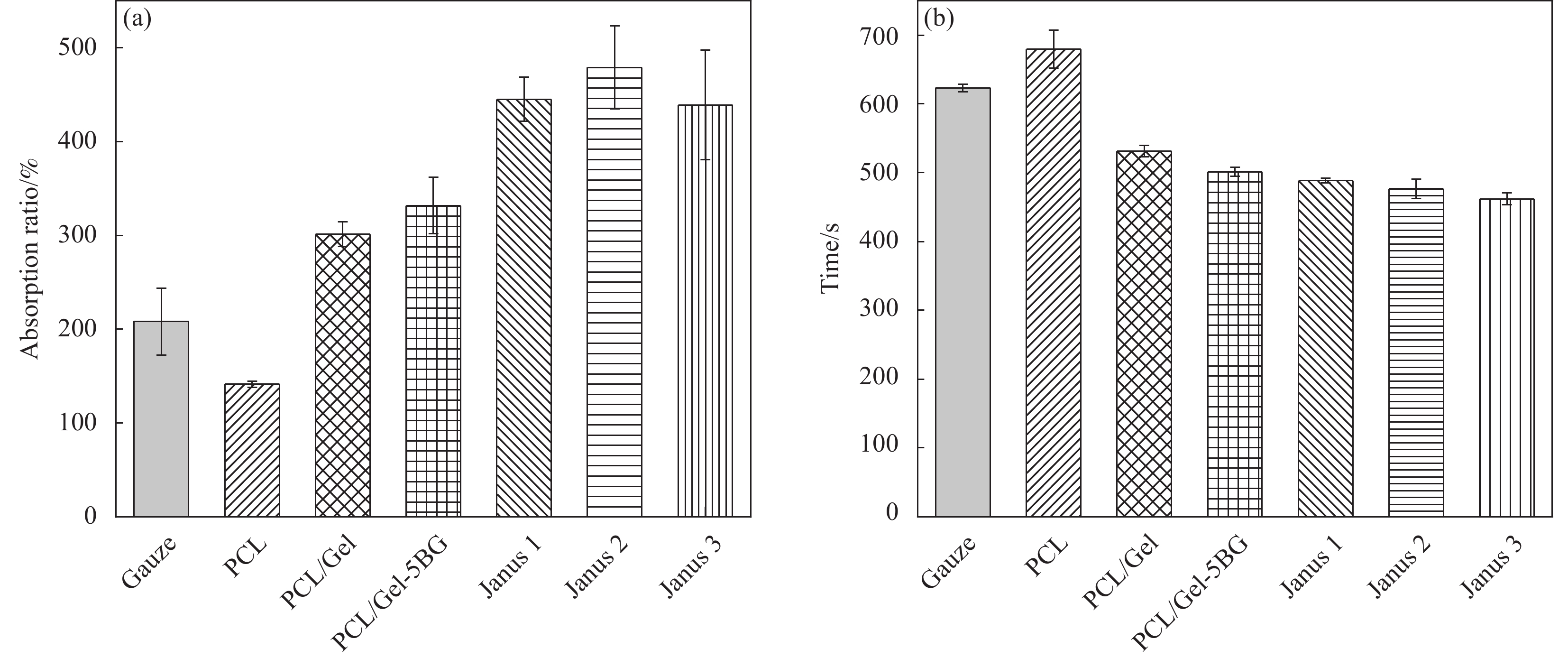
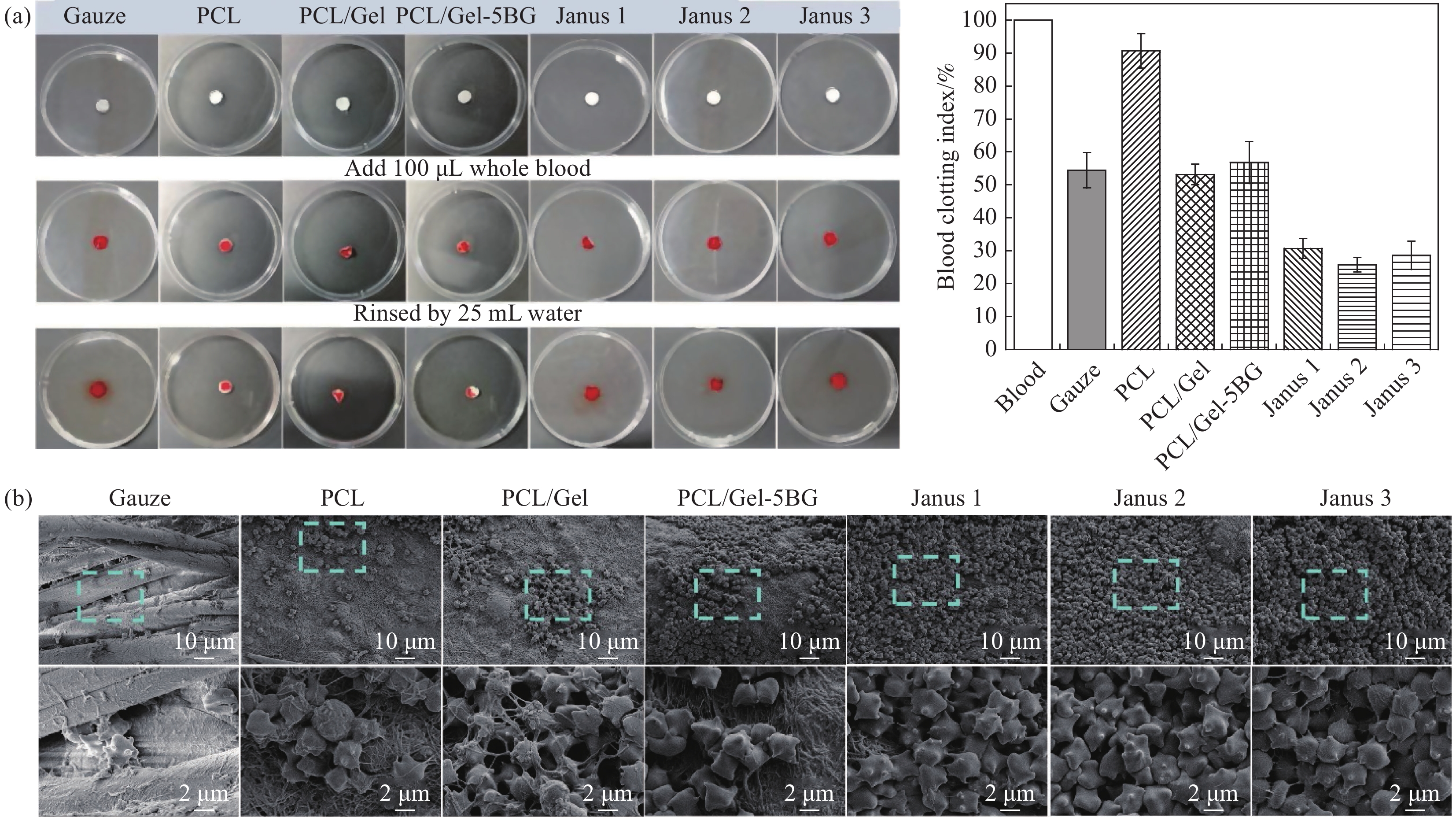
结果从SEM可见BG粒径大小均匀呈光滑的球形结构,平均粒径为(227.1 ± 19.1) nm;Janus复合膜的每层纤维表面光滑,无串珠结构,生物玻璃的掺入影响了纤维直径,且纤维直径随其掺入量增加而增大。Janus复合膜截面的SEM图可以看出复合膜三层之间粘结良好无分层现象。力学性能测试结果表明:复合膜断裂强度均大于3.5 MPa,在人体正常皮肤的拉伸强度(约2.5—16 MPa)范围内,断裂伸长率均在10%以上,表现出比单层纤维膜更好的力学性能;孔隙率均在70%以上,符合伤口敷料(60%—90%)理想孔隙率范围要求;润湿性和渗透性证明了Janus复合膜具有不对称润湿性,使其亲水面能快速吸收液体且疏水面可以抗血液外渗;其中中间层相对含量为5%BG的Janus2复合膜吸收渗出液的能力最佳,其溶胀率可高达990%。此外,Janus复合膜在止血性能测试中表现出比传统止血纱布更佳的止血效果。具体表现为:在血液吸收率测试中Janus1、Janus2、Janus3复合膜高达445.2%、479.1%、439.2%远高于纱布(208.1%),体外凝血指数分别为30.7%、25.7%、28.6%低于纱布(54.4%),体外凝血时间分别约为488 s、476 s、462 s相对纱布623s减少近2.5 min。综上,本文制备的Janus复合膜在止血方面表现出比纱布更优异的性能。
结论本研究成功利用静电纺丝技术制备了一种具有不对称润湿性的三明治结构敷料。将生物玻璃纳米颗粒负载于敷料的中间层纤维膜,不但提高了敷料的溶液吸收,还增强了其凝血效果。此外,该敷料不仅具有与细胞质基质相似的结构,还具有较高的孔隙率,同时还兼具较好的溶液吸收、保湿能力,能为伤口提供相对湿润又不过与干燥的愈合环境加速伤口愈合。有望作为新型创面敷料应用于伤口愈合领域。
-
随着科技的发展,创面敷料的种类越来越多,尤其是多功能的敷料研究受越来越多研究者的关注。理想的创面敷料不仅需要促进伤口愈合,还应具有吸收伤口渗出液、减少细菌的病毒感染等功能,同时还能为伤口提供相对湿润而不过与干燥的环境。然而,目前应用于临床医学的敷料功能都比较单一。
本文通过利用静电纺丝技术,以PCL纤维膜为疏水外层,PCL/Gel混合静电纺纤维膜作为亲水内层,在PCL/Gel溶液中掺入不同含量的生物玻璃所得到的PCL/Gel-BG纤维膜作为中间层,制备具有高效液体吸收、止血协同作用的Janus复合膜。所制备的复合膜具有不对称润湿性,不仅使其溶胀率可高达990%,能吸收大量渗出液,同时还能提供更利于伤口愈合的相对湿润而不脱水的微环境。此外,掺入中间层自制的高硅钙比的硅基无机生物玻璃,不仅能提高吸收溶液能力,还增大了复合膜孔隙率,同时还释放凝血因子加速止血。在血液吸收率测试中Janus1、Janus2、Janus3复合膜高达445.2%、479.1%、439.2%远高于纱布(208.1%),体外凝血指数分别为30.7%、25.7%、28.6%低于纱布(54.4%),体外凝血时间分别约为488 s、476 s、462 s相对纱布623s减少近2.5 min。
单层纤维膜及Janus复合膜的润湿性(a);溶胀率(b); 血液渗透性(c); 凝血时间(d)






 下载:
下载: